成纤维细胞生长因子1对糖尿病小鼠下颌下腺增殖细胞核抗原表达的影响
2017年5月
中华儿科杂志,第52卷第5期 第294页-第299页
周稚辉,施璐,郎淼杰,陈紫璐,王彦亮,何帅
口干是糖尿病主要临床症状之一。下颌下腺是主要唾液分泌器官,分泌70%的唾液。已有研究显示,糖尿病性口干与下颌下腺结构损伤及功能降低相关[1,2]。糖尿病可能通过促进下颌下腺细胞凋亡,抑制增殖,导致腺体萎缩、分泌功能减弱[3,4]。增殖细胞核抗原(proliferating cell nuclear antigen,PCNA)是细胞增殖和凋亡相关的重要因子[5,6,7,8]。糖尿病能使下颌下腺PCNA表达明显降低,且随病程延长,PCNA表达进一步被抑制[9]。成纤维细胞生长因子1(fibroblast growth factor 1,FGF-1)是成纤维细胞生长因子家族的重要成员,有较强的促增殖作用,能刺激血管生长、加速创伤愈合以及促进神经损伤修复[10,11,12]。近年研究显示FGF-1有调节血糖代谢的功能[13,14,15]。对饮食诱导的糖尿病小鼠单次注射FGF-1蛋白,可使血糖恢复至正常,同时FGF-1持续治疗不仅可有效控制血糖,还可逆转小鼠的胰岛素抵抗,且这种降血糖作用独立于促增殖作用,避免了诱发肿瘤的可能。因此,FGF-1成为糖尿病及其并发症,如糖尿病性口干的重要候选治疗药物。目前关于FGF-1对糖尿病下颌下腺组织的影响鲜见报道。本项研究通过观察PCNA在小鼠下颌下腺的表达变化,研究FGF-1对糖尿病下颌下腺细胞生存状态及功能的影响,为防治糖尿病性口干提供新思路。
本项研究时间为2014年11月至2015年9月。
2型糖尿病动物模型C57BL/KsJdb/db雄性小鼠(表型肥胖、血糖高于18.0 mmol/L)及db/m雄性小鼠由南京大学模式动物研究中心提供[动物饲养合格证号:SCXK(苏)2010-0001],FGF-1由温州医科大学基因工程药物国家工程研究中心中试研究基地提供,质量浓度为1 g/L,纯度>95%,血糖仪及血糖试纸(Omitest plus,B.Braun Melsungen,德国),HE染色液(c0105,Beyotime,上海),兔源PCNA一抗和山羊抗兔二抗(sc-2012,Santa Cruz,美国),二氨基苯联胺(diaminobenzidine,DAB)显色剂(ZLI-9019,北京中杉金桥生物技术有限公司),光学显微镜(Eclipse Ni-U,Nikon,日本)。
8周龄雄性db/db糖尿病型小鼠16只,体质量57~62 g,按随机数字表随机分为糖尿病组和给药组,每组8只;8周龄8只雄性db/m小鼠作为空白对照组。给药组小鼠按体质量2 mg/kg腹腔注射FGF-1,每2天1次,共16周。糖尿病组和空白对照组小鼠腹腔注射等量生理盐水。所有动物均饲养于温州医科大学SPF级实验动物中心,普通饲料,3组动物分笼饲养,不限制饮食饮水。
分别于实验0、4、8、12和16周用电子天平测量小鼠体质量后断尾取血,用血糖仪测定血糖值。
分别于实验0、8和16周测量唾液流率。各组小鼠测量体质量,10%水合氯醛(4 ml/kg)腹腔注射麻醉后,0.1%毛果芸香碱(0.5 mg/kg)腹腔注射,15 min后收集唾液。将小鼠保持坐位,头朝下,电子天平测量干棉球质量(W1),棉球置于小鼠下颌下腺导管开口处10 min后称重(W2),唾液流率=(W2-W1)÷10÷小鼠体质量。
实验16周后各组小鼠测量体质量,10%水合氯醛(4 ml/kg)腹腔注射,麻醉后打开胸腔,从左心室插管至升主动脉,同时剪开右心耳。生理盐水快速冲洗,4%多聚甲醛灌注固定,取双侧下颌下腺组织,拍照并称重,计算下颌下腺指数:下颌下腺指数(mg/g)=下颌下腺质量(mg)÷小鼠体质量(g)。左侧下颌下腺固定24 h,经70%、80%、95%、100%乙醇梯度脱水,二甲苯透明,浸蜡,石蜡包埋,连续切片,切片厚度为5 μm,进行常规HE染色。
切片脱蜡至水,浸于3%甲醇-过氧化氢溶液,室温孵育20 min,以清除内源性过氧化物酶活性;切片浸于0.01%枸橼酸缓冲液(pH为6.0),高压锅内加热煮沸2 min,进行抗原修复。每张切片滴加1%正常山羊血清35 μl,37 ℃恒温箱湿盒内孵育30 min;滴加兔源PCNA一抗(1∶100),4 ℃孵育过夜;滴加辣根过氧化物酶标记的山羊抗兔二抗工作液(1∶100),37 ℃温箱湿盒内孵育1 h;滴加DAB显色剂,显色1 min。阴性对照用磷酸盐缓冲液替代一抗,其余步骤同上。光镜观察免疫组化染色切片,细胞内有棕黄色粗颗粒分布或棕黄色细腻颗粒弥漫分布者为阳性细胞。每组选取5张切片,每张切片选取5个互不重叠且清晰的视野观察计数,计算细胞阳性率:细胞阳性率=阳性细胞数÷视野内细胞总数×100%。
用SPSS 19.0软件,用K-S检验和Levene检验分别检测数据正态性和方差齐性,数据用"
见
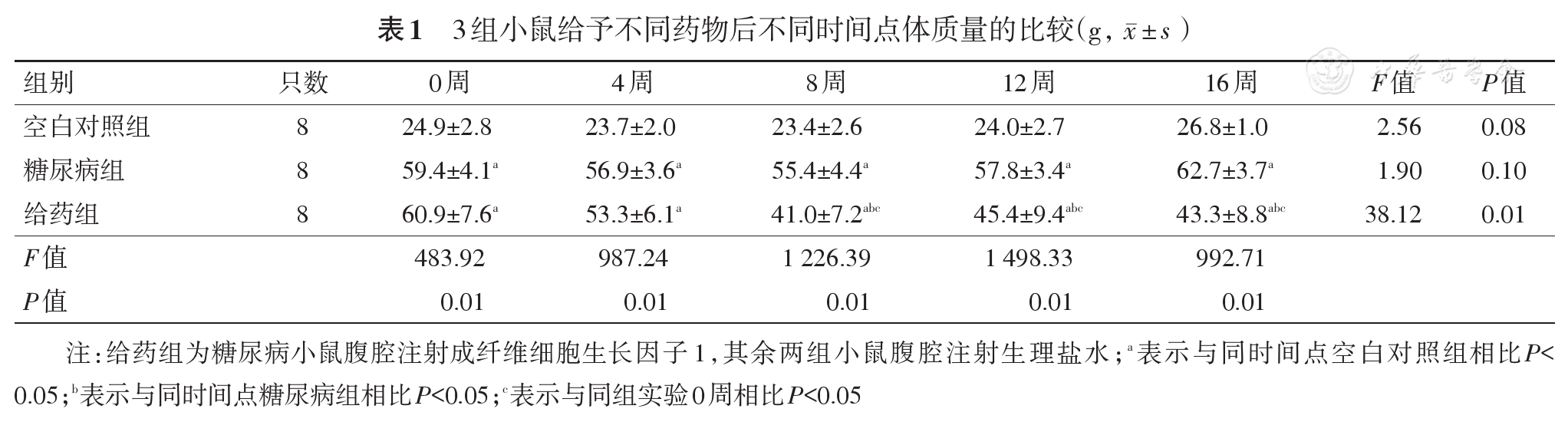
(1)体质量:给药组小鼠体质量从实验4周开始逐渐下降,8周显著低于同时间点糖尿病组(P<0.05),但仍显著高于同时间点空白对照组(P<0.05);实验8至16周给药组小鼠体质量无明显变化(P>0.05)。
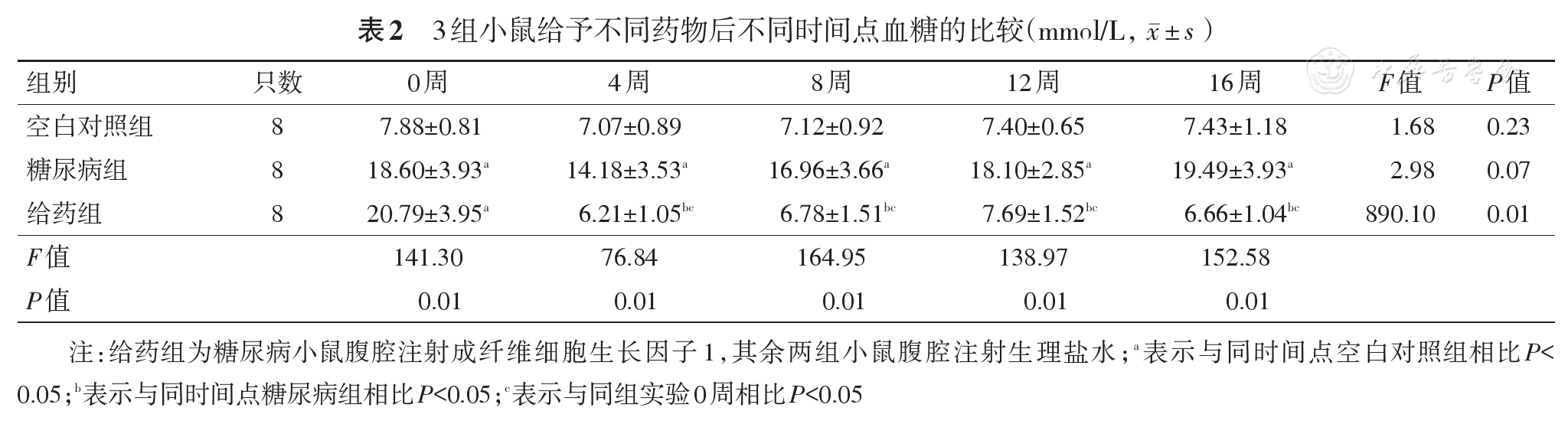
(2)血糖:实验4周给药组小鼠血糖较实验0周显著下降(P<0.05),接近同时间点空白对照组(P>0.05),与同时间点糖尿病组小鼠血糖差异有统计学意义(P<0.05);实验8至16周给药组小鼠血糖无明显变化(P>0.05)。
见
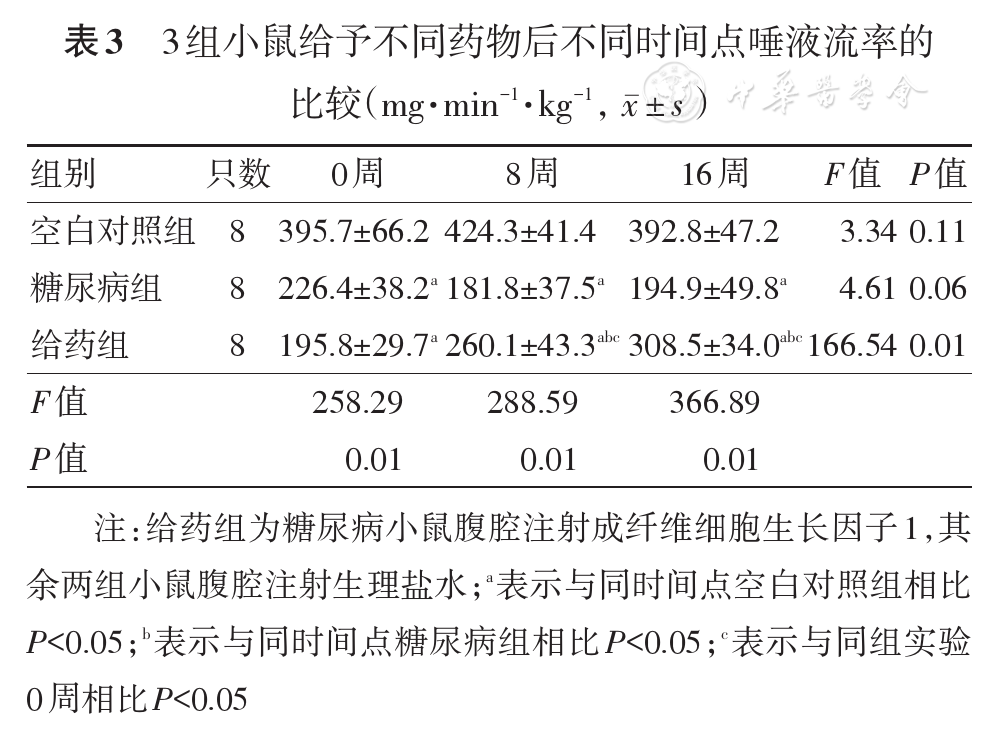
见
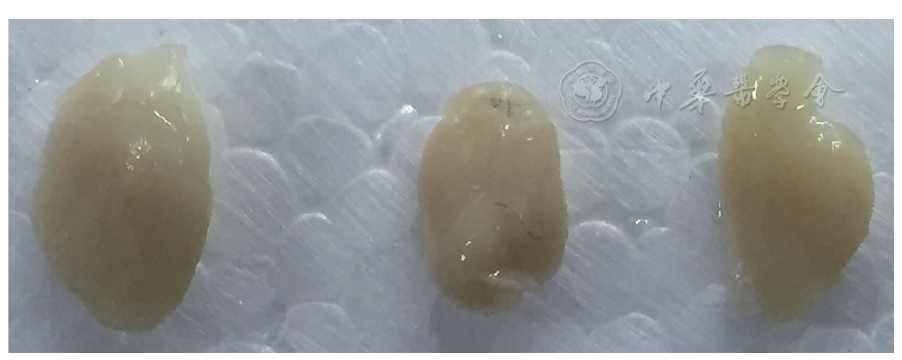
见
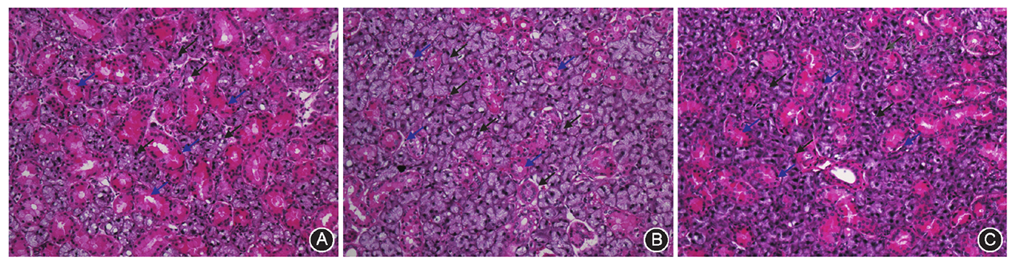
见
糖尿病是一种以全身性代谢紊乱为主的内分泌疾病,不仅能引发全身代谢紊乱,而且随着病情发展,可造成眼、肾脏、心血管、脑和神经等多器官损伤及功能障碍。糖尿病患者有不同程度的口干、多饮症状,以往认为是由于血糖控制不佳,血糖偏高时血液渗透压增加,引起渗透性利尿,使血容量减少,刺激大脑皮层,出现口干感觉。目前研究显示,糖尿病对唾液腺组织本身和功能均有一定损伤[16,17,18]。糖尿病不仅能导致腮腺和下颌下腺体积缩小[2, 16],而且能使腺体唾液流率减少[18,19],同时影响腺体的糖、脂及蛋白质代谢,改变唾液成分及含量[1,17,20,21]。
近年FGF-1在降血糖方面的作用和优势被大量报道[13,14,15],提示FGF-1有可能替代胰岛素在治疗2型糖尿病及其口腔并发症中发挥积极作用。已有研究显示胰岛素能改善糖尿病小鼠下颌下腺颗粒曲管结构[22]。因此本项研究观察FGF-1能否像胰岛素一样对糖尿病导致的下颌下腺结构和功能损伤起保护作用;结果显示,FGF-1给药后,糖尿病小鼠血糖下降明显,而且体质量有一定程度减轻,肥胖症状改善。糖尿病小鼠下颌下腺萎缩明显,组织学亦观察到下颌下腺腺泡明显萎缩,细胞排列紊乱;颗粒曲管导管数目减少,管径变细。与文献结果一致[2,22,23]。而经FGF-1给药后,糖尿病小鼠下颌下腺大体及组织学形态均趋于正常,表明FGF-1能逆转糖尿病导致的下颌下腺结构损伤。唾液流率结果也显示,给药组小鼠唾液流率随着时间延长而逐步增加,提示FGF-1也可逆转糖尿病导致的下颌下腺功能损伤。但本项研究仅为初步研究,故并未评价腺体中糖、脂、蛋白质成分及唾液成分和含量等功能指标,相关功能改变尚待深入研究。
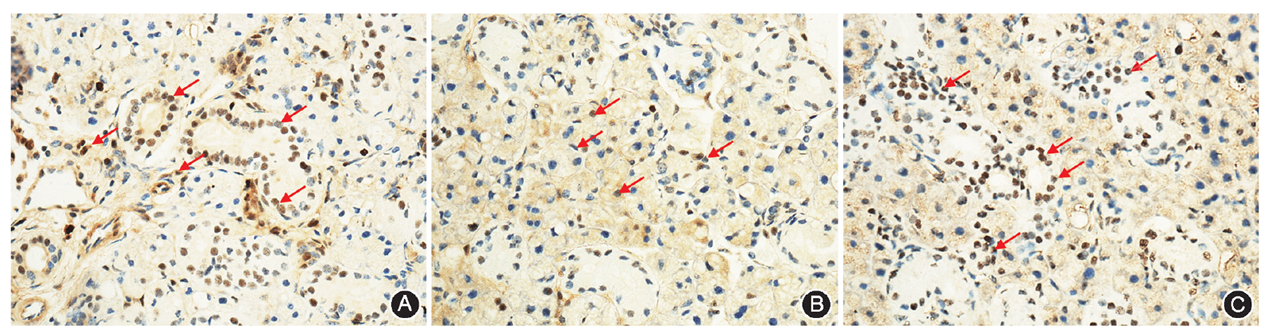
糖尿病使下颌下腺萎缩的病理机制尚不清楚,可能与氧化应激及细胞凋亡相关。氧化应激是糖尿病及其并发症发生发展的关键因素。长期高血糖环境使下颌下腺组织中活性氧产生增加,而抗氧化物质不足,机体对氧自由基的清除能力大大减弱,这种动态失衡引起活性氧有害蓄积,对细胞内蛋白质、核酸和脂质等大分子物质造成氧化损伤,从而导致细胞凋亡[24,25]。而目前研究较多的与细胞凋亡相关的因子包括PCNA、B淋巴细胞瘤2(B-cell lymphoma-2,Bcl-2)和Bcl-2相关X蛋白、自杀相关因子(factor associated suicide,Fas)和Fas配体、肿瘤坏死因子α等[26,27,28,29]。本项实验检测了PCNA在糖尿病小鼠下颌下腺的表达。结果显示糖尿病使小鼠下颌下腺PCNA细胞阳性率显著下降,提示下颌下腺腺体增殖活动减弱,而FGF-1能上调PCNA在下颌下腺的表达,提示FGF-1增强下颌下腺腺体增殖活动。机制可能是FGF-1通过降低血糖,减轻了氧化应激,进而活化磷酸肌醇3激酶(phosphatidylinositol 3 kinase,PI3K)/蛋白激酶B(protein kinase B,PKB,又名AKT)/哺乳动物类雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)及p38促分裂原活化的蛋白激酶(p38 mitogenactivated protein kinase,p38 MAPK)信号通路。通过促进PI3K、AKT、mTOR及胞外信号调节激酶1/2(extracellular signal-regulated kinases,ERK1/2)、p38 MAPK等磷酸化,将细胞外刺激信号转导至细胞及其核内,诱导PCNA表达增多,加速细胞有丝分裂进程,促进细胞增殖[30,31,32]。但目前国内外关于PCNA的研究主要集中于临床病理现象观察,较少涉及作用机制。
本项研究证实了FGF-1能逆转糖尿病导致的小鼠下颌下腺结构萎缩及功能减退,这种作用可能通过上调颌下腺PCNA表达实现。因此,早期应用FGF-1治疗2型糖尿病,不仅能控制糖脂代谢紊乱,而且能缓解糖尿病性口干这一并发症,同时也可能有助于减缓糖尿病其他慢性并发症的发生发展。
[1] Mahay S, Adeghate E, Lindley MZ, et al. Streptozotocin-induced type 1 diabetes mellitus alters the morphology, secretory function and acyl lipid contents in the isolated rat parotid salivary gland[J]. Mol Cell Biochem, 2004, 261(1/2):175-181.
[2] Noorafshan A. Volume-weighted mean volume of the submandibular gland acini in male and female diabetic rats[J]. Micron, 2006, 37(7):613-616.
[3] 吴学平,彭彦霄,伍雪芳,等.凋亡相关蛋白Bcl-2及Bax在糖尿病大鼠下颌下腺内的表达[J].解剖学杂志, 2009, 32(2):155-158.
[4] 刘红艳,高福禄,董福生,等.凋亡细胞在db/db自发性糖尿病小鼠颌下腺的分布[J].解剖学杂志, 2007, 30(3):273-275.
[5]
[6] Dkhil MA, Zrieq R, Al-Quraishy S, et al. Selenium nanoparticles attenuate oxidative stress and testicular damage in streptozotocin-induced diabetic rats[J]. Molecules, 2016, 21(11):1517.
[7] Li DW, Wang YD, Zhou SY, et al. α-lipoic acid exerts neuroprotective effects on neuronal cells by upregulating the expression of PCNA via the P53 pathway in neurodegenerative conditions[J]. Mol Med Rep, 2016, 14(5):4360-4366.
[8] Hao XN, Wang WJ, Chen J, et al. Effects of resveratrol on ARPE-19 cell proliferation and migration via regulating the expression of proliferating cell nuclear antigen, P21, P27 and p38MAPK/MMP-9[J]. Int J Ophthalmol, 2016, 9(12):1725-1731.
[9] 刘红艳,宋晓晨,董福生,等. PCNA在db/db自发性糖尿病小鼠颌下腺的表达[J].实用口腔医学杂志, 2007, 23(1):67-70.
[10] DePaul MA, Lin CY, Silver J, et al. Peripheral nerve transplantation combined with acidic fibroblast growth factor and chondroitinase induces regeneration and improves urinary function in complete spinal cord transected adult mice[J]. PLoS One, 2015, 10(10):e0139335.
[11] Tan Y, Wang KY, Wang N, et al. Ectopic expression of human acidic fibroblast growth factor 1 in the medicinal plant, Salvia miltiorrhiza, accelerates the healing of burn wounds[J]. BMC Biotechnol, 2014, 14:74.
[12] Khanna O, Huang JJ, Moya ML, et al. FGF-1 delivery from multilayer alginate microbeads stimulates a rapid and persistent increase in vascular density[J]. Microvasc Res, 2013, 90:23-29.
[13] Suh JM, Jonker JW, Ahmadian M, et al. Endocrinization of FGF1 produces a neomorphic and potent insulin sensitizer[J]. Nature, 2014, 513(7518):436-439.
[14] Scarlett JM, Rojas JM, Matsen ME, et al. Central injection of fibroblast growth factor 1 induces sustained remission of diabetic hyperglycemia in rodents[J]. Nat Med, 2016, 22(7):800-806.
[15] Jonker JW, Suh JM, Atkins AR, et al. A PPARγ-FGF1 axis is required for adaptive adipose remodelling and metabolic homeostasis[J]. Nature, 2012, 485(7398):391-394.
[16] Lilliu MA, Solinas P, Cossu M, et al. Diabetes causes morphological changes in human submandibular gland: a morphometric study[J]. J Oral Pathol Med, 2015, 44(4):291-295.
[17] Stewart CR, Obi N, Epane EC, et al. Effects of diabetes on salivary gland protein expression of tetrahydrobiopterin and nitric oxide synthesis and function[J]. J Periodontol, 2016, 87(6):735-741.
[18] Izumi M, Zhang BX, Dean DD, et al. Secretion of salivary statherin is compromised in uncontrolled diabetic patients[J]. BBA Clin, 2015, 3:135-140.
[19] Chávez EM, Borrell LN, Taylor GW, et al. A longitudinal analysis of salivary flow in control subjects and older adults with type 2 diabetes[J]. Oral Surg Oral Med Oral Pathol Oral Radiol Endod, 2001, 91(2):166-173.
[20] Nicolau J, de Matos JA, de Souza DN, et al. Altered glycogen metabolism in the submandibular and parotid salivary glands of rats with streptozotocin-induced diabetes[J]. J Oral Sci, 2005, 47(2):111-116.
[21] Nogueira FN, Carvalho RA. Metabolic remodeling triggered by salivation and diabetes in major salivary glands[J]. NMR Biomed, 2017, 30(2):e3683.
[22] Kasayama S, Ohba Y, Oka T. Epidermal growth factor deficiency associated with diabetes mellitus[J]. Proc Natl Acad Sci U S A, 1989, 86(19):7644-7648.
[23] Buyuk B, Parlak SN, Keles ON, et al. Effects of diabetes on post-menopausal rat submandibular glands: a histopathological and stereological examination[J]. Eurasian J Med, 2015, 47(3):199-207.
[24] Rains JL, Jain SK. Oxidative stress, insulin signaling, and diabetes[J]. Free Radic Biol Med, 2011, 50(5):567-575.
[25] Maiese K, Morhan SD, Chong ZZ. Oxidative stress biology and cell injury during type 1 and type 2 diabetes mellitus[J]. Curr Neurovasc Res, 2007, 4(1):63-71.
[26] Takahashi S, Shinzato K, Domon T, et al. Mitotic proliferation of myoepithelial cells during regeneration of atrophied rat submandibular glands after duct ligation[J]. J Oral Pathol Med, 2004, 33(7):430-434.
[27] Takahashi S, Gobe GC, Yoshimura Y, et al. Participation of the Fas and Fas ligand systems in apoptosis during atrophy of the rat submandibular glands[J]. Int J Exp Pathol, 2007, 88(1):9-17.
[28] Takahashi S, Yoshimura Y, Yamamoto T, et al. Cellular expression of Bcl-2 and Bax in atrophic submandibular glands of rats[J]. Int J Exp Pathol, 2008, 89(5):303-308.
[29] Calafat M, Larocca L, Roca V, et al. Vasoactive intestinal peptide inhibits TNF-alpha-induced apoptotic events in acinar cells from nonobese diabetic mice submandibular glands[J]. Arthritis Res Ther, 2009, 11(2):R53.
[30] Liu C, Liang X, Wang J, et al. Protein O-fucosyltransferase 1 promotes trophoblast cell proliferation through activation of MAPK and PI3K/Akt signaling pathways[J]. Biomed Pharmacother, 2017, 88:95-101.
[31] Ma F, Zhou Z, Li N, et al. Lin28a promotes self-renewal and proliferation of dairy goat spermatogonial stem cells (SSCs) through regulation of mTOR and PI3K/AKT[J]. Sci Rep, 2016, 6:38805.
[32] Khan S, Jena GB. Protective role of sodium butyrate, a HDAC inhibitor on beta-cell proliferation, function and glucose homeostasis through modulation of p38/ERK MAPK and apoptotic pathways: study in juvenile diabetic rat[J]. Chem Biol Interact, 2014, 213:1-12.

收藏此内容
推荐给朋友