儿童过敏性疾病诊断及治疗专家共识
2019年3月
中华儿科杂志,第57卷第3期 第164页-第171页
过敏性疾病包括食物过敏、特应性皮炎、过敏性鼻炎和过敏性哮喘等。随着疾病谱的转变,过敏性疾病已成为21世纪常见疾病之一,影响了全球约25%的人群,不仅影响患儿的生活质量,甚至危及生命,并给社会带来沉重的经济负担[1]。近年来中国儿童过敏性疾病的患病率逐渐接近西方国家,如重庆地区2岁以内儿童食物过敏检出率为3.5%~7.7%[2,3];其他过敏性疾病呈上升趋势,如国内1~7岁儿童特应性皮炎患病率由2002年的3.07%升高到2015年的12.94%[4,5];2010年我国14岁以下城市儿童平均累积哮喘患病率已达到3.02%,2年现患率为2.38%,较10年、20年前分别上升了43.4%,147.9%[6]。中国大陆地区人口中过敏性鼻炎的患病率亦高达4%~38%[7]。此外,同一患儿可能共患多种过敏性疾病,给防治工作带来很大困难。我国儿科过敏专科医生相对缺少,患过敏性疾病的儿童多分散于皮肤科、呼吸科、消化科、耳鼻咽喉科及儿童保健科等诊治。因此,存在诊治标准不统一、漏诊、误诊、处理不当或诊断过度并存的情况。此外,各科临床医生对过敏性疾病诊治规范可能存在认知不足和使用不当等问题。为此,中华儿科杂志编辑委员会与中华医学会儿科学分会再一次组织免疫、呼吸、皮肤、消化、耳鼻咽喉、儿童保健等多个学组多学科专家共同讨论、撰写"儿童过敏性疾病诊断及治疗专家共识",以期为儿科全科医生长期综合管理过敏性疾病患儿提供帮助。
机体受到生理剂量的过敏原刺激后,出现异于常人的生理功能紊乱或组织细胞损伤的反应称为超敏反应,可由免疫和非免疫机制介导,免疫机制介导的超敏反应称为过敏。
系一组由于机体免疫系统对环境中典型无害物质产生的超敏反应性疾病。包括过敏性鼻炎、特应性皮炎、过敏性哮喘、食物过敏和严重过敏反应等。
指诱导机体产生过敏的抗原物质,多为蛋白或多肽,部分小分子物质作为半抗原与某些蛋白结合后成为过敏原。
指个体或者个体家族成员在接触过敏原时,倾向于产生IgE类抗体的免疫应答并出现过敏性疾病倾向的特质。
婴儿或者儿童早期出现的某种特应性疾病常预示未来其他特应性疾病的发生称为特应性疾病的自然进程,即特应性进程。
系在接触过敏原后数分钟到数小时内迅速发生的危及生命的严重症候群,累及两个或以上器官和(或)系统,严重时可发生过敏性休克,须给予紧急救治[8]。
通过口服抗原机体对该抗原不产生或产生低免疫反应的特异性无应答状态。
各种常见过敏性疾病的主要免疫学机制见

1.IgE介导过敏主要指临床最常见的Ⅰ型超敏反应。发生过程主要包含(1)致敏期:过敏原进入机体诱导B细胞分泌IgE抗体并结合在肥大细胞、嗜碱粒细胞表面。结合IgE的肥大细胞、嗜碱粒细胞处于致敏状态。(2)发敏期:①速发相反应往往发生于数分钟到2 h内。当相同的抗原再次进入致敏的机体,与2个及以上IgE抗体结合,使FcεRⅠ交联,导致肥大细胞与嗜碱粒细胞释放预存的组胺、缓激肽酶、嗜酸粒细胞(eosinophile granulocyte,EOS)趋化因子等;上述各种介质引起小血管及毛细血管扩张,毛细血管通透性增加,平滑肌收缩,腺体分泌增加,EOS增多、浸润,引起荨麻疹、血管性水肿、支气管哮喘、过敏性休克等临床表现。②迟发相反应常发生于接触过敏原后2~48 h甚至更长,与新合成前列腺素D2、白三烯、肝素、血小板活化因子及细胞因子相关。迟发相反应早期引起黏膜渗出,长期反复发作造成组织损伤和增生性炎症。
2.非IgE介导过敏的发病机制尚不清楚,属免疫延迟反应,参与细胞众多,如T淋巴细胞、调节性T细胞、树突细胞等。
3.部分患儿同时存在IgE及非IgE混合介导的过敏机制。
过敏性疾病为多基因遗传并与环境交互。部分单基因与特应质直接相关,如DOCK8基因缺陷患儿多发生哮喘、特应性皮炎、食物过敏。
卫生假说认为多子家族或农场居住的儿童不易患过敏性疾病。生后与病原及内毒素充分接触,诱导免疫系统产生Th1-干扰素-γ优势应答,抑制Th2类细胞因子,防止过敏性疾病发生。
儿童早期肠道丰富的黏膜相关淋巴组织与大量肠道微生物相互作用对于产生免疫耐受至关重要。不同的菌群模式可诱发不同的免疫反应模式,肠道益生菌群可促进Th1倾向免疫应答,也可促进Treg发育及分泌抑制性细胞因子。益生菌防治过敏性疾病是目前的研究热点领域,以期达到免疫适宜状态。
当主要家族成员患有过敏性疾病时,该儿童应作为过敏性疾病高危儿进行管理。然而,过敏性疾病的临床症状缺乏特异性(

当疑诊过敏性疾病时,病史询问的重点在于推测可疑过敏原。如婴幼儿常发生食物过敏和特应性皮炎,而食物过敏症状常表现于皮肤和消化道,很少单独出现呼吸道症状,通过询问饮食史或饮食日记以帮助寻找致敏食物;吸入过敏原所致季节性过敏多发生于年长儿,如花粉过敏患儿发病一般是在特殊花粉出现的季节,并因地理环境不同发病时间也有变化;霉菌所引起的过敏可能在潮湿的季节多发或加重;全年发作的患儿往往与螨、蟑螂、动物皮毛、食物有关。
严重过敏反应可在暴露于可疑过敏原后数分钟或数小时内症状快速进展,至少累及呼吸或心血管系统,治疗不及时可导致死亡。临床医生应关注严重过敏反应危险信号[9],如消化道(痉挛性腹痛、呕吐、腹泻等)、皮肤及黏膜(突发全身性荨麻疹、瘙痒、脸红、唇-舌-悬雍垂肿胀等)、呼吸系统(喘鸣、哮喘、呼吸费力、持续剧烈咳嗽、发绀等)、心血管系统(低血压、心律紊乱、晕厥等)症状。一旦发生严重过敏反应,应即刻抢救。
用于过敏性疾病诊断的方法较多,每种方法适应对象及疾病存在差异(
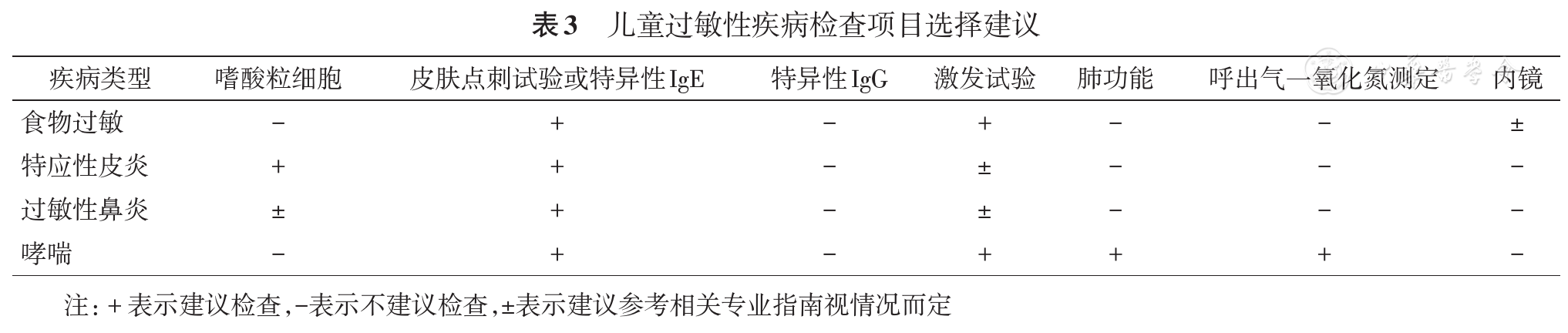
外周血、局部体液(鼻分泌物、皮疱液、支气管肺泡液等)或胃肠黏膜中的EOS增高可辅助诊断过敏性疾病。过敏患儿外周血EOS常>0.5×109/L;当诱导痰液中EOS计数>0.03提示存在EOS性气道炎症[10,11]。EOS升高水平与特应性皮炎症状严重程度正相关,故可作为监测临床疗效的指标之一[12]。EOS增高亦可见生理(如早产儿、家族性或静脉营养后)或病理(如寄生虫感染、EOS肺炎、炎性肠病、T细胞免疫缺陷等)情况,需注意鉴别。
血清总IgE水平对于诊断过敏性疾病价值有限,故应采用血清sIgE测定筛查Ⅰ型超敏反应,灵敏度和特异性较高。血清sIgE的量可根据不同检测方法绘制的标准曲线获得,故因实验室采用的检测方法不同而使得各自测得的sIgE水平不具可比性[13]。通常,血清sIgE水平越高,患儿对相应过敏原发生过敏反应的可能性越大,但并不能反映症状的严重程度[13]。与皮肤点刺试验相同,血清sIgE检测阳性,仅代表致敏状态而不一定出现过敏的临床表现。
不能单纯基于抗原特异性IgG和IgG4抗体滴度检测诊断过敏性疾病,也不能作为进行食物规避或药物治疗的依据[14,15,16]。
所有体内检查均有诱发严重过敏反应风险,故应在有抢救条件的医院内有专业人员监测时进行。
是筛查食入及吸入过敏原诱发IgE介导的速发型变态反应最常用的方法。测试时应同时设立阳性(组胺:10 g/L)及阴性对照(生理盐水)。无论对于吸入或食入过敏原,皮肤点刺试验均具有较低的阳性预测正确率和较高的阴性预测正确率,故皮肤点刺试验阴性可基本排除该过敏原诱发的IgE介导的过敏反应,而阳性者则需进一步确诊。
口服激发试验阳性是确诊食物过敏的依据[17,18,19]。乙酰胆碱支气管激发试验在临床上主要用于判断可疑哮喘患儿是否存在支气管高反应性及其程度。
肺通气功能测定是确定儿童哮喘诊断、评估疾病严重度并指导控制药物治疗强度的主要手段,哮喘患儿存在可逆性通气功能受限,表现为阻塞性通气功能障碍。尽可能对所有怀疑哮喘的适龄儿童进行此项检查,并定期复查。
为无创气道炎症检测手段,有利于气道炎症状况评估,对长期控制治疗药物剂量的调整有一定帮助,建议进行系列动态监测,单次检测的实际临床意义有限。
若病史高度怀疑消化道症状与食物摄入有关,但经饮食回避4周,症状仍不缓解,需要进一步诊断和鉴别诊断时,可由消化科医生决定是否进行消化内镜检查[19]。
诊断标准详见各专科疾病诊疗指南[17,18,19,20,21,22,23],当高度怀疑为过敏性疾病时,需转诊至相应专科进行确诊及长期管理。
过敏性疾病属于慢性非传染性疾病,管理的主要策略包括对因治疗(回避过敏原或对部分患儿采用特异性免疫疗法)和药物对症治疗。患儿和(或)家长的依从性是决定疗效的重要因素。曾发生严重过敏反应者随身携带肾上腺素笔和医疗救助卡片是挽救生命的重要手段。
采用恰当方法避免接触已明确的吸入过敏原是治疗气道过敏性疾病的有效措施(

特异性免疫疗法应在有严格医疗监测的医院进行。对于诊断明确的过敏性鼻炎患儿或哮喘控制不理想且与疾病相关的过敏原已得到确定的儿童,可在基础药物治疗同时使用变应原特异性免疫治疗,但是目前国内仅有螨虫变应原免疫制剂可供临床使用[24]。因食物过敏有自愈倾向,目前口服免疫疗法治疗IgE介导的食物过敏尚未在临床常规开展,国外建议用于5岁以上过敏症状持续的患儿[25]。
需要专科医生根据专业指南进行药物选择并随访[17,18,19,20,21,22,23](
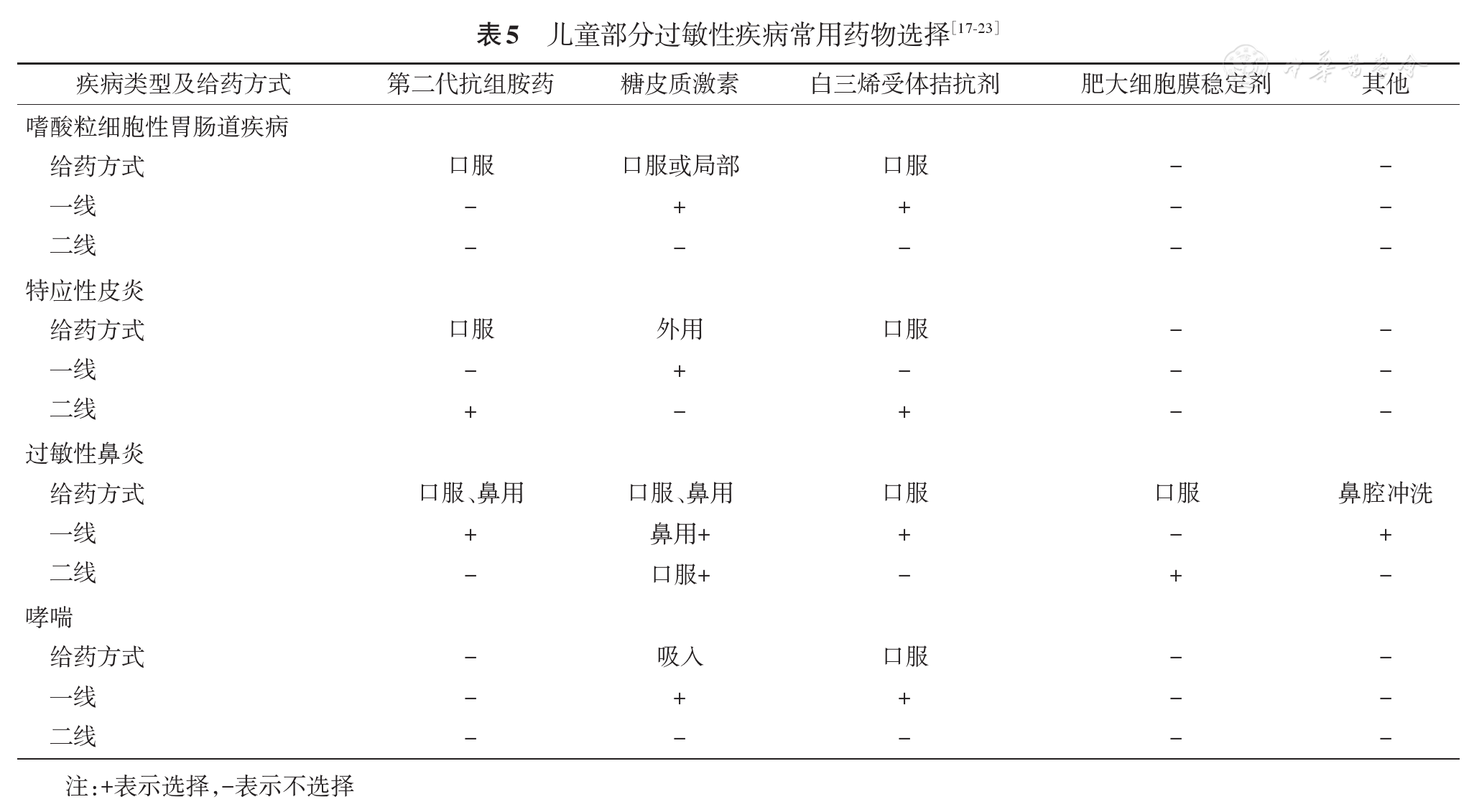
对于严重过敏反应,肾上腺素为一线治疗药物。大腿外侧肌肉注射1∶1 000的肾上腺素,6月龄~6岁(<30 kg),0.15 mg/次;6~12岁(≥30 kg),0.3 mg/次;>12岁0.5 mg/次。若无缓解,5~10 min可重复使用1次。治疗时多选择仰卧位(呕吐者建议左侧卧位,呼吸困难者可以45°坐位),抬高下肢以改善低血压[8,9]。严重过敏反应治疗关键是维持呼吸道通畅和保持有效血液循环,其他治疗药物包括糖皮质激素、抗组胺药物等。
口服抗组胺药可有效控制特应性皮炎的瘙痒,明显缓解过敏性鼻炎所致的鼻痒、流涕打喷嚏症状,对过敏性结膜炎所致眼部症状也有一定缓解作用,但改善鼻塞的效果有限。鼻用抗组胺药对控制过敏性鼻炎的鼻部症状疗效相当于或优于第二代口服抗组胺药,特别是在对鼻塞症状的缓解上更为有效。消化道过敏症状一般不建议使用抗组胺药。儿童应用抗组胺药需注意年龄限制,按照药品说明书应用。
为儿童哮喘和过敏性鼻炎治疗的一线用药;对过敏性鼻炎所致鼻塞症状改善作用优于第二代口服抗组胺药。
对于严重过敏者,如严重喘息发作、喉头水肿、血管性水肿及全身过敏反应可短期全身使用糖皮质激素。口服糖皮质激素对嗜酸粒细胞性胃肠炎治疗有效;嗜酸粒细胞性食管炎亦可采用局部糖皮质激素治疗,无效时可全身应用;而其他消化道过敏症不使用激素治疗。外用糖皮质激素是目前特应性皮炎治疗的一线用药,根据皮损严重程度、皮损部位等因素合理选择不同浓度的糖皮质激素治疗。吸入糖皮质激素是哮喘长期控制治疗的优选药物,喘息急性发作时高剂量吸入糖皮质激素有助于症状的缓解,并可减少全身糖皮质激素的使用强度。此外,鼻用糖皮质激素对过敏性鼻炎的所有症状均有显著改善作用,但起效时间较缓慢;对于哮喘伴过敏性鼻炎患儿可同时局部吸入和鼻用糖皮质激素,根据各自症状缓解的情况分别降阶梯减少药物使用强度,目的是通过同时控制上下气道炎症而减少激素的总体用量。
为治疗过敏性鼻炎的二线治疗药物,对缓解喷嚏、鼻痒、流涕等症状有一定效果,但对鼻塞的改善不明显。也可在致敏花粉播散前2周开始作为预防用药,以缓解发作时症状。
用于6岁以上经吸入激素合并长效β2-肾上腺素受体激动剂治疗控制不佳的中重度过敏性哮喘患儿。
钙调神经磷酸酶抑制剂是目前治疗特应性皮炎的二线外用药物,某些特殊部位,如面部、颈部、外生殖器等,可视皮损情况合理选用。同时需注意使用润肤剂修复和维持皮肤屏障是特应性皮炎治疗长期治疗管理的基础。鼻腔盐水冲洗作为辅助治疗方法,可明显改善过敏性鼻炎患儿喷嚏和鼻塞症状。
应采取有效措施控制室外和室内环境中的过敏原(
预防过敏性疾病的营养策略主要针对过敏性疾病高风险人群[17,18,19,26,27,28,29,30,31]。
纯母乳喂养至少4~6月龄;有条件的配方奶喂养者建议选择部分水解配方。
4~6月龄后常规引入固体食物,不晚于1岁;每次只引入一种新食物且持续3~5 d或5 d以上;食物多样化,保持日常摄入以维持其耐受性。
添加益生菌仅用于预防湿疹;不能母乳喂养者建议添加含有益生元的配方粉;不建议采用其他免疫调节性营养食物(如ω-3,维生素D)预防过敏性疾病。
健康教育在过敏性疾病的防治体系中具有十分重要的意义,治疗依从性常常决定了治疗的效果。世界过敏组织提出,对过敏性疾病患儿的健康教育可以分为3个方面:首诊教育、强化教育(随诊教育)以及家庭和看护人员教育[32]。其主要内容包括:过敏知识的普及和指导,让患儿及家长了解过敏性疾病的病因、危险因素、自然进程以及疾病可能造成的危害性;告知患儿及其家长均衡营养及随访的重要性;指导患儿进行良好的环境控制,避免接触或尽可能少接触过敏原;告知减少经皮肤致敏的方法,培养正确的洗护及穿衣习惯;告知患儿过敏原检查的必要性和主要检测方法;介绍药物治疗和特异性免疫治疗的作用、效果、疗程和可能发生的不良反应,指导患儿用药方法以及剂量和种类的调整。
充分做好与患儿或监护人的沟通,使其正确理解该病的发作因素、慢性和复发性特点,以及对学习能力、生活质量等的影响,使患儿及家长了解过敏性疾病长期用药的必要性,克服激素恐惧,从而增强治疗依从性。
罹患过敏性疾病、特应性体质及有过敏家族史的儿童,只要既往不对疫苗或其成分过敏、所患过敏性疾病与疫苗成分无关,均可按计划常规行疫苗接种[33]。接种时机一般选择过敏缓解期或恢复期,且应在有抢救设施的单位进行。
罹患与疫苗成分有关的过敏性疾病患儿的疫苗接种需谨慎(

黄热病疫苗按①,麻风腮疫苗、流感疫苗按②
疫苗接种4 h内出现≥1个系统的症状或体征(包括皮肤、呼吸道、心血管或胃肠道表现)应考虑为疫苗过敏反应[33,34,35,36]。对于曾发生疫苗过敏,但未确定过敏原者,若发生严重过敏反应,则不再接种该疫苗,并对该疫苗及其成分、周围环境进行充分分析,今后再接种其他疫苗时,也应注意有无不良反应;若发生非致命性疫苗过敏,且有再接种该疫苗的必要性,也对该疫苗及其成分、周围环境进行充分分析,今后每次接种其他疫苗须在配备有抢救物品及设置的医疗机构进行,并在接种后留观。
(胡燕、洪建国、赵晓东、宋红梅、龚四堂、马琳、谷庆隆 执笔)
[1] Haahtela T, von HL, M?kel? M, et al. Finnish allergy programme 2008-2018--time to act and change the course[J]. Allergy, 2008, 63(6):634-645.
[2] Hu Y, Chen J, Li H. Comparison of food allergy prevalence among Chinese infants in Chongqing, 2009 versus 1999[J]. Pediatr Int, 2010,52(5):820-824.
[3] 陈静,廖艳,张红忠,等.三城市两岁以下儿童食物过敏现状调查[J].中华儿科杂志,2012,50(1):5-9.
[4] 顾恒,尤立平,刘永生,等.我国10城市学龄前儿童特应性皮炎现况调查[J].中华皮肤科杂志,2004,37(1):29-31.
[5] Guo Y, Li P, Tang J, et al. Prevalence of atopic dermatitis in Chinese children aged 1-7 ys[J].Sci Rep,2016,6:29751.
[6] 刘传合,洪建国,尚云晓,等.中国16城市儿童哮喘患病率20年对比研究[J].中国实用儿科杂志,2015,30(8):596-600.
[7] Zhang Y, Zhang L. Prevalence of allergic rhinitis in China[J]. Allergy Asthma Immunol Res, 2014, 6(2):105-113.
[8] Jimenez-Rodriguez TW, Garcia-Neuer M, Alenazy LA, et al. Anaphylaxis in the 21st century: phenotypes, endotypes, and biomarkers[J]. J Asthma Allergy, 2018,11:121-142.
[9] Lieberman P, Nicklas RA, Oppenheimer J, et al. The diagnosis and management of anaphylaxis practice parameter: 2010 update[J]. J Allergy Clin Immunol, 2010,126(3):
[10] Hargreave FE, Leigh R. Induced sputum, eosinophilic bronchitis, and chronic obstructive pulmonary disease[J]. Am J Respir Crit Care Med, 1999, 160(5
[11] 许以平.过敏性疾病实验室检测方法的完善刻不容缓[J].中华检验医学杂志,2006,29(8):673-675.
[12] Saeki H, Nakahara T, Tanaka A, et al. Clinical practice guidelines for the management of atopic dermatitis 2016[J]. J Dermatol, 2016, 43(10):1117-1145.
[13] Cox L, Williams B, Sicherer S, et al. Pearls and pitfalls of allergy diagnostic testing: report from the American College of Allergy, Asthma and Immunology/American Academy of Allergy, Asthma and Immunology Specific IgE Test Task Force [J]. Ann Allergy Asthma Immunol, 2008,101(6):580-592.
[14] Stapel SO, Asero R, Ballmer-Weber BK, et al. Testing for IgG4 against foods is not recommended as a diagnostic tool: EAACI Task Force Report[J]. Allergy, 2008, 63(7):793-796.
[15] Burks AW, Tang M, Sicherer S, et al. ICON: food allergy[J]. J Allergy Clin Immunol, 2012,129(4):906-920.
[16] Sampson HA, Aceves S, Bock SA, et al. Food allergy: a practice parameter update-2014[J]. J Allergy Clin Immunol, 2014,134(5):
[17] 中华医学会儿科学分会儿童保健学组,《中华儿科杂志》编辑委员会.婴幼儿食物过敏诊治建议[J].中华儿科杂志, 2011, 49(5):344-348.
[18] 中华医学会儿科学分会免疫学组,中华医学会儿科学分会儿童保健学组,中华医学会儿科学分会消化学组,等.中国婴幼儿牛奶蛋白过敏诊治循证建议[J].中华儿科杂志, 2013, 51(3):183-186.
[19] 中华医学会儿科学分会消化学组.食物过敏相关消化道疾病诊断与管理专家共识[J].中华儿科杂志,2017,55(7):487-492.
[20] 中华医学会皮肤性病学分会免疫学组,特应性皮炎协作研究中心.中国特应性皮炎诊疗指南(2014版)[J].中华皮肤科杂志,2014,47(7):511-514.
[21] 中华耳鼻咽喉头颈外科杂志编辑委员会鼻科组,中华医学会耳鼻咽喉头颈外科学分会鼻科学组.变应性鼻炎诊断和治疗指南(2015年,天津)[J].中华耳鼻咽喉头颈外科杂志,2016,51(1):6-24.
[22] 《中华耳鼻咽喉头颈外科杂志》编辑委员会鼻科组,中华医学会耳鼻咽喉头颈外科学分会鼻科学组、小儿学组,《中华儿科杂志》编辑委员会.儿童变应性鼻炎诊断和治疗的专家共识(2010年,重庆)[J].中华儿科杂志,2011, 49(2):116-117.
[23] 中华医学会儿科学分会呼吸学组,《中华儿科杂志》编辑委员会.儿童支气管哮喘诊断与防治指南(2016年版)[J].中华儿科杂志, 2016, 54(3):167-181.
[24] 中华耳鼻咽喉头颈外科杂志编委会鼻科组,中华医学会耳鼻咽喉头颈外科学分会鼻科学组.变应性鼻炎特异性免疫治疗专家共识[J].中华耳鼻咽喉头颈外科杂志,2011,46(12):976-980.
[25] Arasi S, Caminiti L, Crisafulli G, et al. A general strategy for de novo immunotherapy design: the active treatment of food allergy[J]. Expert Rev Clin Immunol, 2018, 14(8):665-671.
[26] Togias A, Cooper SF, Acebal ML, et al. Addendum guidelines for the prevention of peanut allergy in the United States: report of the national institute of allergy and infectious diseases-sponsored expert panel[J]. J Allergy Clin Immunol, 2017,139(1):29-44.
[27] Fewtrell M, Bronsky J, Campoy C, et al. Complementary feeding: a position paper by the European Society for Paediatric Gastroenterology, Hepatology, and Nutrition (ESPGHAN) committee on nutrition[J]. J Pediatr Gastroenterol Nutr, 2017, 64(1):119-132.
[28] Ricci G, Cipriani F, Cuello-Garcia CA, et al. A clinical reading on "World Allergy Organization-McMaster University Guidelines for Allergic Disease Prevention (GLAD-P): Probiotics"[J]. World Allergy Organ J, 2016, 9:9.
[29] Cuello-Garcia CA, Fiocchi A, Pawankar R, et al. World Allergy Organization-McMaster University Guidelines for Allergic Disease Prevention (GLAD-P): Prebiotics[J]. World Allergy Organ J, 2016,9:10.
[30] Yepes-Nu?ez JJ, Fiocchi A, Pawankar R, et al. World Allergy Organization-McMaster University Guidelines for Allergic Disease Prevention (GLAD-P): Vitamin D[J]. World Allergy Organ J, 2016,9:17.
[31] Turner PJ, Campbell DE, Boyle RJ, et al. Primary prevention of food allergy: translating evidence from clinical trials to population-based recommendations[J]. J Allergy Clin Immunol Pract, 2018,6(2):367-375.
[32]
[33] Nilsson L, Brockow K, Alm J, et al. Vaccination and allergy: EAACI position paper, practical aspects[J]. Pediatr Allergy Immunol, 2017,28(7):628-640.
[34] Dreskin SC, Halsey NA, Kelso JM, et al. International Consensus (ICON): allergic reactions to vaccines[J]. World Allergy Organ J, 2016,9(1):32.
[35] Echeverría ZL, Ortigosa DCL, Alonso LE, et al.Consensus position document on the child with an allergic reaction after vaccination or an allergy to vaccine components[J]. An Pediatr (Barc), 2015,83(1):
[36] Echeverría-Zudaire LA, Ortigosa-del CL, Alonso-Lebrero E, et al. Consensus document on the approach to children with allergic reactions after vaccination or allergy to vaccine components[J]. Allergol Immunopathol (Madr), 2015, 43(3):304-325.
[37] Micheletti F, Peroni D, Piacentini G, et al. Vaccine allergy evaluation and management at the specialized Green Channel Consultation Clinic[J]. Clin Exp Allergy, 2012, 42(7):1088-1096.
[38] Caubet JC, Rudzeviciene O, Gomes E, et al. Managing a child with possible allergy to vaccine[J]. Pediatr Allergy Immunol, 2014,25(4):394-403.
[39] James JM, Burks AW, Roberson PK, et al. Safe administration of the measles vaccine to children allergic to eggs[J]. N Engl J Med, 1995,332(19):1262-1266.
[40] Baxter DN. Measles immunization in children with a history of egg allergy[J]. Vaccine, 1996,14(2):131-134.
[41] Franceschini F, Bottau P, Caimmi S, et al. Vaccination in children with allergy to non active vaccine components[J]. Clin Transl Med, 2015,4:3.

收藏此内容
推荐给朋友