脾硬化性血管瘤样结节性转化合并症状性门静脉高压二例
2019年1月
中华放射学杂志,第53卷第1期 第73页-第75页
罗永竞,叶鹏,缪洪飞,阮德斌,曾庆乐,陈勇
例1 男,26岁。8个月前因反复呕血,伴头晕、左腹胀痛就诊于当地医院。查体:左上腹轻压痛,贫血面容。实验室检查:白细胞(WBC)1.6×109/L[正常值(4.0~10.0)×109/L]、血小板(PLT)121×109/L[正常值(100~300)×109/L]、血红蛋白(HGB)61 g/L[正常值(120~160 g/L]。胃镜检查示:食管胃底静脉重度曲张。术前增强CT扫描示:脾内多发类圆形占位,最大者直径约3 cm,中央可见不均匀低密度影;门静脉主干及脾静脉明显增粗,呈瘤样扩张,其中门静脉主干直径5.2 cm,脾静脉直径4.1 cm;门静脉主干与肠系膜上静脉交界处环状狭窄(
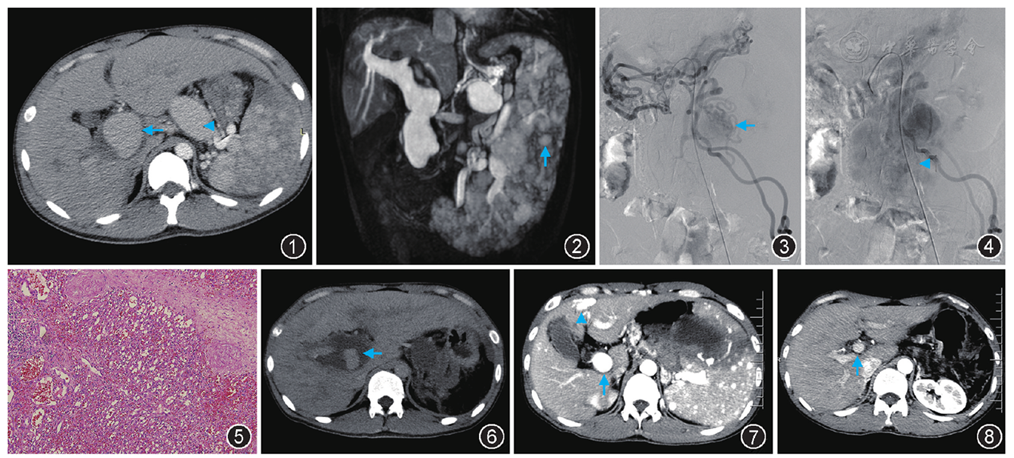
患者于2017年7月20日行"剖腹探查+脾切除术",术中见肝脏无明显肝硬化征象,初次测量胃冠状静脉压力为40.5 mmHg(1 mmHg=0.133 kPa),切除脾脏后再次测量胃冠状静脉压力为18.4 mmHg。手术切除脾脏约26.0 cm×15.0 cm×8.0 cm,脾表面呈多结节状,切面灰红色,质软。术后病理,光学显微镜下见纤维硬化间质中分布大量血管瘤样结节,结节由裂隙状、圆形和不规则血管组成(
术后3个月,复查CT示门静脉主干及左右分支周边低密度影,未见明显食管胃底曲张静脉显影,门静脉主干直径约4.8 cm,内见广泛低密度影分布于血管壁,考虑为部分血栓形成,有效血流腔直径约2.9 cm,较前明显缩小(
例2 男,29岁。因反复上消化道出血6个月2017年7月30日入院。查体:左上腹压痛,脾脏肋下可触及。实验室检查:WBC 2.56×109/L、NEU 1.80×109/L、HGB 72 g/L。CT检查肝脏未见明显硬化征象,门静脉及脾静脉扩张及食管胃底静脉增粗,门静脉主干直径约3.1 cm,脾静脉直径约2.8 cm;脾脏肿大,增强后可见大小不等的结节状染色,呈弥漫性分布(
患者于2017年8月10日行"剖腹探查+脾切除术",术中未见明显肝硬化征象,术中初次测量胃冠状静脉压力为29.2 mmHg,切除脾脏后再次测量为19.4 mmHg。手术切除脾脏大小为21.0 cm×16.0 cm×7.0 cm,脾表面可见多发结节。免疫组织化学检测示:CD31(+)、CD34(+)、CD8(-)、CD68(+)。病理诊断:SANT。术后6个月,复查CT示胃底及食管下段见少量增粗迂曲血管影,较前明显减少,门静脉主干直径1.7 cm,较前明显缩小(
SANT是一种罕见的良性增生性病变,其临床症状不明显,多为体检偶然发现,2004年由Martel等[1]首次提出并命名。SANT具有独特的病理形态学特征,显微镜下可见明显的多结节病变特性,结节为血管瘤样或肉芽肿样表现,其临床症状不明显,常被误诊为炎性假瘤、错构瘤、血管瘤等[2]。在有症状的患者当中,常以腹痛或腹部不适为主要症状,其他包括发热、脾脏肿大、贫血、全血细胞减少等,均无特征性。影像表现尚有一定的特征,增强扫描CT及MRI均从动脉期到延迟期呈现逐渐向心性充填的辐轮状强化[3]。病理检查可明确诊断,表现为:(1)显微镜下可见多结节血管瘤样结构。(2)免疫组化检测显示:CD31(+)、CD34(+)、CD8(+/-)[4]。此2例SANT患者术后病理检查符合上述表现,而临床上表现为门静脉高压并上消化道出血,查阅国内外文献尚未见报道。
在本组2例SANT患者出现的门静脉高压症状中,其临床特点有:(1)均为反复上消化道出血伴脾脏增大,均有食管胃底静脉曲张。而实验室检查提示患者肝功能正常或基本正常,表现为非硬化性门静脉高压症。(2)影像检查提示脾脏巨大,伴脾脏内弥漫性、大小不等的占位性病灶,呈血管瘤样结节改变;周围脏器的部分供血动脉分支如肠系膜上动脉、胃十二指肠动脉和胃左动脉等也参与脾脏供血;脾静脉及门静脉主干明显增宽,与肠系膜上静脉不成比例。本组2例CT图像上测量脾静脉的直径分别为4.1 cm及2.8 cm,门静脉主干的直径分别为5.2 cm及3.1 cm,而肠系膜上静脉的直径分别为0.7 cm及0.8 cm。
笔者认为,本组2例患者的症状性门静脉高压与SANT有密切关系,其原因有:(1)影像检查可见脾脏内弥漫富血供结节灶。病理切片显示血管瘤样结节内有明显充血表现。免疫组化检测显示血管瘤样结节中主要包含3种类型的血管:毛细血管(免疫标记CD34+、CD8-、CD31+);小静脉(免疫标记CD34-、CD8-、CD31+);红髓样窦状隙(免疫标记CD34-、CD8+、CD31+)[5]。(2)本组2例脾脏内均弥漫及大量分布血管瘤样结节,并且脾脏进行性增大,形成巨脾,从而使脾脏内循环血流量增加,造成脾静脉及门静脉主干明显增宽,与肠系膜上静脉不成比例,从而导致门静脉压力升高。综合国内外文献报道的约140例SANT患者中,孤立性结节患者为132例,多灶性结节患者仅为6例[6],尚未见结节弥漫分布整个脾脏的报道。脾脏的血流量虽有增加,但可能难以发展为门静脉高压症。(3)本组2例患者行脾脏切除术后门静脉高压症状缓解,随访期间无再发上消化道出血等症状。(4)临床检查未能发现其他可能导致门脉高压的原因。
综上所述,SANT是一种脾脏慢性增生性疾病,当病情发展致脾脏循环血流量增加时,可导致脾静脉增宽,门静脉压力升高,甚至上消化道出血,是症状性门脉高压的病因之一。
[1] Martel M, Cheuk W, Lombardi L, et al. Sclerosing angiomatoid nodular transformation (SANT): report of 25 cases of a distinctive benign splenic lesion[J]. Am J Surg Pathol,2004,28(10):1268-1279.
[2] 成克伦,马明宗.脾硬化性血管瘤样结节性转化临床病理分析[J].当代医学,2016(21):59-60.
[3] 张育森,鲍世韵.脾脏硬化性血管瘤样结节性转化诊治分析[J].中华普通外科杂志,2014,29(8):637-638.
[4] Falk GA, Nooli NP, Morris-Stiff G, et al. Sclerosing angiomatoid nodular transformation (SANT) of the spleen: case report and review of the literature[J]. Int J Surg Case Rep,2012,3(10):492-500.
[5] Diebold J, Le Tourneau A, Marmey B, et al. Is sclerosing angiomatoid nodular transformation (SANT) of the splenic red pulp identical to inflammatory pseudotumour? Report of 16 cases[J]. Histopathology,2008,53(3):299-310.
[6] Cao Z, Wang Q, Li J, et al. Multifocal sclerosing angiomatoid nodular transformation of the spleen: a case report and review of literature[J]. Diagn Pathol,2015,10:95.
