贲门小弯侧深在性囊性胃炎CT影像诊断一例
2019年1月
中华放射学杂志,第53卷第1期 第77页-第78页
唐军,董江宁,韦超,李信响,韦树华,吴瑶媛,曹锋
女,45岁。主因体检时行B超检查发现肝左叶下方囊性包块1个月入院。患者半年前无明显诱因出现上腹部隐痛,可自行缓解,未予重视,而后上腹痛间断发作,但均可自行缓解。实验室检查:白细胞2.80×109/L(参考值3.50×109~9.50×109/L),红细胞3.63×1012/L(参考值3.80×1012~5.10×1012/L),乳酸脱氢酶81 U/L(参考值120~250 U/L)。外院胃镜提示浅表性胃炎。
CT表现:平扫贲门小弯侧黏膜下囊性低密度灶,2.4 cm×2.3 cm,边界清楚,密度尚均匀,外膜面光整(
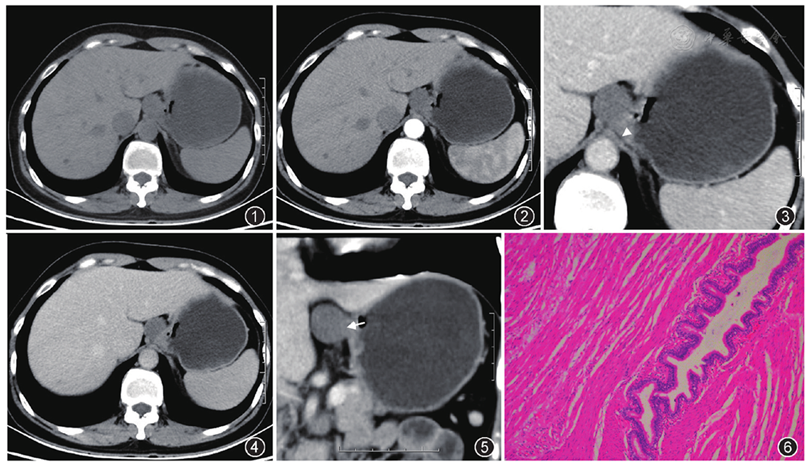
手术及病理:临床术前拟诊腹腔肿瘤,与贲门关系密切,遂行腹腔镜下胃贲门区病灶切除术。术中探查腹腔,肝脏、肠系血管根部未见异常,肿瘤位于胃小弯侧近贲门处,3.0 cm×2.0 cm,未侵及浆膜外。切除肿瘤。术后病理:(胃壁肿瘤)灰白不规则组织,大小2.5 cm×2.0 cm×1.5 cm,上附灰黄脂肪样组织,诊断为深在性囊性胃炎(gastritis cystica profunda,GCP),腺体下陷肌层(
1972年Littler和Gleibermann[1]首次报道了1例胃肠吻合处胃黏膜脱垂伴囊状浸润性增生的患者,将其命名为囊状息肉状胃炎。此后此病陆续被报道,依据病变累及深度,有囊状胃炎、液性囊性胃炎等不同称谓。直至1981年Franzin和Novelli[2]发现这种腺体改变类似发生于结肠的深在性囊性结肠炎病变特点,指在炎性刺激下胃黏膜内的腺体向黏膜肌层以下生长并扩张成囊的一种病变,建议命名为GCP,后来被广泛接受。起初此病多见于胃部手术患者,因而认为是一种可能与手术有关的病变。由于慢性炎症、缺血、手术、异物等因素损伤黏膜肌层,使其局限性断裂,胃腺上皮从固有膜穿过黏膜肌层向黏膜下层移行所致。后来发现该病变不仅局限于胃部手术患者,因此认为该病也可能是一种变性病变。常规胃镜活检取材较表浅有时难以取到病变,故胃镜取材的深度对该病明确诊断有较大影响。GCP的临床表现无特异性,可表现为腹部或胸骨后疼痛、腹泻、恶心呕吐、腹部不适、食欲下降、消瘦等,也可因病灶出血出现黑便、贫血等。上消化道造影可发现局限性充盈缺损或无明显异常。胃镜可见息肉样隆起病变,也可仅见黏膜充血。超声内镜检查特异性较高,可见胃壁增厚及黏膜下层低回声区。组织病理检查,除淋巴细胞、单核细胞、活动性炎性反应外,还可见腺体间质结蹄组织增生,病灶处上皮细胞增生。胃腺体在黏膜深层及黏膜下浸润呈囊性扩张,扩张的腺体较规则、完整,与胃癌存在区别[3]。
本例临床表现无特异性,胃镜仅提示浅表性胃炎,活检取材常难以取得病变,故GCP术前确诊困难。国内报道的GCP多通过超声内镜确诊,其余均通过胃大部分切除术后病理确诊[4]。CT诊断GCP罕见报道,本例病灶位于贲门小弯侧,黏膜下胃壁间囊性病变,黏膜面略显毛糙,浆膜面光整,病灶内未见明显积气或液平面,所以术前除外憩室,考虑为黏膜下良性囊性病变,神经鞘瘤或间质瘤囊性变可能。CT对鉴别胃壁或网膜来源的病变有明显优势[5],超声内镜结合CT有利GCP的诊断[6]。本例病灶术前CT定位诊断明确,纠正了术前超声相对模糊的定位诊断。但术前未能做出正确病理评估,可能与对本病认识不足有关。发生于胃壁上的囊性病变,囊壁与胃壁浆膜面连续、光整,黏膜面毛糙,CT增强不强化或仅轻度渐进性强化时要考虑到此病。笔者认为上述CT表现可能属于GCP相对特异的影像特征,但仍需进一步研究。
GCP主要应与胃癌、胃肠道重复性囊肿、憩室相鉴别。胃癌胃镜下病变隆起处黏膜色泽与周围正常胃黏膜不同,表面糜烂、溃疡或附着污苔等,周围黏膜组织僵硬,黏膜面明显强化,GCP一般无此类征象。胃肠道重复性囊肿多发病于婴幼儿[7],成人罕见,有时会伴发其他畸形[8]。典型胃憩室好发于胃窦部,一般可见憩室口,与胃腔相通,腔内会积液积气,如果憩室口封闭,影像鉴别困难。GCP还需与神经肠源性囊肿、肥厚性胃炎、间质瘤、神经源性肿瘤、胃淋巴瘤等相鉴别。尽管GCP是良性病变,但长期慢性炎性刺激存在,可能会诱导或并发胃癌,故一般需要手术切除治疗。
[1] Littler ER, Gleibermann E. Gastritis cystica polyposa. (Gastric mucosalprolapse at gastroenterostomy site, with cystic and infiltrative epithelialhyperplasia) [J]. Cancer,1972,29(1):205-209.
[2] Franzin G, Novelli P. Gastritis cystica profunda[J]. Histopathology.1981.5(5):535-547.
[3] 沈玲燕,周贤斌,杜娟,等.深在性囊性胃炎1例及文献复习[J].国际消化病杂志,2015,(5):369-370.
[4] 岳晓红,张春礼,明亮,等.深在性囊性胃炎15例诊疗体会[J].中华普通外科杂志,2014,29(8):620-622.
[5] 董鹏,王滨,张仕状,等.CT定位诊断网膜囊原发性和胃源性占位性病变的价值[J].中华放射学杂志,2007,41(7):721-723.
[6] 谭韡,周巍,罗和生,等.深在性囊性胃炎7例临床特点分析[J].疑难病杂志,2017,16(6):627-629.
[7] 任红霞,吴晓霞,孙小兵,等.腹腔镜诊治新生儿胃重复畸形[J].中华小儿外科杂志,2016,37(2):144-146.
[8] 王琦,邓子清,杨小峰,等.成人胃重复囊肿伴异位胰腺1例[J].中南大学学报(医学版),2017,42(5):596-599.
