基于肾窦间隙解剖的肾唇重建技术在肾门肿瘤机器人保留肾单位手术中的应用:单中心286例分析
2018年6期
中华泌尿外科杂志,第39卷第6期 第413页-第418页
高宇,张旭,马鑫,李宏召,王保军,史涛坪
肾门肿瘤的概念为肿瘤紧邻肾门大血管(动脉、静脉)和集合系统[1]。针对此部位肿瘤的保留肾单位手术是较大挑战,肿瘤切除时可能引起肾门血管和集合系统损伤,而肾脏缺损重建时需防止创面出血和漏尿,同时避免缝扎大血管和集合系统[1]。机器人手术具有3D视野、灵活的缝合角度以及第3机械臂辅助功能等明显优势,更适合于肾门肿瘤的保留肾单位手术。鉴于此,本研究回顾性分析2013年6月至2016年12月我院实施机器人辅助腹腔镜保留肾单位手术治疗的286例肾门肿瘤患者的临床资料,以探讨基于肾窦间隙解剖的肾唇重建技术(Garland技术)处理肾门肿瘤的解剖基础、技巧方法和疗效。
本组286例。男202例,女84例。年龄(56.2±9.2)岁。体重指数(26.8±3.5)kg/m2,肿瘤最大径中位值为2.6cm(0.8~6.0)cm, R.E.N.A.L.评分为(8.2±1.8)分,所有患者术前血清eGFR、尿素氮均正常。术前eGFR为(84.5±19.6 )ml/(min·1.73 m2)。
术前腹部CT及磁共振检查示肾唇占位性病变,紧邻肾门大血管(
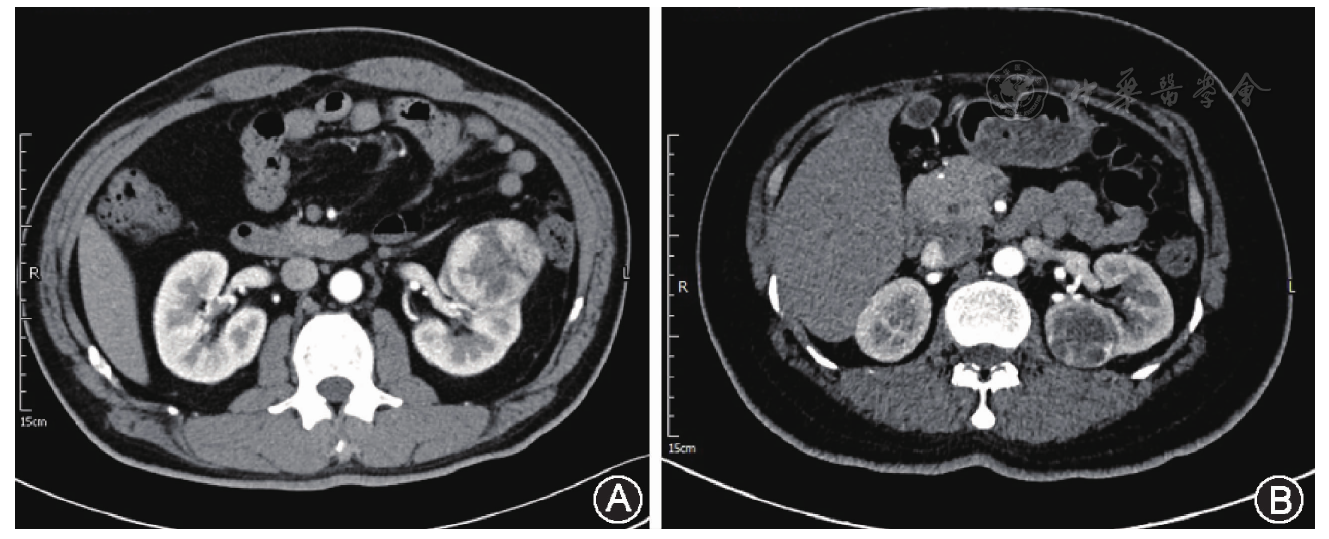
肾门前唇肿瘤选择经腹腔入路,肾门后唇肿瘤采用经腹膜后入路进行肿瘤切除和创面缝合。
机器人辅助腹腔镜保留肾单位手术(经腹腔入路):麻醉后健侧斜卧45°体位,调整手术床使患侧腰部抬高。建立气腹后,取脐部外上方2 cm皮肤切口作为机器人系统镜头孔,分别于镜头孔上方肋缘下、患侧麦氏点、镜头孔下方10 cm腹直肌旁做皮肤切口,分别为机器人系统第1、2、3机械臂孔,于剑突与脐连线中点及剑突下2 cm分别做12 mm和5 mm切口为辅助孔。
机器人辅助腹腔镜保留肾单位手术(经腹膜后入路):麻醉成功后健侧卧位,调整手术床抬高患侧腰部。取腋中线上髂嵴与肋缘连线中点做长约3 cm切口,依次切开皮肤、皮下,钝性分开肌肉和筋膜,示指扩张通道后,置入球囊扩张器,充气600 ml扩张腹膜后手术操作空间,取该切口为镜头孔。于镜头孔旁开一掌左、右侧分别做皮肤切口并置入机器人专用8 mm套管,为第1、2机械臂孔,于镜头孔与腹侧机械臂连线中点下方约5 cm处,做12 mm切口置入套管作为辅助孔。
首先在肾脂肪囊内进行肾脏游离,充分显露肿瘤的边界(
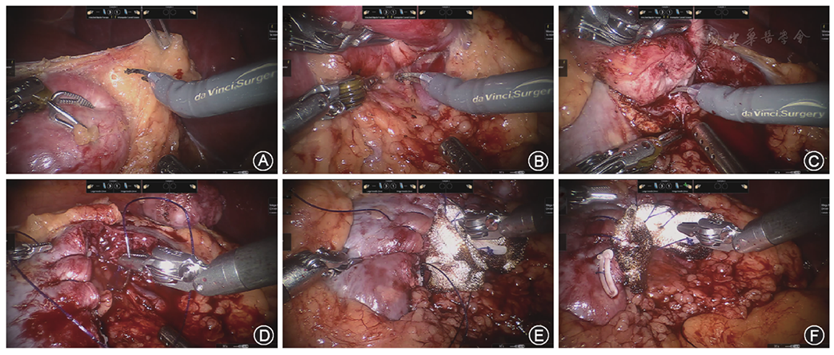
在切除肿瘤之前,需仔细辨认肿瘤与正常肾实质的边界。对于外生型肿瘤,此时由于第3机械臂对肿瘤托举的张力,"拱桥"两端肿瘤与肾实质交界处组织相对较薄,此处也是肿瘤切除的起始点。必要时术中可使用超声引导,划定肿瘤的边界,指导精准切除。切除时利用第3臂的牵拉和悬吊,钝性分离和锐性切除相结合,可以较为迅速地找到肿瘤边界,甚至假包膜,保证肿瘤切缘阴性的同时最大限度地保留肾单位(
肾脏巨大创面,很难对合。我们在进行肾唇重建时予最小张力进行缝合,使用1-0 Quill线连续全层缝合创面,提前在线尾固定1枚Hem-o-lok夹。从肾门部肾脏创面的肾窦侧进针,针背贴着肾静脉属支表面,利用针的弧度,从肾皮质出针,连续全层缝合至肾门部肾脏创面闭合(
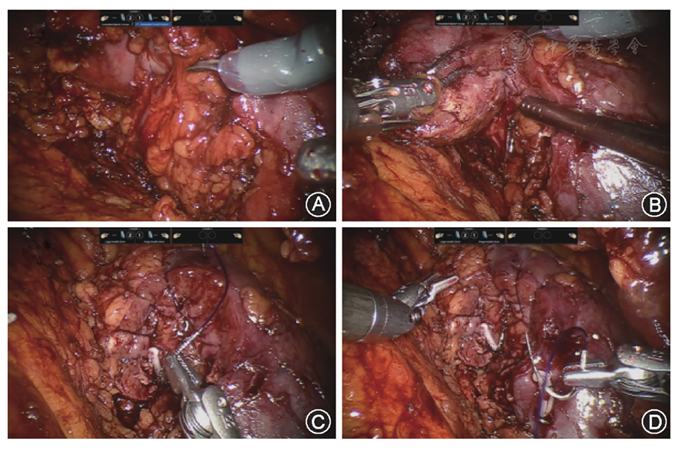
采用SPSS 18.0统计软件处理数据,所有数据进行正态性检验,符合正态分布的计量资料采用
本组286例中,经腹腔入路197例(68.9%),经腹膜后入路89例(31.1%)。284例保留肾单位手术顺利完成,无中转开放病例;2例术中转根治术,其中1例术中发现肿瘤卫星灶,另1例术中出现难以控制的创面出血。284例手术时间中位值为120 min(60~230 min),肾动脉阻断时间为(18.2±4.1)min,术中出血量中位值100 ml(10~600)ml。术中修补肾静脉主干或较大属支明确破损9例,术中、术后输血2例。284例术后住院时间中位值为4 d(2.0~9.0 d),无血尿、尿漏、动静脉瘘、假性动脉瘤等术后并发症。
在284例成功行保留肾单位手术的病例中,病理检查结果示切缘阳性3例(1.1%),余281例切缘阴性。病理类型:透明细胞癌260例(91.5%),嫌色细胞癌8例(2.8%),乳头状肾细胞癌7例(2.5%),嗜酸性细胞瘤5例(1.8%),血管平滑肌脂肪瘤3例(1.1%),黏液小管梭形细胞癌1例(0.3%)。
284例患者中位随访36个月(12~54个月),失访率为7.7%(22/284)。术后1 d eGFR为(72.6±22.9)ml/(min·1.73 m2),术后6个月eGFR为(83.2±21.1)ml/(min·1.73 m2),所有患者术后肾功能恢复良好。术后局部复发3例(1.1%),其中1例为发现切缘阳性后5个月出现肿瘤局部复发,另2例分别于术后9、11个月复发,均于我院行根治性肾切除术,恢复良好。284例无肿瘤远处转移,总体生存率100%。
机器人和腹腔镜保留肾单位手术是T1a期肾癌治疗的金标准[2,3]。欧洲一项多中心Ⅲ期临床试验结果表明,与根治性肾切除术相比,肾功能正常患者保留肾单位手术后远期出现慢性肾功能不全风险显著下降[4]。所以目前绝大多数文献报道外凸于肾表面的T1期肾肿瘤首选机器人或腹腔镜保留肾单位手术[5]。在临床实践中,随着技术的发展,部分中心尝试对肾门肿瘤、完全内生型肾肿瘤、肾窦内肿瘤等特殊类型选择实施保留肾单位手术[6,7,8,9]。
肾门肿瘤的概念为肿瘤紧邻肾门大血管(动脉、静脉)和集合系统[1]。针对此部位肿瘤的保留肾单位手术难度较其他部位肿瘤手术明显增加。肿瘤切除时可能伤及血管和集合系统,而修复肾脏缺损时既要避免围手术期创面出血和漏尿,又要避免缝扎大血管和集合系统,以免引起肾单位损失和集合系统损伤。
有研究结果表明,在肿瘤学控制和肾功能保留方面,机器人保留肾单位手术与腹腔镜手术和开放手术效果相当,但在围手术期指标方面,机器人手术能显著减少术中出血量、术后住院时间等[10,11]。具有3D手术视野、更灵活的缝合角度和速度以及第3机械臂辅助功能等明显优势的机器人更适合于肾门肿瘤的保留肾单位手术。
临床实践中对于肾门肿瘤的治疗,国内外多个中心进行了较多探索,获得了较为满意的结果。Gill等[1]报道了2001—2004年对25例肾门肿瘤患者行腹腔镜保留肾单位手术的资料,无中转开放病例,也无需术后任何介入治疗,是较早的对肾门肿瘤成功行保肾手术的报道。Lattouf等[8]报道了2000—2006年行保留肾单位手术的18例肾门肿瘤患者的资料,中位随访时间为26个月,无肿瘤局部复发和全身进展。一项多中心研究比较了机器人保留肾单位手术处理肾门肿瘤和非肾门肿瘤的围手术期数据和肿瘤学随访结果,对于肾动脉阻断时间,肾门肿瘤组显著高于非肾门肿瘤组[(26.3±7.4) min与(19.6±10.0) min]。其他术中术后并发症发生率以及远期随访肿瘤复发率的差异并无统计学意义[12]。国内俞鸿凯等[13]最早报道了应用机器人技术对肾门肿瘤成功实施保留肾单位手术,对肾门解剖学原理进行了阐述,初步探索了新的肾门肿瘤处理方法和技巧。
针对肾门肿瘤进行手术设计,首先是手术入路的选择,对于肾门前唇肿瘤,我们采用经腹腔途径,优势在于该途径能够直接显露前唇肿瘤,空间充足,操作方便,尤其是第3臂的使用能够帮助牵拉瘤体,有助于肾窦间隙的显露和肿瘤切除。经腹膜后入路适用于肾门后唇肿瘤。我国后腹腔镜技术比较成熟,术者对腹膜后解剖结构较为熟悉,可以直接分离出肾动脉而不被肾静脉干扰[14]。
肾门部位肿瘤紧邻肾蒂血管和集合系统,无论是肿瘤切除还是创面缝合,难度都非常大。我们受到治疗鹿角形肾结石的启示:在肾窦脂肪囊包膜平面,分离肾窦间隙,能够清晰显露肾门血管和肾实质之间的解剖层面,采用肾实质肾盂分层切口处理结石[15]。常规的肾部分切除术是先从肿瘤边缘切开肾实质,逐步深入到肿瘤的基底部。然而在切除肾门肿瘤时,不能沿用这种"由表及里"的常规方法,因其容易损伤肾门大血管。以肾门前唇肿瘤处理为例,我们首先对肾窦间隙进行充分游离,沿肾静脉及其属支表面尽量往深处分离,找到肾肿瘤的基底部,将血管和肿瘤基底分开,利用稳定的第3臂托起瘤体,保持合适的张力,形成"拱桥样"形状,切除起始点为瘤体与肾实质相连的最薄处,由一侧向肾门方向钝性分离结合锐性切除,保证肿瘤完整切除,切除过程中应用可吸收夹离断肿瘤穿支血管。
肾门肿瘤手术的关键步骤还在于肾脏创面的对合方式。肿瘤切除后在肾门部位留下了较大的创面,Benway等[16]介绍的Hem-o-lok间断减张对合创面的方法,能够成功完成保留肾单位手术。Khalifeh等[17]报道了"V"形肾门对合技术关闭肾门创面的方法,但是在实际临床应用中,在肾脏缺损的创面巨大时,采用上述技术处理创面张力仍然较大。我们早期在腹腔镜下应用Garland技术成功实施了多例肾门肿瘤保留肾单位手术,但是手术难度较大,肾动脉阻断时间较长,术中出血量较多。近年来迅速发展的机器人技术使手术视野更加稳定,缝合角度更佳,缝合速度大幅提高,使Garland技术应用更加成熟。这种从肾门向肾实质逆行进针,连续全层缝合的方法以最小张力关闭肾脏创面,又避免了损伤肾盂和肾门大血管。对于肾门前唇肿瘤,因其毗邻肾静脉及其属支,将止血纱布叠成卷状压在肾实质创缘上,用可吸收倒刺线将止血纱布卷缝合填压在肾脏创面上,可有效压迫肾静脉属支微小缺损的出血。对于肾门后唇肿瘤,由于邻近肾动脉及其分支,常无需第2层止血纱布卷加压缝合,但对于一些病例,肾静脉属支和肾动脉走行有交叉缠绕,也可能导致肾静脉属支微小破损,因此也需第2层加压缝合。
本研究为目前国内外较大规模的单中心肾门肿瘤机器人保留肾单位手术报告,在284例行保留肾单位手术的患者中,病理结果切缘阳性3例(1.1%),集中在机器人手术开展早期,可能与术者手术学习曲线有关,中位随访36个月(12~54个月),术后患者总肾功能复查全部正常,但是本研究的缺陷在于缺乏分肾功能检查,无法评估患侧肾脏术后恢复情况。术后局部复发3例(1.1%),后于我院行根治性肾切除术,恢复良好。所有病例无肿瘤远处转移,总体生存率100%。这里需要说明,切缘阳性病例和术后复发病例并非一一对应,仅1例发现切缘阳性后5个月复查示肿瘤局部复发,遂行根治性肾切除术,术后恢复良好。值得注意的是,复发的3例患者术前影像学表现共同点是肿瘤假包膜征象不清晰,形状不规则,所以对于此类病例,保肾手术需再严格评估,术后需要严密随访。
综上所述,机器人保留肾单位手术处理肾门肿瘤安全可行,根据肿瘤位置选择合适入路,在充分显露肾窦间隙基础上,进行肾门肿瘤的切除和肾唇重建,Garland技术能够有效避免术后创面出血、术后漏尿、动静脉瘘、假性动脉瘤等并发症。远期肿瘤学控制和肾功能恢复良好,患者获得满意的总体生存率。
[1] Gill IS, Colombo JR
[2] Volpe A, Blute ML, Ficarra V, et al. Renal ischemia and function after partial nephrectomy: a collaborative review of the literature [J]. Eur Urol, 2015, 68: 61-74.
[3] 张树栋,马潞林. 2017年欧洲泌尿外科学会年会肾癌指南更新及研究进展[J]. 中华泌尿外科杂志,2017,38: 485-488.
[4] Scosyrev E, Messing EM, Sylvester R, et al. Renal function after nephron-sparing surgery versus radical nephrectomy: results from EORTC randomized trial 30904 [J]. Eur Urol, 2014, 65: 372-377.
[5] Campbell S, Uzzo RG, Allaf ME, et al. Renal mass and localized renal cancer: AUA guideline [J]. J Urol, 2017, 198: 520-529.
[6] Lee H, Oh JJ, Byun SS, et al. Can partial nephrectomy provide equal oncological efficiency and safety compared with radical nephrectomy in patients with renal cell carcinoma (>/=4 cm)? A propensity score-matched study [J]. Urol Oncol, 2017, 35: 379-385.
[7] Caputo PA, Zargar H, Ramirez D, et al. Cryoablation versus partial nephrectomy for clinical T1b renal tumors: a matched group comparative analysis [J]. Eur Urol, 2017, 71: 111-117.
[8] Lattouf JB, Beri A, D'Ambros OF, et al. Laparoscopic partial nephrectomy for hilar tumors: technique and results [J]. Eur Urol, 2008, 54: 409-416.
[9] Wang B, Gong H, Ma X, et al. Retroperitoneal laparoscopic nephrotomy along the brodel line and tumor enucleation for complete intraparenchymal renaltumors: a single institution experience [J]. J Endourol, 2017, 31: 1044-1048.
[10] 夏丹,王平,秦杰,等. 经腹膜后和经腹途径机器人辅助腹腔镜下肾部分切除术围手术期比较分析[J]. 中华泌尿外科杂志,2016,37: 81-84.
[11] Chang KD, Abdel Raheem A, Kim KH, et al. Functional and oncologic outcomes of open, laparoscopic and robotic partial nephrectomy: a multicenter comparative matched-pair analyses with a median 5 years follow up [J]. BJU Int, 2018[
[12] Dulabon LM, Kaouk JH, Haber GP, et al. Multi-institutional analysis of robotic partial nephrectomy for hilar versus nonhilar lesions in 446 consecutive cases [J]. Eur Urol, 2011, 59: 325-330.
[13] 俞鸿凯,马鑫,李宏召,等. 一种新的肾门前后唇巨大肾门肿瘤的肾部分切除术外科技术及其局部解剖学原理(附18例报告) [J]. 微创泌尿外科杂志,2015, 6: 163-166.
[14] 吕香君,张旭,马鑫,等. 经后腹腔与经腹腔入路机器人肾部分切除术的对照研究:单中心418例报告 [J]. 中华泌尿外科杂志,2016, 37: 641-646.
[15] 张旭,叶章群,李家贵,等. 肾实质肾盂分层切口治疗复杂性肾鹿角状结石 [J]. 临床泌尿外科杂志,1999, 14:
[16] Benway BM, Wang AJ, Cabello JM, et al. Robotic partial nephrectomy with sliding-clip renorrhaphy: technique and outcomes [J]. Eur Urol, 2009, 55: 592-599.
[17] Khalifeh A, Autorino R, Hillyer SP, et al. V-hilar suture renorrhaphy during robotic partial nephrectomy for renal hilar tumors: preliminary outcomes of a novel surgical technique [J]. Urology, 2012, 80: 466-471.