基于全基因组测序技术分析深圳市人民医院2008—2016年碳青霉烯类耐药大肠埃希菌的耐药基因及分子流行病学特征
2020年11月
中华内分泌代谢杂志,第43卷第11期 第1086页-第1092页
林豪芸,梁训宏,胡珍,卢月梅,吴劲松,吴文苑
大肠埃希菌是临床上常见的病原菌之一。据2018年中国细菌耐药监测网公布数据显示大肠埃希菌分离菌株数量居临床分离菌种的榜首[1]。近年来多重耐药已经成为21世纪全球公共卫生面临的最重要的威胁之一。大肠埃希菌多重耐药的主要机制是产超广谱β内酰胺酶(extended-spectrum β-lactamase,ESBL)及AmpC酶,亚胺培南、美罗培南等碳青霉烯类抗菌药物是治疗该类耐药菌感染的最有效抗菌药物。然而,碳青霉烯类耐药大肠埃希菌(carbapenem-resistant escherichia coli,CR-ECO)的出现限制了该类抗菌药物的选用,使感染者的死亡率升高,严重威胁着人类健康[2]。大肠埃希菌对碳青霉烯类抗菌药物的耐药机制在不同国家和地区之间存在差异,深圳市人民医院接收病源以外来人口居多,人口流动量大,病原菌的耐药机制有自己的特点。
临床微生物实验室多局限于CR-ECO的表型检测,其准确性有限,且不能明确耐药的具体机制。碳青霉烯酶检测的金标准为基因检测方法,常用的有聚合酶链反应(polymerase chain reaction,PCR),但PCR操作繁琐且难以识别检测体系以外的耐药因子,所以在实际操作中也受到限制。近年来随着二代测序技术的快速发展,解决通量问题后,其检测成本已大大降低。通过对培养皿上的病原菌进行全基因组测序(whole genome sequencing,WGS),实验室可获得该菌株的所有DNA信息。
本研究收集了深圳市人民医院从2008年1月1日至2016年12月31日的CR-ECO共16株。将这16株菌株进行常规碳青霉烯酶表型检测的同时也通过WGS分析其相关耐药信息和分子生物学要点,从而展现深圳地区CR-ECO的菌群特点。
连续收集深圳市人民医院检验科微生物实验室2008—2016年的CR-ECO菌株共16株。其中样本来源包括血液5株,尿液3株,腹透液3株,引流液2株,分泌物1株,胆汁1株,心包积液1株。16株CR-ECO感染的患者分别来自重症监护室(7株),老年科(2株),神经外科(2株),肝胆外科(1株),胃肠外科(1株),心内科(1株),血液内科(1株),呼吸重症监护室(1株)。年龄24~87岁,男性11例,女性5例。所有菌株均为不同来源标本非重复菌株。
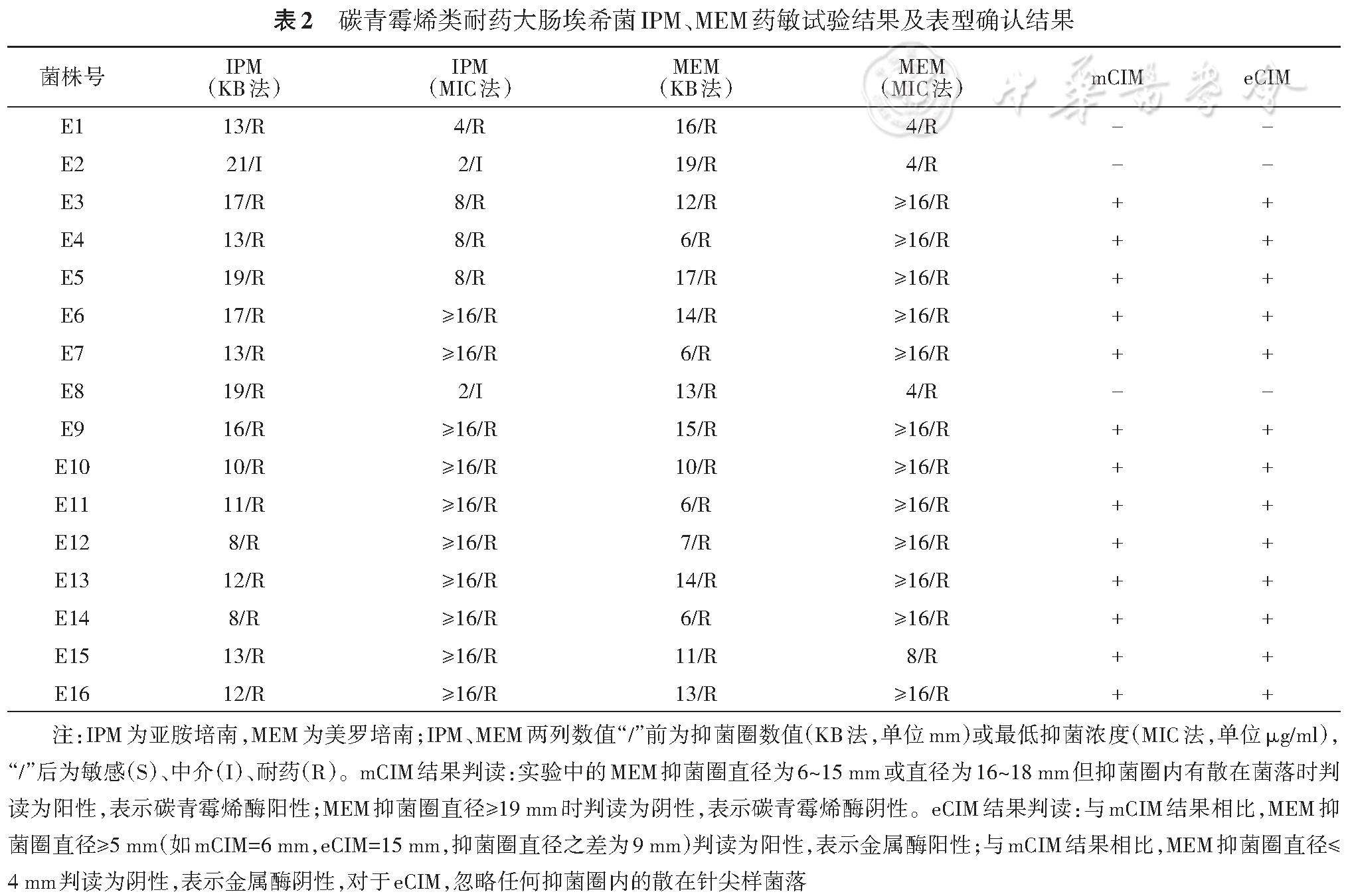
所有菌株均采用Vitek MS(法国梅里埃公司)鉴定为大肠埃希菌,鉴定值为99.9%,且以药敏试验纸片扩散法(药敏纸片,英国Oxoid公司)为初次筛选方法测得美罗培南(含量10 μg)抑菌圈值≤19 mm和(或)亚胺培南(含量10 μg)抑菌圈值≤19 mm,同时采用全自动细菌鉴定药敏仪VITEK 2(法国梅里埃公司)和N335药敏卡进行药敏试验。16株菌株均采用改良碳青霉烯类失活法(modified carbapenem inactivation method,mCIM)和EDTA碳青霉烯类失活法(EDTA carbapenem inactivation method, eCIM)进行表型确证。mCIM可用于检测肠杆菌科细菌中的碳青霉烯酶,eCIM与mCIM联合使用可用于区分肠杆菌科细菌产金属-β内酰胺酶型和丝氨酸碳青霉烯酶型。大肠埃希菌ATCC25922为药敏试验质控菌株。肺炎克雷伯菌35492(KPC-2阳性,丝氨酸碳青霉烯酶产生株)、肺炎克雷伯菌ATCC 13883(碳青霉烯酶阴性株)、肺炎克雷伯菌34978(NDM-1阳性,金属β内酰胺酶产生株)为mCIM和eCIM实验方法的质控菌株。
采用细菌基因组DNA提取试剂盒(北京天根公司)根据操作说明提取DNA。通过Qubit荧光定量仪检测保证DNA样本浓度>20 ng/μl,总量≥1.5 μg,A260/A280=1.8~2.0。采用NEBNext Ultra DNA文库构建试剂盒(美国illumina公司)进行文库构建。利用HiSeq测序平台进行双末端测序,测序仪:NovaSeq 6000,测序策略:PE 150。WGS委托深圳海一时代基因科技有限公司进行。
1.每个样品的基因组测序后得到的illumina测序数据,先进行低质量数据过滤。
2.样品全基因组组装:使用SOAPdenovo(版本:2.04,
3.基因预测:使用GeneMarkS(版本:4.6b,
4.基因功能注释:通过比对NR、KEGG、COG、GO及Swiss-Prot等5个数据库进行基因功能注释,查找候选的外排泵系统相关基因,再与各菌株的CARD抗性相关基因数据库注释结果进行交集判断,找出与抗性相关的外排泵系统相关基因。通过CARD数据库及CGE中的ResFinder查找产碳青霉烯酶耐药基因、β内酰胺酶耐药基因、AmpC酶耐药基因。通过CGE查找菌株的血清分型、多位点序列分型(multilocus sequence typing,MLST)分型。功能数据库的注释均使用BLAST软件比对得到。
选择参考序列,在GenBank里挑选7株大肠埃希菌的完整基因组作为参考序列,分别是E.coli.K12.MG1655、E.coli.ATCC.25922、E.coli.IAI39、E.coli.O104.H4.2011C.3493、E.coli.O157.H7.Sakai、E.coli.O83.H1.NRG.857C和E.coli.UMN026。
利用MUMmer比对软件,找差异位点并进行初步过滤,测出潜在单核苷酸多态性(single nucleotide polymorphism, SNP)位点;提取参考序列SNP位点两边各100 bp序列,使用BLAT(版本:35,
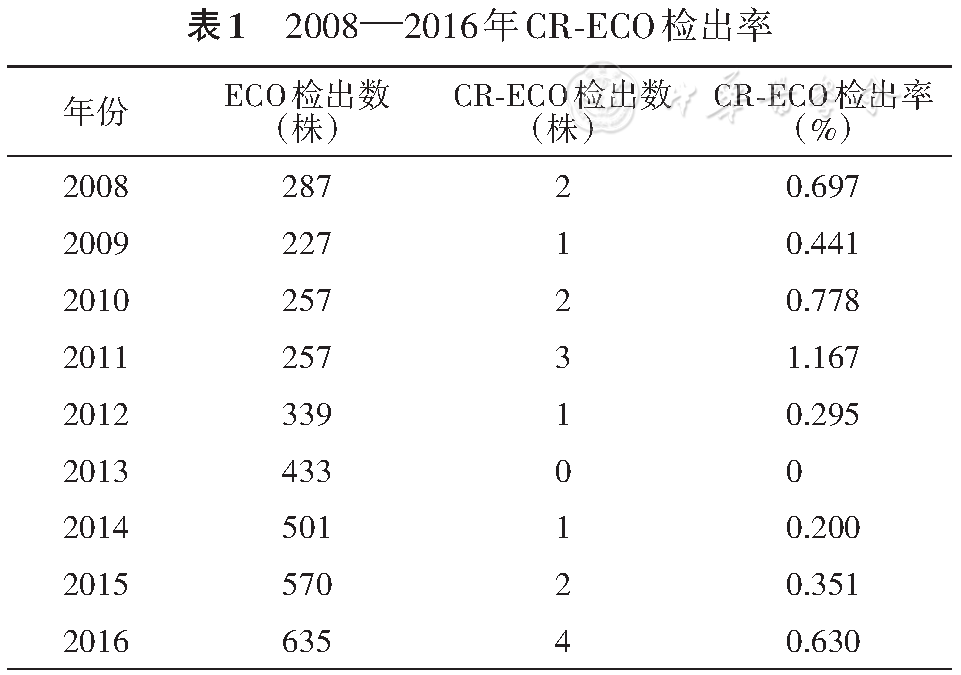
在16株大肠埃希菌中,对亚胺培南的耐药率15/16;对美罗培南耐药率为16/16;对氟喹诺酮类药物环丙沙星耐药率为12/16。另外对于头孢类抗菌药物包括头孢克洛、头孢噻肟、头孢曲松、头孢他啶及头孢吡肟的耐药率为16/16。对氨曲南耐药率为11/16。对头霉素类抗菌药物头孢西丁耐药率为16/16。对氨基糖苷类药物庆大霉素耐药率为13/16。利用mCIM和eCIM实验方法对16株CR-ECO进行表型确证,结果显示mCIM阳性菌株13株、阴性菌株3株,eCIM阳性菌株13株、阴性菌株3株(
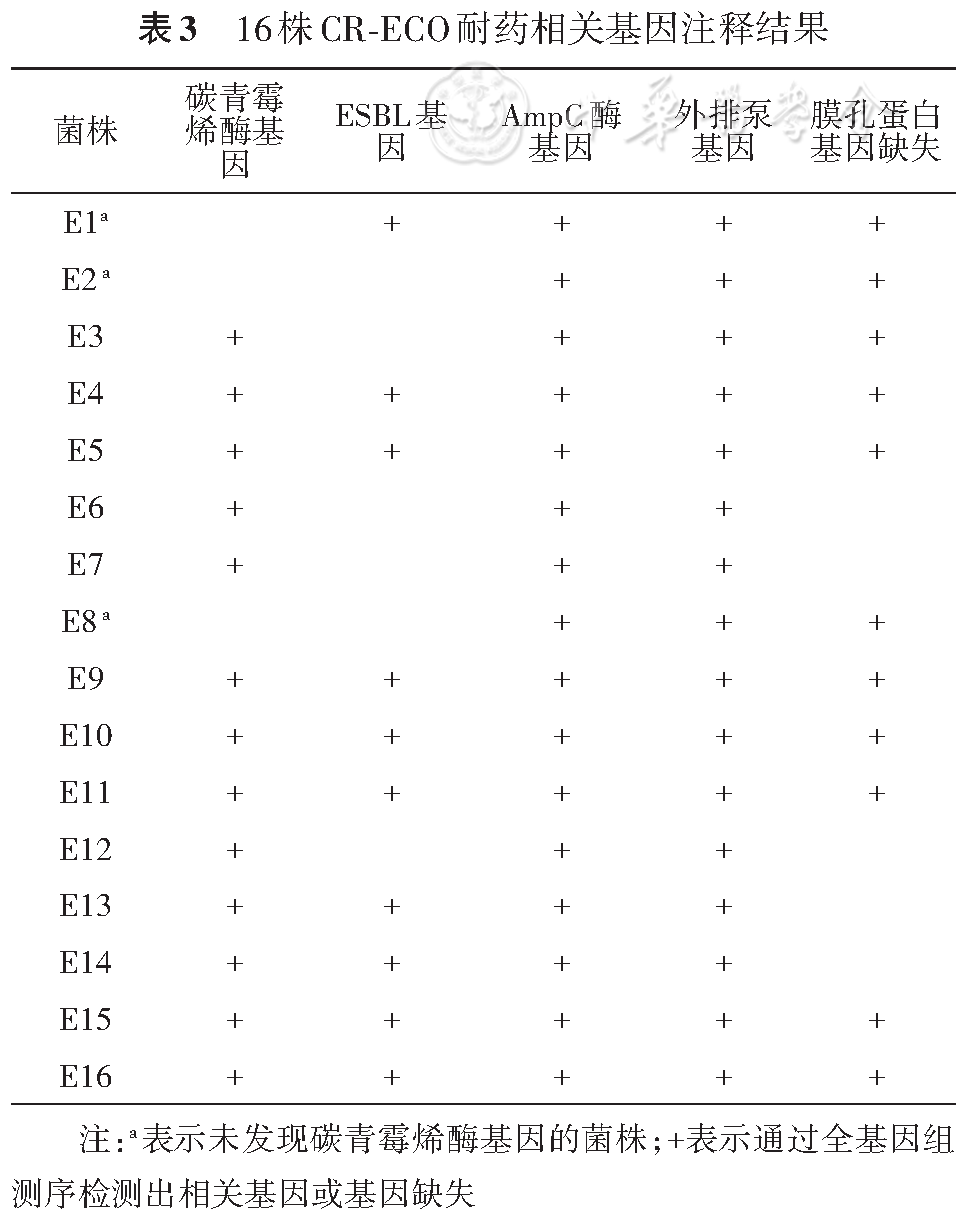
碳青霉烯类耐药的主要机制包括产碳青霉烯酶、AmpC酶或ESBL高表达,膜孔蛋白缺失或改变以及外排泵。16株CR-ECO经过WGS,再对其耐药相关基因进行注释后发现,所有菌株同时存在多种耐药机制相关基因。如有7株CR-ECO均被检测出碳青霉烯酶基因、ESBL基因、AmpC酶基因和外排泵基因,以及存在膜孔蛋白基因缺失。而有3株CR-ECO未发现碳青霉烯酶基因,但是存在其他耐药机制相关基因(
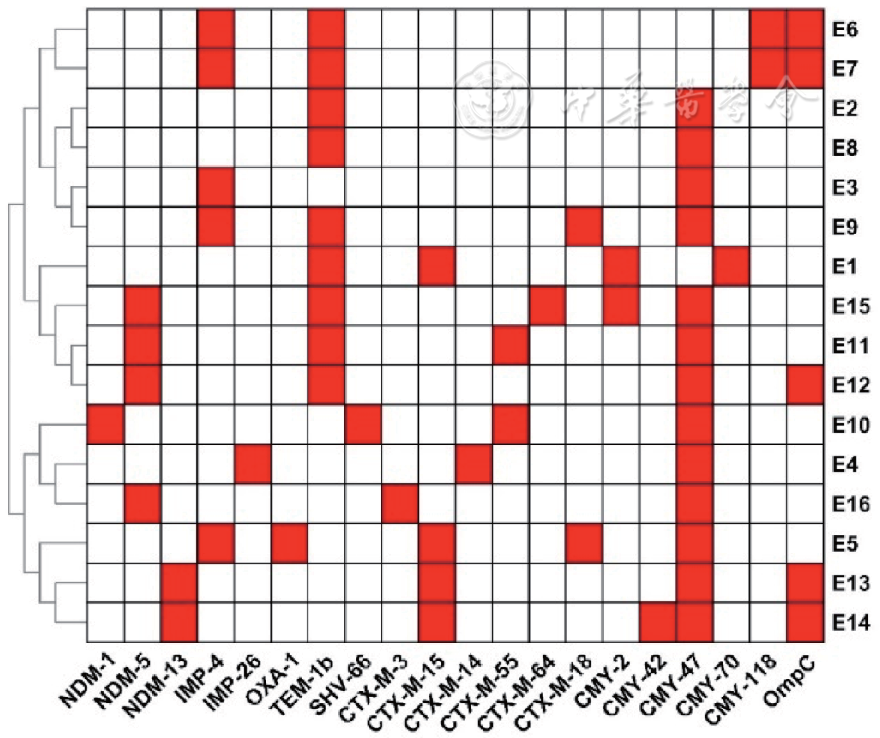
碳青霉烯酶基因按照Ambler分子分类主要可分为A、B、D三类,A类为丝氨酸蛋白质酶,包括KPC、IMI、SME、NMC-A、FRI、GES,B类为金属型-β内酰胺酶(Metallo-β-lactamase,MBL),包括NDM、VIM、IMP、GIM、SIM、SPM,D类为OXA酶,包括OXA-48、OXA-181、OXA-23等。通过CARD、ResFinder筛选碳青霉烯类耐药基因及膜孔蛋白基因。16株CR-ECO产碳青霉烯酶以MBL为主,主要包括NDM-1(1株),NDM-5(4株),NDM-13(2株),IMP-4(5株),IMP-26(1株)。其余3株通过比对未找到相关碳青霉烯酶基因,但这3株菌株均表达包括CMY、CTX-M、SHV、TEM-1b等在内的AmpC酶、ESBL、广谱β-内酰胺酶等β-内酰胺酶耐药基因。另外共11株CR-ECO有膜孔蛋白OmpC基因缺失(
革兰阴性菌主要通过位于细胞质膜上的蛋白、周质间隙中的融合蛋白(membrane fusion protein, MFP)及外膜上的外排蛋白(outer membrane protein,OMP)来组成外排泵系统。外排泵蛋白常位于胞质膜上,目前被分为:易化因子超家族(major facilitator superfamily,MFS);ATP耦联盒超家族(ATP-binding cassette superfamily,ABC);小多重耐药家族(the small multidrug resistance family,SMR);耐药结节化细胞分化家族(resistance-nodulation-division superfamily,RND)和多药与毒物外排家族(multidrug and toxic compound extrusion family MATE)五大类。所有外排泵蛋白中以RND家族最常见。RND家族已被证实在革兰阴性菌的耐药改变中起着很大作用。
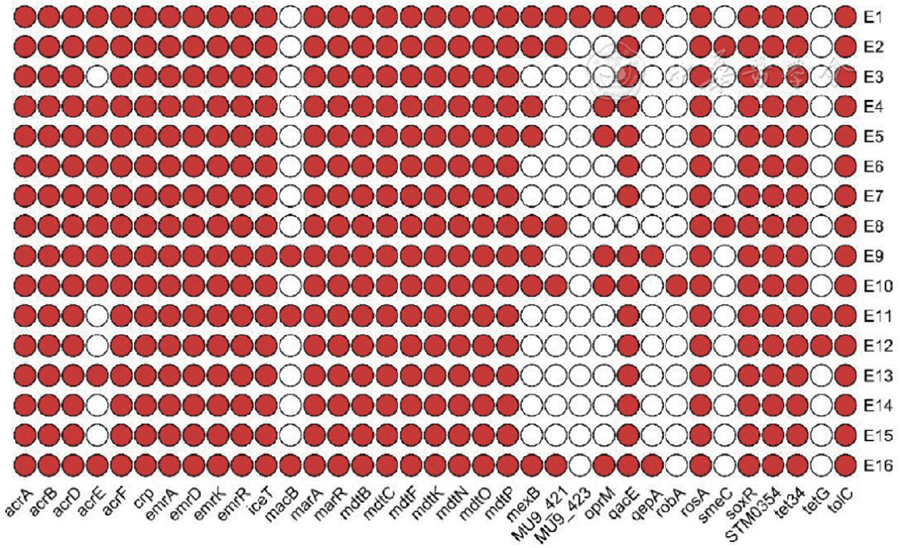
16株CR-ECO的外排泵相关基因种类丰富,经比对基因注释结果共有442个。其中以编码RND家族的基因最多,主要包括所有菌株(16株)都携带的acrB、acrF、acrD、mdtB、mdtC、mdtF基因,以及部分菌株(8株)携带的mexB基因;而16株菌株中也有大部分菌株携带编码MFS家族外排泵的emrD(16株)、emrK(16株)、iceT(16株)、tet34(16株)、tetG(2株)、MU9_421(5株)、qepA(3株)基因;有15株菌株表达了编码SMR型外排泵的qacE(15株)基因;所有菌株均携带编码MATE型外排泵的mdtK基因;还有3株菌株同时携带了编码ABC型外排泵的macB基因。除编码外排泵蛋白的基因外,acrA(16株)、acrE(11株)、emrA(16株)、mdtN(16株)基因主要构成外排泵系统中MFP;而tolC(16株)、oprM(6株)、smeC(2株)、mdtP(16株)为编码OMP的基因;其余基因:marA(16株)、marR(16株)、soxR(16株)、crp(16株)、emrR(16株)、STM0354(16株)、robA(16株)主要参与外排泵系统中的遗传调控。16株CR-ECO的外排泵相关基因的具体分布如
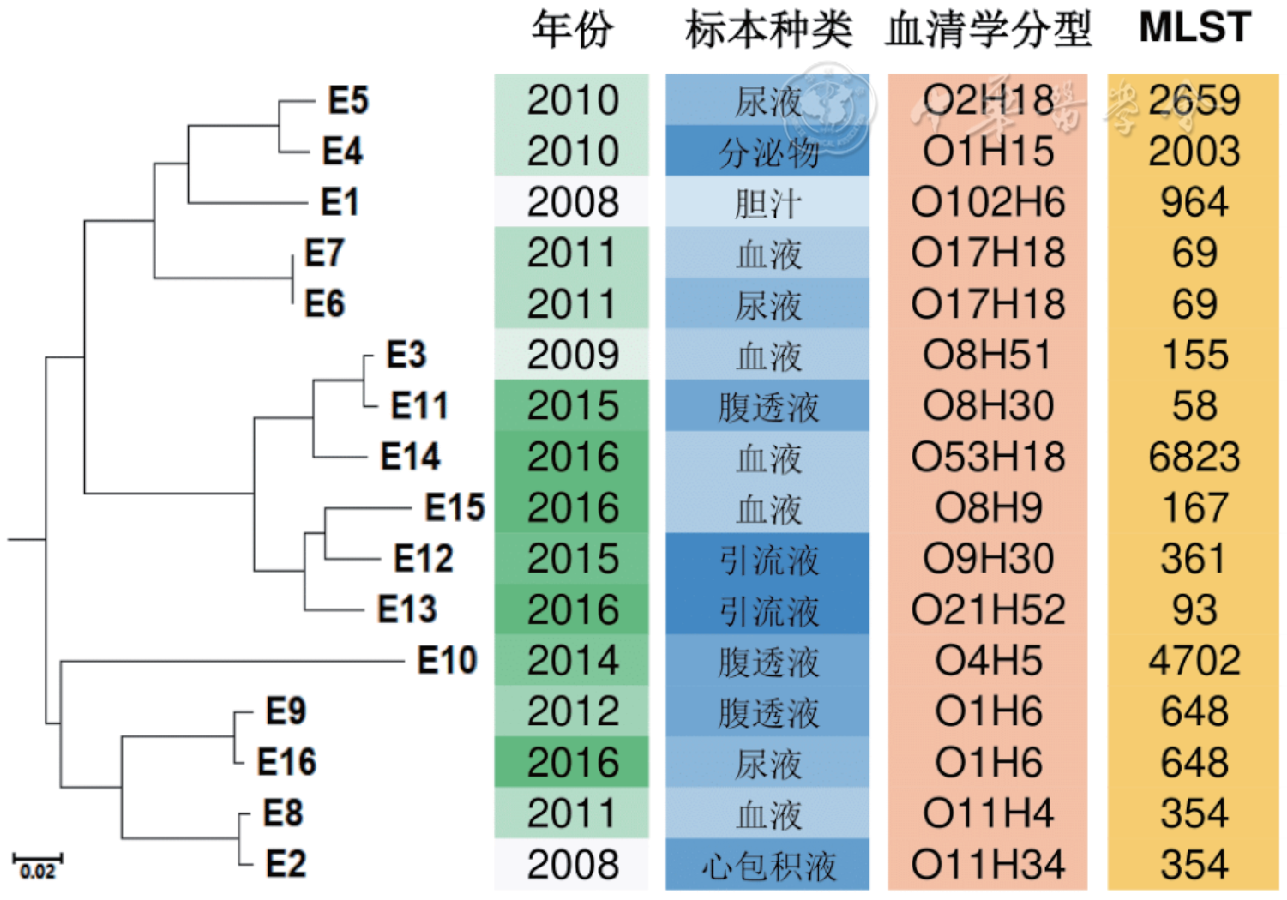
基于SNP分析在进行进化树构建之前,引入7株大肠埃希菌株为参考,对23株菌进行SNP检测并构建进化树。结果发现7株参考菌株散在分布在环形进化树图上,16株CR-ECO与7株参考菌株分别聚类到不同的分支上,其中E.coli.UMN026与E6、E7聚类到同一分支上,进化关系最为接近;E15与E.coli.K12.MG1655进化关系较近,其余菌株的进化关系详见

WGS技术已经开始作为一种常见的分子生物学技术应用于临床微生物研究当中。在临床微生物实验室中分离的各类多重耐药及泛耐药菌株,通过WGS可以快速获得丰富的分子生物学及分子流行病学信息,如血清学分型,MLST,耐药基因及毒力因子等等,而在过去这些信息需要通过繁琐冗长的实验设计才能获得。本研究通过对16株CR-ECO进行WGS分析,检测出13株为产碳青霉烯酶型大肠埃希菌,产酶类型均属于MBL,包括IMP型(6/13)及NDM型(7/13),这与其他人报道的数据不一致。陈韩等[3]的研究发现产碳青霉烯酶大肠埃希菌的主要耐药机制为产KPC-2型和NDM-5型。Zhang等[4]统计的中国14个省市25家医院的产碳青霉烯酶大肠埃希菌的产酶类型为KPC型及NDM型,且以NDM-5型为主。Mahalingam等[5]在印度南部的医院分离的产碳青霉烯酶大肠埃希菌以NDM型及OXA-181型为主。Dagher等[6]公布的数据显示黎巴嫩三级医院的产碳青霉烯酶大肠埃希菌为OXA-48型和OXA-181型。从历年中国检出CR-ECO变迁水平来看,CR-ECO检出率在1.5%[7]左右波动,而我院CR-ECO的检出率一直处于较低水平,平均为0.51%,低于全国检出率。可见由于地域性及医院感染防控力度的差异,不同地区及医院的CR-ECO检出率及耐药相关信息或有不同,了解CR-ECO的具体耐药机制可为临床用药及院感防控提供依据。
另外在这16株CR-ECO中均检测到产AmpC酶的耐药基因CMY型。CMY型AmpC酶虽说不能直接水解碳青霉烯类,但是在高水平表达及合并膜孔蛋白缺失的情况下,可以在周质中以共价结合的形式阻止碳青霉烯类药物到达靶点发挥作用。CMY-2分布广泛,目前被认为是世界上最流行的质粒介导的AmpC酶[8]。在本研究中以CMY-47为主(13/16),CMY-2仅有2株(2/16)。另外研究中超过一半的菌株(10/16)同时含有CTX-M耐药基因。MBL一般被认为可以水解除氨曲南以外的所有β内酰胺类药物。本研究中氨曲南耐药的菌株有11株(11/16),结合本研究的耐药基因检测结果,推测可能因为ESBL耐药基因和(或)AmpC酶耐药基因的表达,导致这些菌株对氨曲南产生耐药。在16株CR-ECO表型确认实验中,有3株菌株检测结果为mCIM阴性、eCIM阴性,菌株号分别为E1、E2、E8;在后续WGS数据显示E1、E2、E8菌株没有发现携带碳青霉烯酶耐药基因,两者结果证明该表型确认与基因检测符合度为100%。但E1同时携带ESBL基因、 AmpC酶基因和外排泵基因,且存在OmpC膜孔蛋白基因缺失,E2和E8则同时携带AmpC酶基因和外排泵基因,且存在OmpC膜孔蛋白基因缺失,这可能是这3株菌耐碳青霉烯类药物的原因。
利用WGS除了可以发现产碳青霉烯酶、β内酰胺酶及AmpC酶的耐药基因以外,亦可以筛选其他种类抗菌药物的耐药基因,如氟喹诺酮类、氨基糖苷类、四环素类、多黏菌素类等。通过WGS可快速了解菌株在基因水平上的耐药全貌,这是通过常规分子生物学方法不能实现的。
细菌外排作用也是细菌耐药的重要机制之一,从底物特异性上而言,外排泵一般可以分为特异性外排泵及多重耐药外排泵两种,本研究中的tet34、tetG编码的外排泵对四环素有特异性的外排作用,qepA也被认为是一种由质粒介导能引起大肠埃希菌对氟喹诺酮类药物特异性外排的基因[9]。而QacE可对季胺类化合物外排,IceT是一种可对柠檬酸根离子化合物产生特异性外排作用的内膜蛋白。属于RND类的外排泵AcrD主要可排出细胞内的氨基糖苷类药物。对于多重耐药外排泵系统,如AcrAB-TolC这种RND/MFP/OMP三方结构的外排泵系统已经因为对β内酰胺类、氯霉素、溴化乙锭、氟喹诺酮、大环内酯类、新霉素和利福平等抗菌药物的多重耐药被业界熟知[10]。外排泵系统除了因外排抗菌药物导致细菌耐药以外,还可能在细菌感染、定植或毒力产生中发挥重要作用[11]。本研究中的16株CR-ECO经过WGS已筛选出相关外排泵基因,以此为基础,通过逆转录PCR法检测相关基因的mRNA表达水平,再结合药敏试验结果可进一步揭示相关外排泵在多重耐药形成中起到的关键作用,这为外排泵的研究提供一种新思路。
此外,利用WGS所得序列筛选出可靠的SNP,SNP可以反映细菌之间的微小差异,利用它构建高质量进化分析树,可以进行更加准确的谱系发育、同源性研究分析。本研究在选取参考序列构建进化发育树时,由于菌株年限跨度久远且没有出现医院暴发流行,所以为了更加清楚地了解进化关系选用了7株GenBank中的大肠埃希菌作为参考菌株。近来研究发现WGS可作为一种追踪感染疾病暴发的新型手段,脉冲场凝胶电泳(pulsed field gel electrophoresis, PFGE)在过去20年被认为是分析细菌相关性的金标准方法,而目前认为WGS比PFGE有着更高的准确性[12]。
本研究除了耐药基因以外,利用相关软件(包括简便的线上工具如CGE等)分析WGS数据,可得到血清学分型、MLST等相关信息。16株CR-ECO的MLST结果多元化,其中ST648、ST2003、ST167、ST354分型的CR-ECO已被报道引起各类感染[3, 6]。
此次回顾性研究利用WGS分析了深圳市人民医院2008—2016年CR-ECO的耐药机制及分子流行病学特征。目前WGS因其高效、成本可控的优势已经快速在临床及科学研究中占领市场[13]。在微生物领域,WGS作为一种研究病原菌相关分子生物学特征的新技术,使得微生物研究对象由少量基因及其功能转变为病原菌的全基因组结构及相关基因功能。当然该技术目前也存在一些缺陷,如测序前样本的处理要求高,培养、提取菌株DNA耗时长;菌株基因型与相关表型的对应关系研究不足等;且缺乏统一、快速、有效及大容量的生物信息学数据处理分析系统更是阻碍这一技术在全球应用的主要原因[14]。但是相信在不久的将来,这一瓶颈将会被突破,使得WGS技术在微生物领域得到更加广泛的应用。
1
2
3
4
5
6
7
8
9
10
11
12
13
14
