肌张力障碍诊断中国专家共识
2020年1月
中华神经科杂志,第53卷第1期 第8页-第12页
1911年Oppenheimsh首次提出变形性肌张力障碍一词,描述具有异常运动、姿势扭转及肌张力波动变化的一种疾病[1]。1984年国际肌张力障碍医学研究基金会顾问委员会提出了肌张力障碍的定义:一种不自主、持续性肌肉收缩引起的扭曲、重复运动或姿势异常的综合征[2]。这个定义在相当长的时间里被临床医生和相关领域的研究者普遍接受并采用。2008年中华医学会神经病学分会帕金森病及运动障碍学组制定了我国首个肌张力障碍诊断和治疗指南,对于肌张力障碍领域的规范诊断和治疗发挥了积极的作用[3]。
近10年来,国内外在肌张力障碍领域的研究非常活跃,特别是在遗传学方面取得重大进展[4,5],以脑深部电刺激为代表的治疗方法在疑难病例的治疗上获得突破[6,7],对于肌张力障碍的定义、分类、诊断、评价等方面也有了新的认识,因此在总结国内外最新研究成果的基础上,结合专家组的临床经验,制定了《肌张力障碍诊断中国专家共识》。
肌张力障碍是一种运动障碍,其特征是持续性或间歇性肌肉收缩引起的异常运动和(或)姿势,常重复出现。肌张力障碍性运动一般为模式化的扭曲动作,可以呈震颤样。肌张力障碍常因随意动作诱发或加重,伴有肌肉兴奋的泛化[8]。"肌张力障碍"可用于描述一种具有独特表现的不自主运动,与震颤、舞蹈、抽动、肌阵挛等类同;也可用于命名一种独立的疾病或综合征,其中肌张力障碍症状是唯一或主要的临床表现,肌张力障碍是神经系统运动增多类疾病的常见类型。
肌张力障碍作为不自主运动的一种形式,常可以观察到以下现象[9]。
用于纠正异常姿势或缓解肌张力障碍性运动的随意动作,通常是涉及受累部位的简单运动,而不是用力对抗肌张力障碍症状。
一种对侧运动诱发的单侧肢体的姿势或运动,与肌张力障碍的特征相同或类似,常见于受累较严重的一侧肢体。
常在肌张力障碍性运动的高峰出现,在邻近的身体区域较正常运动范围扩大的肌肉兴奋。
仅在特定活动或执行特定任务时出现肌张力障碍,例如某些职业(如书写痉挛、音乐家痉挛)或运动,以局灶型肌张力障碍多见。
异常的肌张力障碍性姿势在不刻意纠正下充分展现的身体位置,此处肌张力障碍性运动往往减轻。
一种自发的振荡性、节律性运动,常不恒定,由肌张力障碍性肌肉收缩导致,试图维持正常姿势时常加重。在"零点"时,肌张力障碍性震颤往往减轻。肌张力障碍性震颤有时可能需要与原发性震颤相鉴别。
肌张力障碍多以异常的表情姿势和不自主的变换动作而引人注目。肌张力障碍所累及肌肉的范围和肌肉收缩强度变化很大,因而临床表现各异。但某些临床特点有助于肌张力障碍与其他形式的运动障碍相鉴别,主要有以下几点。
1.肌张力障碍时不自主动作的速度可快可慢,可以不规则或有节律,但在收缩的顶峰状态有短时持续,呈现为一种奇异动作或特殊姿势。
2.不自主动作易累及头颈部肌肉(如眼轮匝肌、口轮匝肌、胸锁乳突肌、头颈夹肌等)、躯干肌、肢体的旋前肌、指腕屈肌、趾伸肌和跖屈肌等。
3.发作的间歇时间不定,但异常运动的方向及模式几乎不变,受累的肌群较为恒定,肌力不受影响。
4.不自主动作在随意运动时加重,在休息睡眠时减轻或消失,可呈现进行性加重,疾病晚期时症状持续、受累肌群广泛,可呈固定扭曲痉挛畸形。
5.症状常因精神紧张、生气、疲劳而加重。
肌张力障碍依据临床特征和病因两条主线进行分类[8]。
临床特征的分类依据包括发病年龄、症状分布、时间模式、伴随症状等。
(1)婴幼儿期(出生至2岁);(2)儿童期(3~12岁);(3)青少年期(13~20岁);(4)成年早期(21~40岁);(5)成年晚期(>40岁)。
(1)局灶型:只有一个身体区域受累,如眼睑痉挛、口下颌肌张力障碍、颈部肌张力障碍、喉部肌张力障碍和书写痉挛。(2)节段型:2个或2个以上相邻的身体区域受累,如颅段肌张力障碍、双上肢肌张力障碍。(3)多灶型:2个不相邻或2个以上(相邻或不相邻)的身体区域受累。(4)全身型:躯干和至少2个其他部位受累。(5)偏身型:半侧身体受累,常为对侧半球,特别是基底节损害所致。
包括疾病进程和变异性:(1)疾病进程:①稳定型;②进展型。(2)变异性:①持续型:肌张力障碍几乎以同等程度持续存在;②动作特异型:肌张力障碍只在特定的活动或任务中出现;③日间波动型:肌张力障碍的持续时间、严重程度和临床表现在1 d中具有波动性变化;④发作性:突然出现的肌张力障碍动作,通常由某种因素诱发,往往自发缓解。
发作性肌张力障碍依据诱发因素的不同分为3种主要形式:(1)发作性运动诱发的运动障碍,由突然的动作诱发;(2)发作性过度运动诱发的运动障碍,由跑步、游泳等持续运动诱发;(3)发作性非运动诱发的运动障碍,可因饮用酒、茶、咖啡或饥饿、疲劳、情绪波动等诱发。
(1)单纯型:肌张力障碍是唯一的运动症状,可伴有肌张力障碍性震颤;(2)复合型:肌张力障碍合并其他运动障碍,如肌阵挛或帕金森综合征;(3)复杂型:肌张力障碍合并其他神经系统或全身系统疾病表现。
组织病理、结构影像和遗传学研究是判断肌张力障碍病因的重要手段,可以相互补充。
(1)有神经退行性病变证据:如神经元缺失;(2)有结构性病变证据:如非进展性神经发育异常或获得性病变;(3)无神经退行性病变或结构性病变证据。
(1)遗传性:已明确致病基因:①常染色体显性遗传;②常染色体隐性遗传;③X连锁隐性遗传;④线粒体遗传。(2)获得性:已明确致病原因:①围产期脑损伤;②感染:病毒性脑炎、昏睡性脑炎、亚急性硬化性全脑炎、HIV感染、其他(结核、梅毒等);③药物:左旋多巴、多巴胺受体激动剂、神经安定类药物(多巴胺受体阻断剂)、抗惊厥药、钙拮抗剂;④中毒:锰、钴、氰化物、甲醇等;⑤血管病:梗死、出血、动静脉畸形(包括动脉瘤);⑥肿瘤:脑肿瘤、副肿瘤性脑炎;⑦脑损伤:外伤、手术、电击伤;⑧免疫:系统性免疫病、自身免疫性脑炎;⑨功能性。(3)特发性:在限定时间和条件下,尚无遗传性和获得性病因证据:①散发性;②家族性。
肌张力障碍的诊断可分为3步:(1)明确不自主运动是否为肌张力障碍性运动;(2)明确肌张力障碍是否为获得性;(3)明确肌张力障碍是遗传性或特发性(
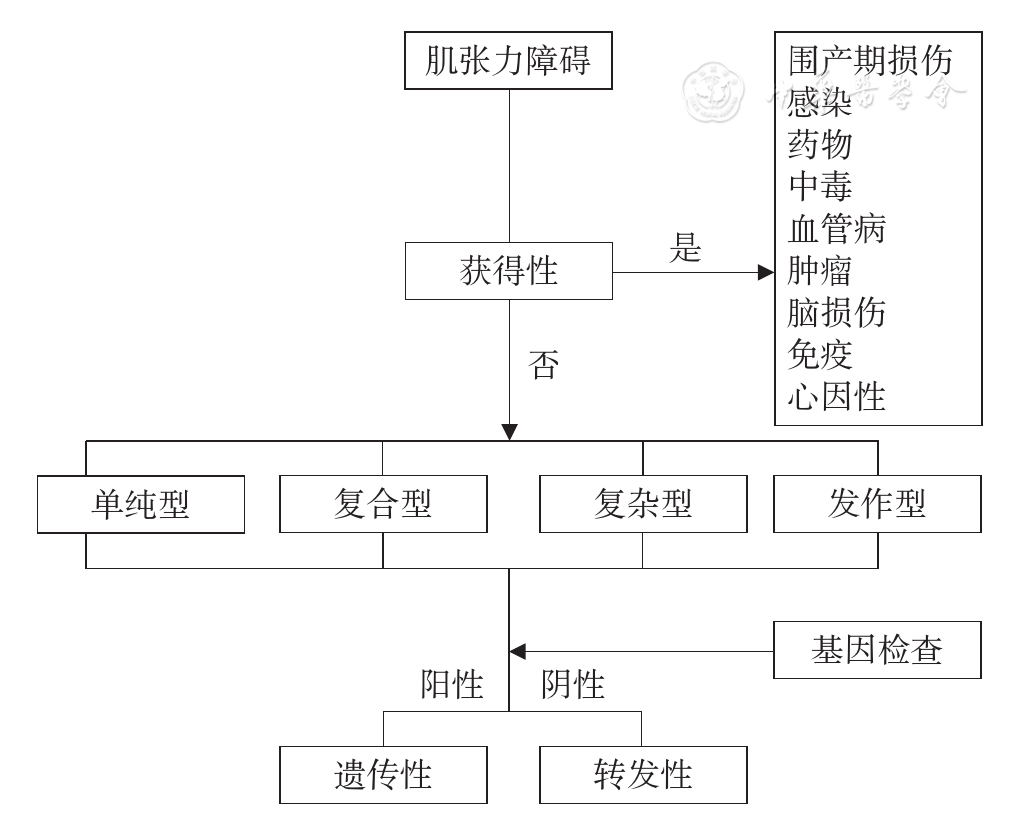
眼部感染、干眼症和眼睑下垂应与眼睑痉挛鉴别;牙关紧闭或颞下颌关节病变应与口-下颌肌张力障碍鉴别;颈椎骨关节畸形,外伤、疼痛、感染或眩晕所致强迫头位,先天性肌性斜颈或第Ⅳ脑神经麻痹形成的代偿性姿势等应与颈部肌张力障碍鉴别;掌腱膜挛缩、扳机指、低钙血症等应与手部肌张力障碍鉴别。其他需鉴别的还有脊柱侧弯、僵人综合征、后颅窝肿瘤、脊髓空洞症、裂孔疝-斜颈综合征(Sandifer综合征)、Satoyoshi综合征、神经肌肉病等表现的异常姿势或动作。
以下临床线索往往提示获得性肌张力障碍:(1)起病突然,病程早期进展迅速;(2)持续性偏身型肌张力障碍;(3)儿童期颅段起病;(4)成人起病的下肢或全身型肌张力障碍;(5)早期出现固定的姿势异常;(6)除肌张力障碍外存在其他神经系统体征;(7)早期出现语言功能障碍,如构音障碍、口吃;(8)混和性运动障碍伴神经系统异常,如痴呆、癫痫、视觉障碍、共济失调、肌无力、肌萎缩、反射消失、感觉缺失、自主神经功能障碍。
功能性肌张力障碍是功能性运动障碍的一种形式,诊断线索包括常与感觉不适同时出现、缺乏感觉诡计和动作特异性、假性无力、假性感觉症状、多重的躯体症状、自我伤害、古怪的运动或假性发作、明显的精神疾病、无人观察时好转、暗示下急性加重和应用心理治疗、强烈暗示、安慰剂或物理治疗可好转甚至痊愈。
基因诊断方面,遗传性肌张力障碍基因检测的策略为:首先考虑主要症状特征,其次考虑起病年龄和遗传方式等因素,综合考虑筛选候选基因进行检测,并针对候选致病基因选取相应的检测技术,必要时可选择新一代高通量测序技术[10,11,12,13]。
对于单纯型肌张力障碍,当以全身型表现为主时,应考虑DYT-TOR1A、DYT-THAP1、DYT-HPCA、DYT-TUBB4等亚型,尤其对于起病年龄小于26岁或者有早发患病亲属的患者,应首选检测TOR1A基因[14],其次检测THAP基因,之后可结合具体遗传方式和临床特点进行相应基因的检测。而当以局灶型和节段型表现为主时,尤其是颅颈段受累明显时,应考虑DYT-GNAL、DYT-ANO3、DYT-COL6A3等亚型,并优先检测GNAL基因。
对于复合型肌张力障碍,应对早发、诊断不明的患者优先考虑DYT-GCH1、DYT-TH等亚型,并进行基因诊断。当持续性肌张力障碍主要伴随肌阵挛表现时,应考虑DYT-SGCE、DYT-CACNA1B、DYT-KCTD17等亚型;进行基因诊断时,应首选检测SGCE基因,其次需结合具体遗传方式和临床特点进行相应基因的检测。而当以伴随帕金森综合征表现为主时,应考虑DYT-TAF1、DYT-ATP1A3、DYT-PRKRA、DYT-GCH1、DYT-TH等亚型,但值得注意的是,PARK-Parkin PARK-PINK1、PARK-DJ1亚型也常出现类似表现。
对于发作性肌张力障碍,根据诱发因素的不同,应选择检测相应的基因。如以随意运动为主要诱发因素,则首选PRRT2基因进行检测,其次检测SLC2A1、MR-1基因;如无明显随意运动诱发,则首先检测MR-1基因,其次检测PRRT2、SLC2A1、KCNMA1基因;如以持续运动为主要诱发因素,则首先检测SLC2A1基因,其次检测PRRT2、MR-1基因。
此外,当患者的临床特点提示神经变性、遗传代谢等相关的复杂型肌张力障碍时,需完善相关疾病的致病基因的检测。随着二代测序技术不断进步,系统的致病基因检测成本显著降低,在遗传因素筛查上越来越具有优势。推荐结合患者的实际情况,选择性价比高的基因检测手段。
对于某些仅凭临床特征不足以诊断的病例,应用神经生理检测手段进行观察、分析是辅助诊断的有利工具[8]。
1.筛查或排除获得性肌张力障碍需行脑影像学检查[15,16],特别是当肌张力障碍症状累及较为广泛的儿童或青少年患者。
2.除非怀疑脑钙化,头颅MRI检查对肌张力障碍的诊断价值要优于脑CT。磁敏感加权成像(susceptibility weighted imaging,SWI)或T2*对于脑组织铁沉积神经变性病的诊断价值优于常规MRI[17]。
3.目前没有证据显示更复杂、高超的影像学技术,包括脑容量形态测量(voxel based morphometry)、弥散加权成像(diffusion weighted imaging)、功能磁共振(functional MRI)对肌张力障碍的诊断或分类具有任何价值。但MRI中的一些特殊序列如SWI或T2*、弥散张量成像(diffusion tensor imaging)等可能有助于脑深部电刺激中靶点定位。
可以采用量表或问卷对肌张力障碍进行评价,对量表及问卷的推荐如

[1] Oppenheim H. About a rare spasm disease of childhood and young age (dysbasia lordotica progressiva, dystonia musculorum deformans)[J]. Neurologische Centralblatt, 1911,30: 1090-1107.
[2] Fahn S. Concept and classification of dystonia[J]. Adv Neurol, 1988, 50: 1-8.
[3] 中华医学会神经病学分会帕金森病及运动障碍学组.肌张力障碍诊断与治疗指南[J].中华神经科杂志, 2008, 41(8): 570-573.
[4] 马俊,王琳,万新华.肌张力障碍基于临床特征分类的遗传学进展[J].中华神经科杂志, 2018, 51(10): 839-845.
[5] Ma J, Wang L, Yang YM, et al. Targeted gene capture sequencing in diagnosis of dystonia patients[J]. J Neurol Sci, 2018, 390: 36-41.
[6] Kupsch A, Benecke R, Müller J, et al. Pallidal deep-brain stimulation in primary generalized or segmental dystonia[J]. N Engl J Med, 2006, 355(19): 1978-1990.
[7] Volkmann J, Mueller J, Deuschl G, et al. Pallidal neurostimulation in patients with medication-refractory cervical dystonia: a randomised, sham-controlled trial[J]. Lancet Neurol, 2014, 13(9): 875-884.
[8] Albanese A, Bhatia K, Bressman SB, et al. Phenomenology and classification of dystonia: a consensus update[J]. Mov Disord, 2013, 28(7): 863-873.
[9] Albanese A, Di Giovanni M, Lalli S. Dystonia: diagnosis and management[J]. Eur J Neurol, 2019, 26(1): 5-17.
[10] Müller U. The monogenic primary dystonias[J]. Brain, 2009, 132(
[11] Klein C. Genetics in dystonia[J]. Parkinsonism Relat Disord, 2014, 20
[12] Lohmann K, Klein C. Update on the Genetics of Dystonia[J]. Curr Neurol Neurosci Rep, 2017, 17(3): 26.
[13] 王琳,万新华,成伏波,等. DYT6型肌张力障碍患者的临床表现和影像学特点[J].中华神经科杂志, 2013, 46(3): 148-152.
[14] Klein C, Friedman J, Bressman S, et al. Genetic testing for early-onset torsion dystonia (DYT1): introduction of a simple screening method, experiences from testing of a large patient cohort, and ethical aspects[J]. Genet Test, 1999, 3(4): 323-328.
[15] Albanese A, Barnes MP, Bhatia KP, et al. A systematic review on the diagnosis and treatment of primary (idiopathic) dystonia and dystonia plus syndromes: report of an EFNS/MDS-ES Task Force[J]. Eur J Neurol, 2006, 13(5): 433-444.
[16] Albanese A, Asmus F, Bhatia KP, et al. EFNS guidelines on diagnosis and treatment of primary dystonias[J]. Eur J Neurol, 2011, 18(1): 5-18.
[17] 中华医学会神经病学分会帕金森病及运动障碍学组,中国医师协会神经内科医师分会帕金森病及运动障碍专业委员会.脑组织铁沉积神经变性病诊治专家共识[J].中华医学杂志, 2016, 96(27): 2126-2133.
[18] Albanese A, Sorbo FD, Comella C, et al. Dystonia rating scales: critique and recommendations[J]. Mov Disord, 2013, 28(7): 874-883.
