胰高糖素样肽-1对非酒精性脂肪肝病状态下生长分化因子15表达的影响
中华糖尿病杂志,第13卷第5期 第482页-第489页
甘露,林倍思,苏燕娜,陈亚兰,许雯,杨黛稚,梁华,徐芬,严晋华
非酒精性脂肪肝病(non-alcoholic fatty liver disease,NAFLD)影响着全球1/4的人口,在我国患病率高达29.6%,目前尚无明确批准的治疗药物[1, 2, 3]。胰高糖素样肽-1(glucagon-like peptide-1,GLP-1)受体激动剂或类似物是已在临床广泛使用的降糖药,具有减重、降糖等多重作用机制[4, 5]。生长分化因子15(growth differentiation factor 15,GDF15)是功能多样的转化生长因子β超家族的非典型成员之一[6, 7]。通常情况下,GDF15蛋白以35 kDa全长形式合成,在N末端被切割后,成熟蛋白质以25 kDa二硫键连接的二聚体形式分泌至外周血[8]。研究表明,GDF15表达水平与NAFLD的发生发展密切相关[9, 10],GDF15可作为NAFLD的生物标志物[11]。既往的临床和基础研究发现,GLP-1可改善NAFLD的肝脏脂质沉积[12, 13, 14, 15, 16]。GDF15是否参与了GLP-1改善NAFLD肝脏脂质沉积的作用值得进一步研究。本研究中我们旨在探讨GLP-1对NAFLD状态下GDF15表达与分泌的影响。
人群数据来自前期LIGHT-ON研究[13],对NAFLD合并2型糖尿病(type 2 diabetes mellitus,T2DM)患者分别给予利拉鲁肽(Novo Nordisk,丹麦,简称GLP-1组)、西格列汀或甘精胰岛素治疗26周,在治疗前后收集患者的临床资料,包括性别、年龄、体重、体重指数(body mass index,BMI)等,通过酶联免疫吸附法测定血清GDF15水平,磁共振成像-质子密度脂肪含量检测肝内脂肪含量(intrahepatic lipid,IHL)。西格列汀用量为100 mg/d,利拉鲁肽和甘精胰岛素起始及加量方法详见文献[13],26周时利拉鲁肽组和甘精胰岛素组的用量分别为(1.7±0.3)mg、(21.7±9.5)U/d。研究方案经中山大学附属第三医院伦理委员会批准,批准文号为中大附三医伦[2013]2-116(补)1号,所有患者均签署知情同意书。
1.小鼠模型与实验分组:8周龄雄性C57BL/6小鼠(南京动物模式研究所提供)根据体重按随机数字表法分为正常饮食对照组和高脂饮食(high fat diet,HFD)组(各6只),分别给予普通饲料(59%碳水化合物、13%脂肪和28%蛋白质)和高脂饲料(26%碳水化合物、35%脂肪和26%蛋白质,美国Research Diets,D12492)喂养12周。12周后HFD组分别予腹腔注射艾塞那肽(24 nmol·kg??·d??,美国,Lilly)(简称GLP-1组,6只)或生理盐水8周,正常饮食组予腹腔注射等量生理盐水作为对照[15,17]。干预结束后小鼠行麻醉后处死,留取肝脏组织标本,将其分成2份,置于4%多聚甲醛中固定后包埋,行石蜡组织切片,或经液氮快速冷冻后于-80 ℃冰箱保存。以上实验经中山大学实验动物伦理委员会批准,批文号SYSU-IACUC-2018-000234号。
2.细胞模型与干预方法:人HepG2细胞株从中国科学院干细胞库购买。予10%胎牛血清、100 U/ml青链霉素的DMEM培养基培养HepG2细胞。
干预前对HepG2细胞予无血清培养基饥饿4 h。用10%脱脂牛血清白蛋白(bovine serum albumin,BSA)、300 μmol/L棕榈酸钠(sodium palmitate,PA)以及300 μmol/L PA+100 nmol/L Exendin-4(简称GLP-1组)干预HepG2细胞,分别于0、3、6 h检测GDF15 mRNA水平。对HepG2细胞分别予10% BSA、300 μmol/L PA、300 μmol/L PA+1 nmol/L GLP-1、300 μmol/L PA+20 nmol/L GLP-1或300 μmol/L PA+100 nmol/L GLP-1干预6 h,检测GDF15 mRNA水平及细胞上清中GDF15蛋白含量。用10% BSA、10% BSA+100 nmol/L GLP-1、300 μmol/L PA以及300 μmol/L PA+100 nmol/L GLP-1干预HepG2细胞,在6 h检测GDF15 mRNA水平及细胞上清GDF15蛋白含量,并采用油红O染色评估细胞脂质沉积,及GPO-Tinder酶法试剂盒测定HepG2细胞甘油三酯(triglyceride,TG)水平。
利用CRISPR/Cas9基因编辑技术,使用插入sgRNA片段的lentiCRISPRv2载体在HepG2细胞中靶向敲除GDF15基因。空白lentiCRISPRv2载体作为阴性对照。转染后24 h加入嘌呤霉素(1 μg/ml)以筛选稳定敲除GDF15基因的细胞和阴性对照细胞。1周后收集细胞及细胞上清,检测细胞上清GDF15蛋白的分泌水平。分别予以10% BSA、10% BSA+100 nmol/L GLP-1、300 μmol/L PA以及300 μmol/L PA+100 nmol/L GLP-1干预转染的HepG2细胞6 h。使用上述方法测定细胞的TG水平。
3.油红O染色及定量分析:用3 mg/ml的油红工作液对小鼠肝脏组织冰冻切片或4%多聚甲醛固定后的HepG2细胞避光室温染色1 h,60%异丙醇漂洗至间质清晰后用磷酸盐缓冲液缓慢冲洗,10%甘油封片,封片后用显微镜观察并采集图像。采集图像后,加入无水异丙醇至染色后的细胞,室温摇匀5 min。吸取200 μl至96孔板,酶标仪检测492 nm波长处吸光度(A值)。
4.免疫荧光:石蜡切片脱蜡后用BSA孵育30 min,封闭后加一抗。切片平放于湿盒内于4 ℃孵育过夜。用磷酸盐缓冲液清洗3遍,使用对应的二抗避光室温孵育50 min,缓慢清洗3遍后滴加DAPI染液室温孵育10 min染核,再次清洗3遍后用抗荧光淬灭封片剂封片。切片于荧光显微镜下观察并采集图像。
5.实时定量逆转录聚合酶链反应:用TRIzol法提取肝脏组织或HepG2细胞总RNA。使用逆转录试剂盒将RNA逆转录为cDNA。扩增体系:SYBR Green 5.0 μl,上下游引物各0.5 μl,cDNA 1.0 μl,无酶水3.0 μl,总体积10.0 μl。用Ct(2-ΔΔCt)比较法计算目的基因的转录水平。
DMEM培养基、胎牛血清、青链霉素、0.25%胰酶(Gibco,美国);GDF15酶联免疫吸附法测定试剂盒(R&D,美国);组织细胞甘油三酯酶法测定试剂盒(普利莱,中国);逆转录试剂盒、SYBR Green荧光定量PCR试剂(Roche,瑞士);艾塞那肽(Lilly,美国);lentiCRISPRv2(Addgene,美国,52961);10%脱脂BSA(Millipore,美国,126575);Exendin-4、棕榈酸钠、油红O、嘌呤霉素、TRIzol(Sigma,美国);F4/80抗体,荧光二抗CY3标记,抗荧光淬灭封片剂(赛维尔生物,中国)。
所有数据采用SPSS 23.0软件进行统计学分析,采用GraphPad Prism 8绘制统计图。正态分布的连续变量使用
25例NAFLD合并T2DM患者被纳入分析,其中GLP-1组9例(男4例、女5例)、西格列汀组8例(男4例、女4例)、甘精胰岛素组8例(男6例、女2例)。糖尿病病程分别为(4.0±4.8)、(4.9±3.2)和(5.1±3.6)年,患者年龄分别为(43.7±10.5)、(55.1±10.5)和(48.0±8.7)岁。3组患者的性别分布、糖尿病病程和年龄差异均无统计学意义(P值分别为0.479、0.081和0.818)。
各组间治疗前的糖尿病病程、体重、BMI、糖化血红蛋白(glycated hemoglobin A1c,HbA1c)、血脂、IHL及血清GDF15水平等差异均无统计学意义(

与正常对照相比,HFD组小鼠肝脏组织GDF15 mRNA表达明显上调(P<0.05)。GLP-1干预后,小鼠肝脏GDF15 mRNA表达水平较HFD组进一步升高(P<0.05)(
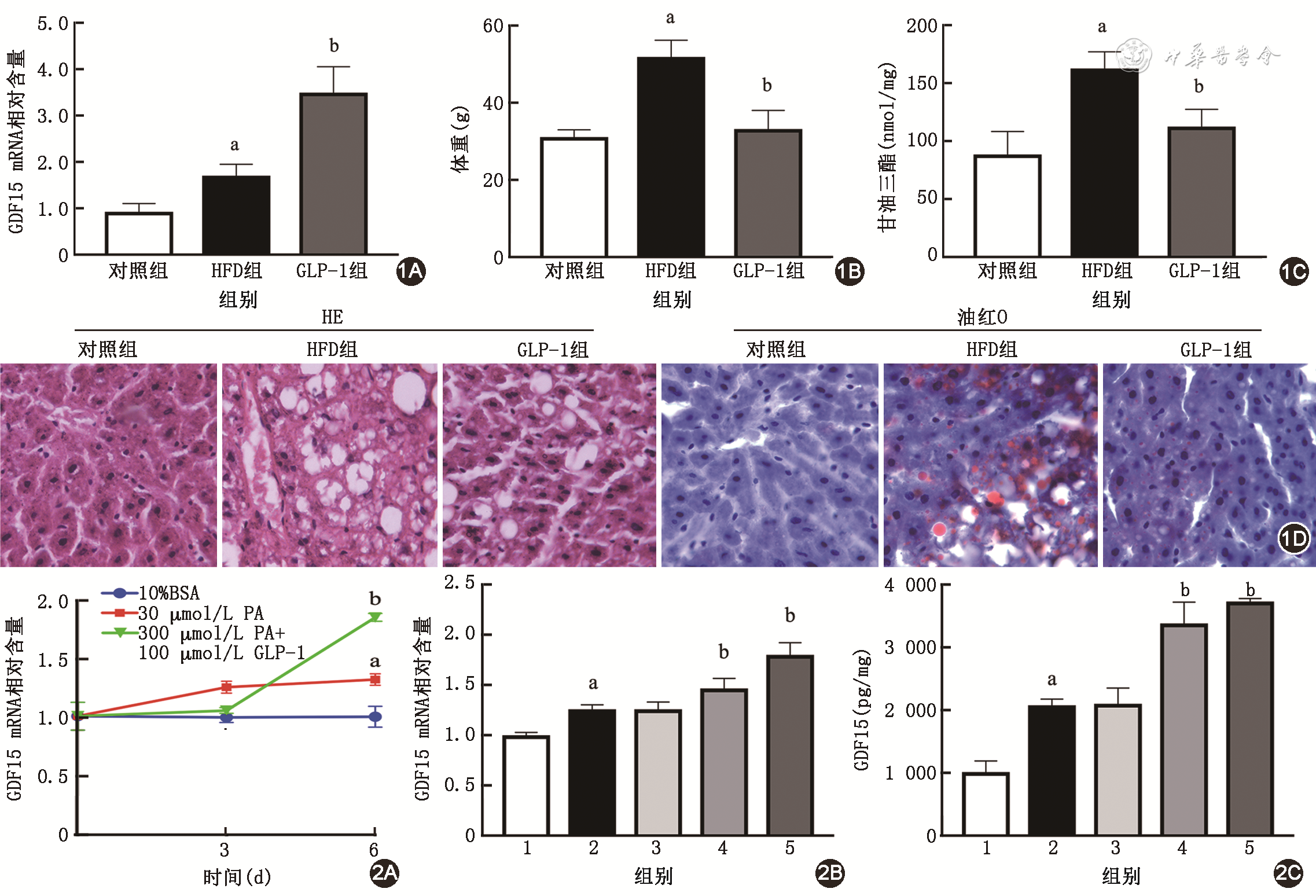
给予高脂饮食喂养12周时,小鼠血糖[分别为(10.4±1.3)和(7.1±1.1)mmol/L]、体重[(42.1±3.2)和(28.9±1.9)g]与正常对照相比明显升高,差异均有统计学意义(P均<0.05)。GLP-1干预8周后,与HFD组小鼠相比,GLP-1组小鼠血糖[(8.0±0.9)和(10.6±0.9)mmol/L,P<0.05]、体重、肝脏TG明显降低(P均<0.05)(
1.GLP-1时间依赖性促进GDF15的表达:与对照组相比,PA诱导HepG2细胞的GDF15 mRNA表达水平在6 h上调差异有统计学意义。GLP-1干预后,HepG2细胞的GDF15 mRNA表达水平呈时间依赖性升高,并在6 h较PA组差异有统计学意义(P均<0.05)(
2.GLP-1剂量依赖性促进GDF15的表达与分泌:与PA组相比,HepG2细胞在GLP-1干预后胞内GDF15 mRNA表达水平及上清GDF15蛋白含量呈剂量依赖性升高(P均<0.05)(
3.GLP-1仅在病理状态下促进GDF15的表达与分泌并改善HepG2细胞脂质沉积:与BSA对照组相比,GLP-1对生理状态下的HepG2细胞中GDF15的表达与分泌的影响差异无统计学意义。而在PA诱导的HepG2细胞中,GLP-1明显促进HepG2细胞GDF15的表达与分泌(P均<0.05)(
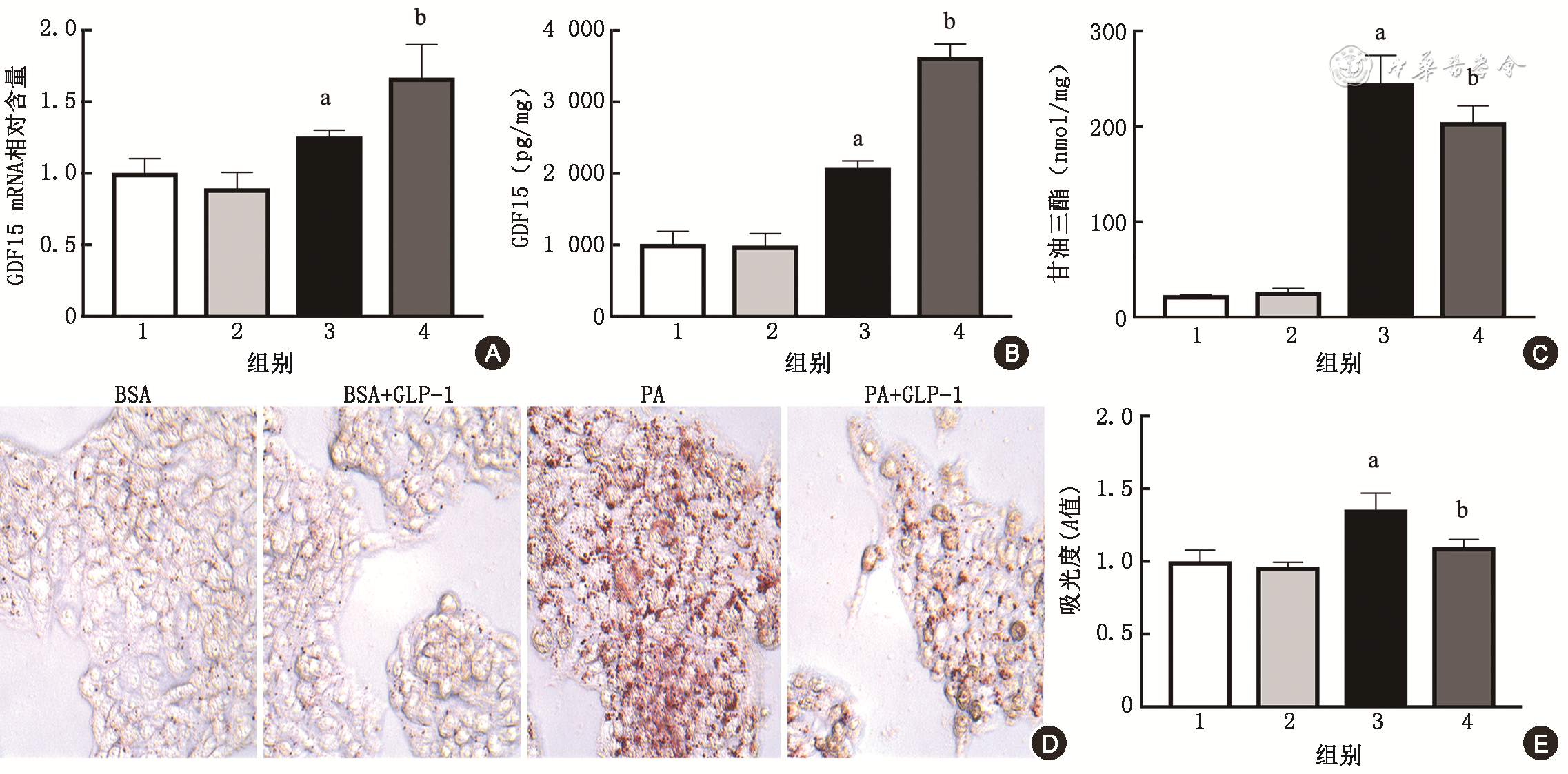
注:GLP-1为胰高糖素样肽-1;GDF15为生长分化因子15;10%脱脂牛血清白蛋白(BSA)为对照组;300 μmol/L PA为棕榈酸钠(PA)干预组;1为10%BSA组;2为10%BSA+100 nmol/L GLP-1组;3为300 μmol/L PA组;4为300 μmol/L PA+100 nmol/L GLP-1组;与对照组比较,aP<0.05;与PA干预组比较,bP<0.05
与正常对照组相比,HFD组小鼠肝脏组织炎症相关基因F4/80、肿瘤坏死因子(tumor necrosis factor,TNF)-α mRNA表达水平显著上调(P均<0.05),而过氧化物酶体增殖物激活受体γ共激活因子(peroxisome proliferator-activated receptor γ coactivator,PGC)1α mRNA表达明显下调(P<0.05)。与HFD组相比,GLP-1组炎症相关基因mRNA表达显著下调(P均<0.05),而促进糖脂代谢相关基因mRNA表达上调(P均<0.05)(
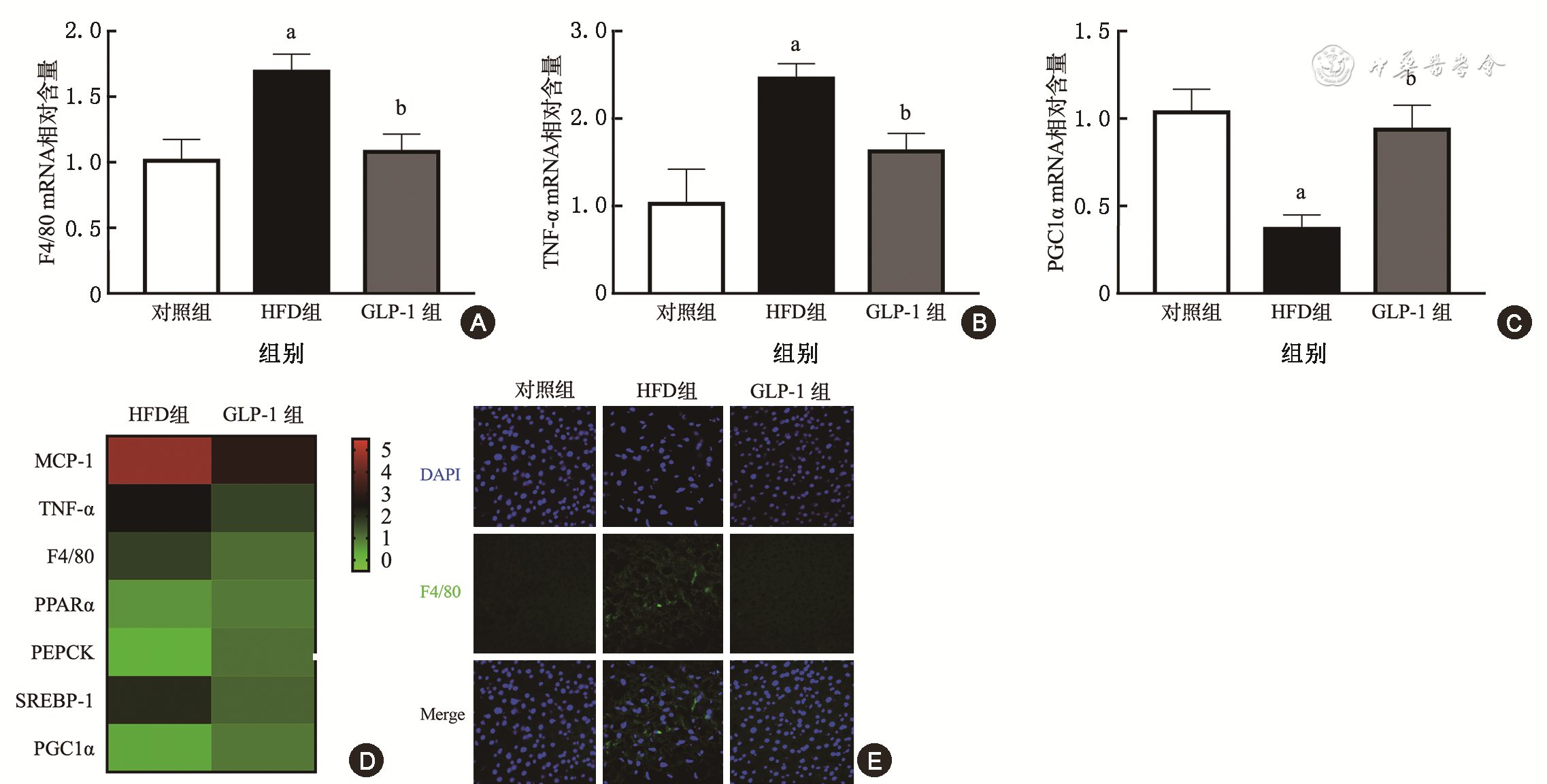
注:GLP-1为胰高糖素样肽-1;TNF为肿瘤坏死因子;PGC为过氧化物酶体增殖物激活受体γ共激活因子;HFD为高脂饮食;与对照组比较,aP<0.05;与HFD组比较,bP<0.05
敲除GDF15基因后,HepG2细胞的GDF15蛋白分泌被显著抑制(
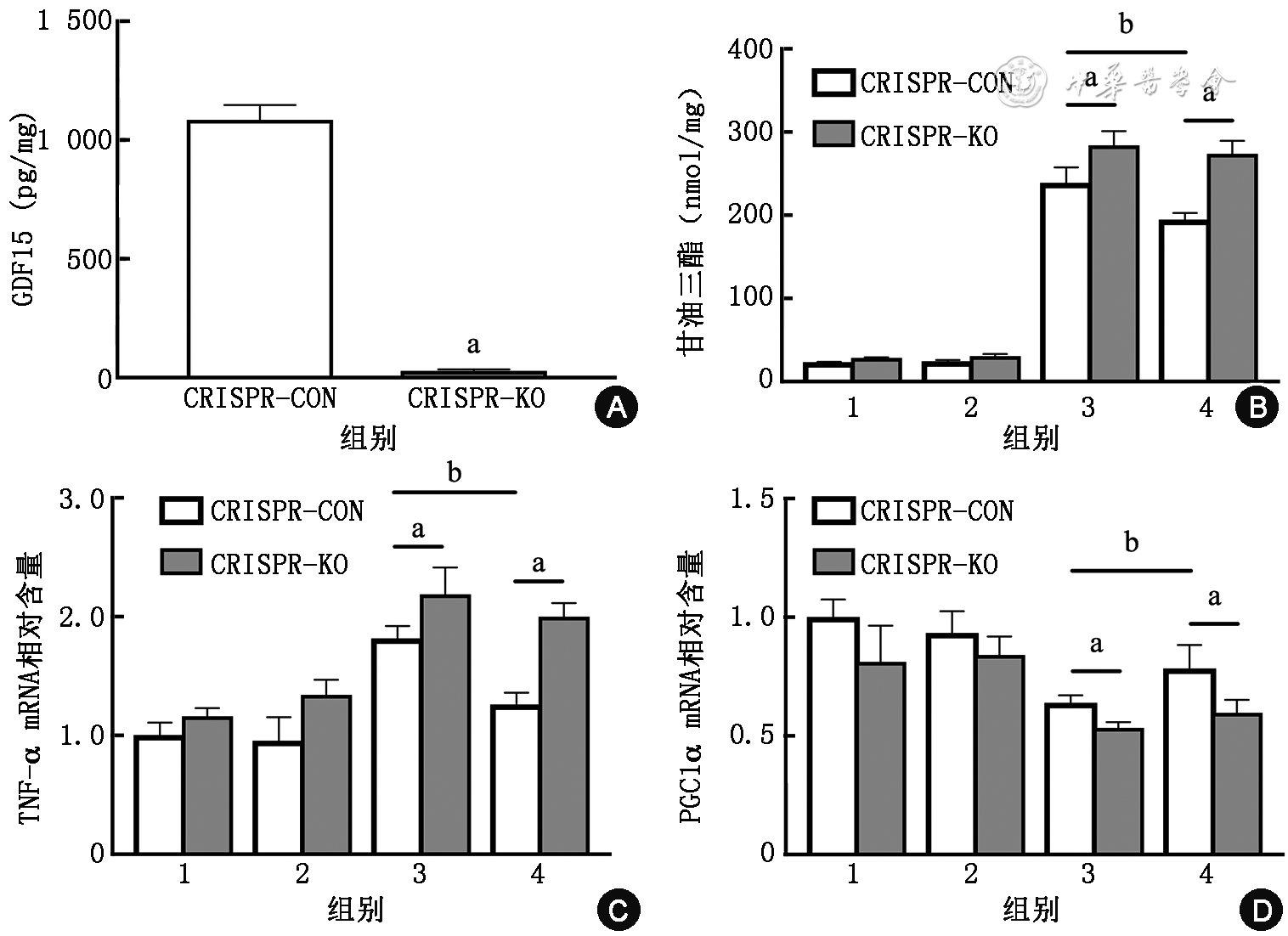
注:GLP-1为胰高糖素样肽-1;GDF15为生长分化因子15;TNF为肿瘤坏死因子;PGC为过氧化物酶体增殖物激活受体γ共激活因子;CRISPR-CON为阴性对照组;CRISPR-KO为GDF15敲除组;300 μmol/L PA为棕榈酸钠(PA)干预组;1为10%BSA组;2为10%BSA+100 nmol/L GLP-1组;3为300 μmol/L PA组;4为300 μmol/L PA+100 nmol/L GLP-1组;与阴性对照组比较,aP<0.05;与PA干预组比较,bP<0.05
NAFLD是一类以肝脏脂质沉积为病理特点的获得性代谢应激性肝损伤[18]。既往研究发现,GLP-1可通过减少脂肪从头合成、促进脂肪β氧化等作用减少肝脏脂质沉积,改善胰岛素敏感性[19, 20]。本研究在人群、动物、细胞三个层次上的结果均表明,GLP-1可改善NAFLD的肝脏脂质沉积。
肝脏组织是循环GDF15的主要来源之一[7]。GDF15可通过减少脂肪合成、促进脂肪利用改善肥胖相关NAFLD[21]。对GDF15敲除小鼠喂养高果糖高脂饮食,小鼠表现出更显著的肝脏组织炎症及纤维化、更严重的肝内脂质沉积及外周胰岛素抵抗[7],说明GDF15可参与调控肝脏脂质代谢。既往研究表明,二甲双胍可剂量依赖性的促进T2DM患者血清GDF15表达水平[22]。另有研究发现,二甲双胍可上调T2DM患者及HFD小鼠的血清GDF15表达及降低体重,推测二甲双胍可能通过上调GDF15从而抑制食欲进而降低体重[23]。我们发现,在NAFLD合并T2DM人群上,GLP-1可显著升高血清GDF15水平。进一步相关性分析表明,ΔGDF15与ΔIHL呈负相关关系。提示GDF15可能参与了GLP-1改善NAFLD肝脏脂质沉积的作用。在高脂喂养小鼠及PA诱导的HepG2细胞中,GLP-1可上调肝脏GDF15表达及分泌,这种作用在HepG2细胞中表现为时间及剂量依赖性的升高。且GDF15基因敲除显著削弱了GLP-1改善细胞TG蓄积和炎症的作用。以上结果表明,GLP-1可显著促进肝细胞GDF15的表达与分泌,且GDF15参与了GLP-1改善肝脏的脂质沉积及炎症状态。
我们发现,GLP-1仅在PA诱导的病理状态下促进GDF15的表达与分泌,而在无PA干预的BSA对照组中,GLP-1对GDF15的表达及分泌无明显影响。有研究报道,GDF15敲除小鼠在给予普通饮食时,小鼠的糖脂代谢及肝脏TG含量均无明显变化[7]。Day等[23]研究也表明,GDF15的敲除只削弱了二甲双胍在高脂饮食小鼠中的作用,而对普通饮食小鼠无明显影响。因此推测,GDF15可能仅在病理状态下参与GLP-1改善肝脏脂质沉积的作用。
此外,我们发现无论是在高脂饮食喂养的小鼠中,还是在PA诱导的HepG2细胞中,GDF15水平较正常对照组相比均有统计学差异的升高。既往临床研究发现,NAFLD患者血清GDF15水平与其肝脏炎症、气球样变和纤维化的严重程度呈正相关[11]。长期高脂喂养可上调血清和肝脏GDF15水平[7]。但过表达GDF15,高脂饮食喂养的C57小鼠肝脏脂质沉积及胰岛素抵抗均得到明显改善[21]。这种内源性的GDF15增多可能是机体延缓NAFLD进展的一种代偿机制。但仍需进一步研究以阐明其中可能的作用机理。
综上所述,GLP-1可促进GDF15的表达及分泌,并改善NAFLD的肝脏脂质沉积和炎症状态。GDF15可能仅在病理状态下参与GLP-1改善肝脏脂质沉积的作用。
作者投稿及专家审稿请登录中华糖尿病杂志官方网站:zhtnbzz.yiigle.com
