食欲调控机制的研究进展
中华糖尿病杂志,第13卷第12期 第1177页-第1182页
卢琰,郝瑞英,何钊,李秋,肖新华
近年来,肥胖的发病率和患病率迅速上升,全球成人肥胖人数达6.5亿,中国成人肥胖患病率达14.0%,较1980年增加近8倍[1]。这也显著增加了人们患心血管疾病、2型糖尿病、卒中以及某些癌症的风险[2]。由于食欲调控系统功能障碍可导致机体过度进食,进而引起肥胖。因此,深入了解食欲的调控机制对于防治肥胖症及相关代谢疾病具有重要意义。本文重点综述了食欲的中枢调控机制,并阐述外周食欲调节系统对食欲中枢的影响,以期为防治肥胖症及其相关代谢疾病提供参考。
下丘脑是调控食欲的重要中枢部位,由多个相互联系的灰质核团组成,包括内侧区核团和外侧区核团。其中弓状核、腹内侧核、背内侧核、室旁核、视交叉上核位于下丘脑内侧区,外侧下丘脑位于下丘脑外侧区,它是下丘脑与其他部位联系的神经纤维出口。
1.弓状核:弓状核内含有两类神经元,一类是表达前阿片黑素细胞皮质激素/可卡因-苯丙胺调节转录肽(pro-opiomelanocortin/cocaine amphetamine regulated transcript,POMC/CART)神经元,另一类是表达神经肽Y/刺豚鼠相关蛋白(neuropeptide Y/Agouti-related protein,NPY/AgRP)神经元。其中POMC/CART神经元主要产生抑制进食的作用,NPY/AgRP神经元主要产生促进进食的作用。两类神经元的相互关系及其作用机制如
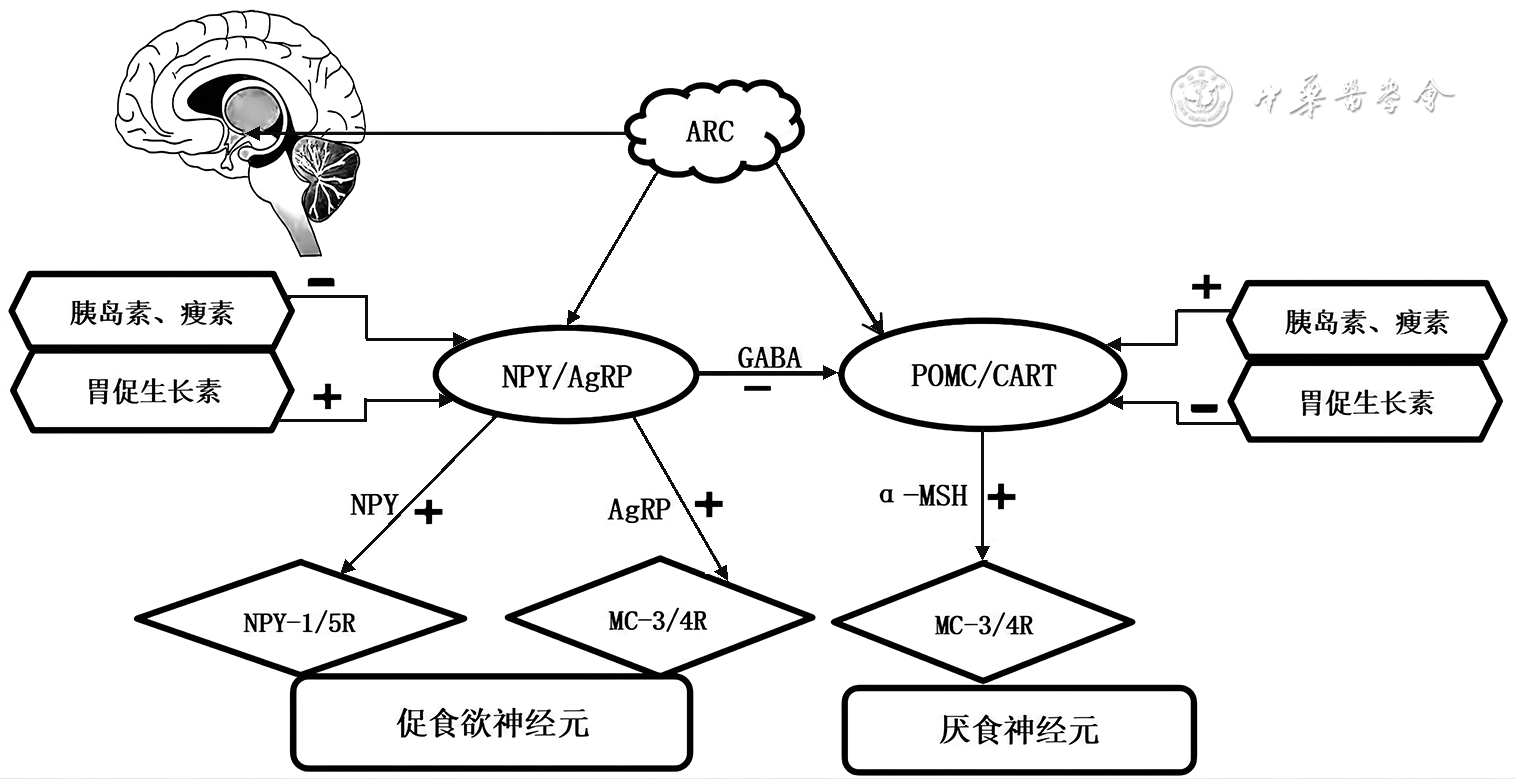
注:ARC为弓状核;NPY为神经肽Y;AgRP为刺豚鼠相关蛋白;GABA为γ-氨基丁酸;POMC为前阿片黑素细胞皮质激素;CART为可卡因-苯丙胺调节转录肽;α-MSH为α-黑色素细胞刺激素;NPY-1/5R为神经肽Y受体-1或神经肽Y受体-5;MC-3/4R为黑皮质素受体-3或黑皮质素受体-4。+表示促进,-表示抑制
其中POMC可裂解生成α-黑色素细胞刺激素(α-menalocyte-stimulating hormone,α-MSH),其受体MC-3/4R在室旁核、外侧下丘脑等诸多核团及下丘脑外区域广泛表达。α-MSH与MC-3/4R结合,特别是与MC-4R结合时,可抑制进食,而AgRP与MC-3/4R结合、NPY与NPY-1/5R结合可拮抗α-MSH的作用,促进进食[3]。近年来研究发现,NPY/AgRP神经元还可释放抑制性神经递质γ-氨基丁酸(γ-aminobutyric acid,GABA),作用于脑内几种厌食神经元(包括POMC/AgRP神经元),这与NPY/AgRP对POMC/CART神经元的直接抑制作用有关,在弓状核内可形成一个调控进食的回路,将信息传递到室旁核及其他核团,共同调控食欲[4]。此外,由于弓状核靠近正中隆起,缺乏完整的血脑屏障,各种外周因子可通过与弓状核内相应受体结合调控食欲。
2.室旁核:室旁核通常被认为是抑制食欲的中枢,主要产生抑食欲神经肽,包括促肾上腺皮质激素释放激素、促甲状腺激素释放激素、血管加压素和催产素(oxytocin,OT)。在早期,Atasoy等[5]用光遗传学方法激活由弓状核内AgRP神经元投射至室旁核的轴突,发现正常状态的小鼠食欲会明显增长,随后他们用药理学方法表明AgRP神经元可向室旁核的突触后神经元释放抑制性神经递质GABA。他们还通过化学遗传学的方法抑制室旁核内的OT神经元,发现正常状态的小鼠食欲也会增加,并且同时激活AgRP神经元和OT神经元可引发食欲,但同时激活OT神经元时小鼠的进食量要低于只激活AgRP神经元时的小鼠进食量,这表明AgRP神经元对于OT神经元的抑制性投射可能对于激发食欲具有重要的作用。此外,Krashes等[6]研究表明,室旁核中表达促甲状腺激素释放激素和垂体腺苷酸环化酶激活肽的神经元是AgRP神经元的重要兴奋性传入来源,激活这些神经元可显著活化AgRP神经元并引发进食,若抑制这些神经元,即使在饥饿状态下小鼠的进食量也会明显减少,这表明室旁核内某些类型的神经元是促进食欲神经环路的节点。
3.腹内侧核:腹内侧核是接受、整合与传递代谢信号的饱食中枢。它主要接受来自弓状核的信息,并投射至弓状核、背内侧核、外侧下丘脑和脑干等区域。腹内侧核可合成Ⅰ型类固醇生成因子和释放脑源性神经营养因子,抑制机体进食[7]。此外,腹内侧核内含有感受葡萄糖和瘦素的神经元,腹内侧核受损可产生迅速而持久的食欲亢进、体重增加以及高血糖[8]。
4.背内侧核:背内侧核通常是促进进食的饥饿中枢,其内富含NPY,可接受来自弓状核投射的神经纤维。Yokosuka等[9]早期研究发现并推断NPY和瘦素相互作用的区域可能存在于背内侧核,背内侧核与腹内侧核之间的神经通路是相互联系的。近年来有研究发现,背内侧核的NPY神经元可发出纤维直接投射至孤束核的儿茶酚胺能神经元,抑制胆囊收缩素厌食效应,促进机体进食[10]。
5.外侧下丘脑:外侧下丘脑通常是促进进食的饥饿中枢,可同时接受来自弓状核的NPY/AgRP和POMC/CART神经元投射,并投射至大脑系统以及大脑皮层外区域。其内有表达抑食欲因子黑素浓集素和神经降压素及促食欲因子食欲素的神经元。其中食欲素表达神经元可广泛投射至弓状核(尤其是NPY神经元)、腹内侧下丘脑、背内侧核、室旁核以及腹侧被盖区(ventral tegmental area,VTA)[11]。外侧下丘脑受损后可引起暂时性食欲亢进及体重增加。
6.视交叉上核:视交叉上核是哺乳动物脑内的昼夜节律起搏器,其神经元可接受光信息,感知外界环境的昼夜变化。Granados-Fuentes等[12]发现视交叉上核能调控动物食欲的昼夜变化,其内个别区域受损以及持续的光照可以引起食欲调控丧失。此外,个体的代谢状态也以昼夜节律的方式影响食欲的昼夜变化。研究发现,健康个体在夜间瘦素水平较高,有利于降低食欲,白天瘦素水平低,可使饥饿感增加,促进机体进食,而肥胖个体在白天和夜间的瘦素水平均比瘦弱个体高得多,这表明其瘦素抵抗状态较高,但循环中瘦素的昼夜节律并不改变[13]。
7.孤束核:孤束核靠近室周器官最后区,由于缺乏完整的血脑屏障,它可同时接受中枢和外周信号的调控,与弓状核共同被认为是大脑感知机体营养状态的第一级神经元。孤束核内富含儿茶酚胺能神经元,近年来有研究者通过化学遗传学和光遗传学的方法激活儿茶酚胺能神经元,可明显促进小鼠进食,抑制儿茶酚胺能神经元可明显降低饥饿诱导的进食,这表明孤束核儿茶酚胺能神经元可感知饥饿信号并促进食欲,此外,通过肠胃迷走神经切断的方法,研究者进一步发现儿茶酚胺能神经元可通过迷走神经感知饥饿信号促进进食[14]。
近年来,研究者发现人们经常在没有饥饿的情况下进食,即享乐性进食。这种享乐性进食是指不受代谢反馈调节的食物摄入,与认知、奖励和情绪因素有关[15]。目前认为,享乐性进食主要受大脑奖赏系统的调控,其重要脑区包括VTA、伏隔核、背侧纹状体和腹侧纹状体等。其中,从中脑VTA至伏隔核的多巴胺能通路是大脑奖赏系统的核心,多巴胺能神经元胞体主要位于中脑VTA和黑质[16]。机体进食时,食物信号可激活中脑VTA中的多巴胺能神经元,进而增加伏隔核中多巴胺的含量及促进多巴胺的释放,使机体获得进食后的快乐感,使机体有持续进食的倾向[16]。此外,外侧下丘脑内的黑素浓集素神经元可投射到丘脑外区,包括伏隔核,调节VTA和脑干核(如孤束核),在调节肠道信号和饱腹感信号中起重要作用[17]。胰岛素、瘦素等也可与VTA的多巴胺能神经元表达的相应受体结合,调节中脑多巴胺系统的活性[11]。当食欲奖赏系统发生功能障碍时,会引起机体享乐性过度进食,导致享乐性肥胖。因此,深入了解大脑奖赏系统的食欲调控机制对防治享乐性肥胖及相关代谢疾病具有重要的意义。
1.食欲素:食欲素包括食欲素A和食欲素B。早期研究发现,向脑室内注射食欲素A和食欲素B可引起剂量依赖性进食增加,且食欲素A的作用要比食欲素B强,但食欲素A和食欲素B的增食效应均低于NPY[18]。研究发现,用NPY拮抗物进行预处理可显著降低食欲肽的诱食反应,这提示NPY神经位于食欲调节机制的下游区[19]。
2.谷氨酸和GABA:谷氨酸是脑内主要的兴奋性神经递质,Liu等[20]发现AgRP神经元上存在谷氨酸能的兴奋性输入,这种兴奋性突触能够显著影响进食量和增加体重。将AgRP神经元上的N-甲基-D-天冬氨酸受体敲除,小鼠的进食量和体重均显著降低。因此,谷氨酸在饥饿引起AgRP神经元激活中起重要作用。GABA是脑内重要的抑制性神经递质。通常认为,AgRP神经元活性在能量缺乏时迅速升高,而在进食后又迅速下降。近年来研究发现,在机体进食前,即机体感官检测到食物存在时就能使AgRP神经元的活性下降,这正是通过GABA作用于AgRP神经元实现的[21]。
1.促肾上腺皮质激素释放激素家族:该家族主要包括促肾上腺皮质激素释放激素(corticopin releasing hormone,CRH)与尿皮质素。早期研究发现,将CRH注入脑室可明显减少动物在夜间及禁食诱导的进食行为,向中枢注射CRH也可产生同样的效应[22]。尿皮质素虽与CRH具有45%的同源性,但尿皮质素抑制饥饿诱导的进食作用的能力比CRH强,主要是因为尿皮质激素与CRHR2受体的亲和力比CRH高[23]。此外,Spina等[23]发现,尿皮质激素可降低大鼠在夜晚的进食量和进食频率。
2.胰高糖素样肽-1:在中枢神经系统内,孤束核是脑源性胰高糖素样肽-1(glucagon-like peptide-1,GLP-1)的来源,即前胰高糖素原神经元,前胰升糖素原神经元可直接投射至表达GLP-1受体的VTA和内侧纹状体[24]。早期研究发现,向大鼠的VTA内注入GLP-1受体激动剂可明显降低大鼠的进食量和体重,将GLP-1受体阻断剂注入VTA中,会明显增加大鼠的进食量[24],这表明GLP-1可作用于中脑边缘奖赏系统参与食欲调控。近来研究发现,GLP-1还可降低弓状核中的5-羟色胺受体的表达,刺激POMC/CART发出饱感信号,并通过GABA依赖的信号通路减少NPY/AgRP神经元产生的饥饿信号,抑制食欲[25]。此外,临床研究证实,GLP-1受体激动剂能有效延缓肥胖者及2型糖尿病患者的胃排空,减少进食和控制体重[26]。因此,对于2型糖尿病伴肥胖的患者,GLP-1类药物比其他传统降糖药物更有优势。
1.瘦素:瘦素主要在弓状核内发挥作用,弓状核内的NPY/AgRP神经元和POMC/CART神经元均可表达瘦素受体,瘦素与其受体结合可抑制NPY/AgRP神经元,并激活POMC/CART神经元,抑制食欲。早期研究发现,瘦素可抑制胃促生长素在胃和弓状核的促食欲作用,同时胃促生长素也可反转瘦素的抗食欲作用[27],这提示胃促生长素在NPY/AgRP调控系统中可能具有抵抗瘦素的效应。近年来研究发现,瘦素还可抑制食欲素和黑素浓集素神经元,这些神经元可投射到至中脑区,发挥调节多巴胺的作用[28]。
2.胰岛素:近年来,中枢胰岛素的作用成为当前研究的热点之一。目前研究认为,脑组织不能或只能合成微量的胰岛素,中枢胰岛素主要经由血脑屏障进入脑内发挥作用[29]。在脑内,中枢胰岛素既可以促进葡萄糖进入脑细胞,维持中枢神经系统的正常运行,也可作为一种厌食信号调节食欲。在早期,研究者发现长期向狒狒的侧脑室灌注微量的胰岛素可减少狒狒的食物摄取和体重[30]。后来在人类身上也观察到了同样的现象[31]。目前研究发现,向啮齿类动物第三脑室注射胰岛素可抑制NPY和AgRP的表达,增强POMC和CART的表达,从而刺激α-MSH的活性,抑制食欲,且在胰岛素绝对缺乏的大鼠(链脲佐菌素诱导的糖尿病大鼠)的下丘脑中,NPY和AGRP的表达增加,POMC表达减弱,这表明胰岛素在中枢主要通过上调α-MSH来发挥抑食效应[27]。
3.脂联素:脂联素是一种主要由脂肪细胞分泌的激素,其受体AdipoR1和AdipoR2主要在弓状核和外侧下丘脑核中表达。目前研究发现,脂联素与AdipoR1结合可增强弓状核中的AMP依赖的蛋白激酶(adenosine 5′-monophosphate-activated protein kinase,AMPK)活性,促进食物摄入[32]。主要表现为:禁食时,血清和脑脊液脂联素水平和弓状核中AdipoR1表达增加,下丘脑AMPK被激活,增加进食;进食后,机体脂联素水平和AdipoR1表达降低,导致AMPK激活降低,减少进食[32]。此外,研究发现,患有进食障碍(如神经性厌食症和暴食症)的患者的脂联素水平有所改变[33, 34],特别是神经性厌食症患者的脂联素水平会明显升高,而脂联素的下降则与暴饮暴食密切相关[34]。
4.胃促生长素:胃促生长素是目前已知的唯一一种增强食欲的胃肠激素。Iyer等[35]第一次证明了胃促生长素受体的促食欲作用与下丘脑POMC mRNA的表达减少有关,而并不是只依靠增加NPY mRNA表达来增加食欲。他们还发现,在弓状核中,胃促生长素可刺激NPY通路,抑制POMC通路。另外,有研究表明,胃促生长素能够部分引起AgRP神经元的兴奋性输入,但这一效应可被瘦素相关作用阻断[36]。瘦素与胃促生长素的作用机制如

注:POMC为前阿片黑素细胞皮质激素;CART为可卡因-苯丙胺调节转录肽;NPY为神经肽Y;AgRP为刺豚鼠相关蛋白。虚线表示抑制,实线表示促进
1.大麻素系统:大麻素系统通常参与促进机体脂肪积累和能量储存。近年来,Harrold等[11]发现,在饱足状态下大麻素也会促进食欲,增加对甜食和高脂肪食品的摄入,其机制可能是动物进食时大麻素所导致的愉快心情与进食本身形成一种条件反射,使动物乐于进食。
2.肠道菌群:近年来许多研究认为,肠道菌群可通过肠道菌群-肠-脑轴参与食欲调控。其主要机制为:(1)调节胃肠激素。有研究发现,无菌小鼠表达瘦素、胆囊收缩素及其他抑食欲激素的基础水平较正常小鼠明显降低[37],在小鼠日常饮食中加入含乳杆菌菌株混合物的补充物后可增加血清GLP-1的含量,并减少下丘脑中AgRP和NPY的表达[38],抑制小鼠的食欲。此外,Schéle等[39]发现,一些肠道菌群还可通过降低瘦素的敏感性调节食欲。(2)调节与食欲相关的神经递质。肠道微生物可促进血液中色氨酸分泌并通过短链脂肪酸作用于肠嗜铬细胞促进5-羟色胺(5 hydroxytryptamine,5-HT)分泌[40]。研究发现,5-HT与POMC神经元表达的5-HT2C受体结合,可刺激POMC神经元,使α-MSH水平升高,进而刺激黑皮质素系统,同时,5-HT也可激活5-HT1B受体抑制NPY/AgRP神经元,抑制食欲[41]。(3)肠道菌群还影响中脑边缘多巴胺系统,其分泌的丙酸盐可通过调节纹状体通路减少对高能量食物的预期回报反应,从而抑制食欲[42]。此外,研究发现,高脂饮食诱导的肥胖小鼠对甜味刺激感觉减弱,补充益生菌后,小鼠的甜味味觉改善,对脂肪的摄入减少,这说明肠道菌群还可通过改变动物对食物的偏好来调控摄食行为[43]。
3.叉头状转录因子O亚族1(forked head transcription factor O1,FoxO1):FoxO1是胰岛素和瘦素信号途径中的重要调节蛋白。目前研究表明,胰岛素可以调节FoxO1的活性,影响AgRP和POMC的基因表达[43]。人体在空腹时胰岛素分泌减少,FoxO1在下丘脑细胞核中功能活跃,可增强食欲并产生摄食行为,进食后胰岛素分泌增加,FoxO1磷酸化失活后进入下丘脑细胞质,抑制食欲[43]。另外,瘦素在细胞内主要通过转录激活因子3(signal transducer and activator of transcription 3,STAT3)和FoxO1来调节AgRP和NPY的转录活性[21]。FoxO1可显著增加AgRP的转录活性,而STAT3主要阻断FoxO1对AgRP启动子区的激活作用[21],瘦素可通过抑制FoxO1和激活STAT3下调AgRP的转录水平,抑制食欲。
4.游离脂肪酸受体4(free fatty acid receptor 4,FFA4):FFA4是Fredriksson等[44]在2003年发现的一种G蛋白偶联受体。研究表明,下丘脑对营养过量会产生炎症反应,引起抑食欲激素抵抗,FFA4的中枢激活可抑制NPY神经元并减轻下丘脑损伤,提高中枢瘦素和胰岛素等食欲抑制因子的敏感性,还可促进POMC神经元分泌POMC,参与食欲的调控[45]。FFA4也可通过抑制胃促生长素的表达来增加GLP-1和胆囊收缩素的分泌[45]。此外,食欲奖赏相关的脑区,如VTA、伏隔核等也可表达FFA4[45],这提示FFA4可能也参与食欲奖赏系统的调控。因此,FFA4有潜力成为降低食欲的新靶点。
综上所述,食欲既受下丘脑食欲调节中枢的调控以满足机体代谢所需,又受食欲奖赏系统的调控。中枢或外周的各种促进/抑制食欲的调节因子可通过与两大系统内的相应受体结合对食欲进行综合调控。此外,大麻素系统、肠道菌群、FoxO1、FFA4等也参与食欲的调控,但其详细机制还未被完全阐明,未来仍需对此进行更加深层的研究,为控制食欲和防治相关代谢疾病提供更加科学的依据。
作者投稿及专家审稿请登录中华糖尿病杂志官方网站:zhtnbzz.yiigle.com
