mA结合蛋白YTHDC2调节p38MAPK信号通路影响结直肠癌细胞凋亡
中华结直肠疾病电子杂志,第12卷第2期 第117页-第124页
张师垚,徐岩岩,张琦,李春强,赵智成,刘刚
2020年全球范围内新发癌症病例中,结直肠癌发病率位列第三,占全部新发病例的9.8%,死亡率为9.4%[1],近年来结直肠癌发病率和死亡率呈上升趋势。结直肠癌的发生和转移是由多基因共同参与的复杂过程,相关研究表明,RNA参与基因的表达和调控,在结直肠癌的发生与发展中起到了重要作用[2]。N6-甲基腺苷(m6A)修饰是真核生物RNA中最常见的转录后修饰,其参与RNA代谢的多个过程,包括mRNA前剪接、3’端加工、核输出、翻译调控、mRNA降解和非编码RNA加工,在癌症发生与发展中起到了关键作用[3, 4, 5]。YTHDC2是m6A结合蛋白中YTH域蛋白家族成员之一,有研究表明,YTHDC2在胰腺癌和肝癌的发生与发展过程中可能起到一定作用[6, 7],在结直肠癌中所起作用尚未清楚,本实验对YTHDC2在结直肠癌发生发展中的作用进行探讨,探究其参与的分子调控机制及影响的信号通路,为结直肠癌药物治疗提供新思路。
抗YTHDC2、抗p38MAPK、抗p-p38MAPK、抗Fas、抗Caspase-8、抗Caspase-9、抗Bax、抗细胞色素、抗甘油醛3-磷酸脱氢酶抗体购自美国Abcam公司;Anti-Fas Ligand、Anti-Caspase-12购自Bioss公司(中国北京);辣根过氧化物酶(HRP)偶联二抗购自美国CST公司。异硫氰酸荧光素(FITC)和四甲基罗丹明(TRITC)标记的二抗购自美国Earthox公司。pCMV3-YTHDC2-Flag和pCMV3-C-Flag质粒由北京义翘神州生物技术有限公司合成,si-YTHDC2由苏州吉玛基因股份有限公司合成。
1. 生物信息学数据分析:使用人类蛋白质图谱(The Human Protein Atlas)和基因表达谱交互分析(GEPIA)网站上的在线工具,分析TCGA数据库中结直肠癌和YTHDC2之间的关系。在cBioPortal和Xena数据库下载与结直肠癌相关的基因表达量和临床数据,在KEGG和GO数据库中下载注释基因集。用基因集富集分析(GSEA)软件对数据进行富集分析,以研究YTHDC2在结直肠癌中参与调控的信号通路和生物学过程。
2. 细胞培养:分别培养HCT116、HCT-8、Caco2、HT29、SW480、SW620等结直肠癌细胞系,Western blot检测各细胞系中YTHDC2的表达量,发现YTHDC2表达量在HCT116细胞系中比Caco2细胞系显著降低,选用Caco2细胞系为YTHDC2高表达细胞系,HCT116细胞系为YTHDC2低表达细胞系。两细胞系均在5%CO2、37 ℃饱和湿度环境下的含有10%胎牛血清、链霉素(100 μg/mL)和青霉素(100 单位/mL)的培养基中进行培养。
3. 质粒转染:当细胞密度达到80%~90%时,根据后续处理分为4组:YTHDC2组(过表达YTHDC2)转染pCMV3-YTHDC2-Flag质粒,siYTHDC2组(敲低YTHDC2组)转染si-YTHDC2,con-YTHDC2组(过表达YTHDC2组阴性对照组)转染pCMV3-C-Flag,NC-siYTHDC2组(敲低YTHDC2组阴性对照组)转染si-NC。用Lipofectamine 2000试剂(Invitgen,USA)进行质粒和siRNA的转染。
4. 免疫荧光分析:采用免疫荧光法检测YTHDC2在Caco2细胞中的定位。将Caco2细胞的单细胞悬液等分到24孔板中。当细胞密度达到80%~90%时,用4%多聚甲醛在室温下固定细胞20分钟,然后用0.3% TritonX-100钻取1小时。在用5%牛血清白蛋白阻断30分钟后,用抗YTHDC2孵育细胞1小时,在黑暗条件下用FITC和TRITC标记的第二抗体孵育0.5 h~1 h,用4’,6-二脒基-2-苯基吲哚对细胞进行反染色,并在共聚焦显微镜下观察。
5. 流式细胞术检测细胞凋亡变化:将转染的HCT116和Caco2细胞重新悬浮,用流式细胞仪计数并收集5×105个细胞。依次加入结合缓冲液(500微升)、Annexin V-FITC试剂(5微升)和碘化丙啶试剂(5微升),并在黑暗条件下将混合物在室温下孵化5~15分钟。激发波长(Ex)=488纳米,发射波长(Em)=530纳米。1小时内进行细胞检测。
6. 划痕实验:在转染后24小时,用微吸管尖端在每个孔的中心做一直划痕。用无菌的磷酸盐缓冲盐水清洗自由悬浮的细胞,并在划痕后0、12、24和48小时用显微镜对该溶液进行成像。
7. RT-PCR:转染后分离出总RNA,逆转录为cDNA,进行转录定量,详细步骤按试剂盒说明书操作。
8. Western blot检测蛋白表达:获得转染的HCT116和Caco2细胞后,使用放射免疫沉淀试验(RIPA)裂解液进行裂解。测量总蛋白浓度后,用十二烷基硫酸钠聚丙烯酰胺凝胶电泳(SDS-PAGE)分离蛋白样品,电转至聚偏氟乙烯膜(PVDF)上。PVDF用5%的无脂牛奶阻断,并与一抗在4 ℃下孵育过夜,与二抗在室温下孵育1小时,用Chemi Doc XRS系统分析蛋白条带,以GAPDH作为内部对照。
使用SPSS 23.0软件分析数据。采用独立样本t检验对两组间数据进行比较,采用单因素方差分析(ANOVA)对三组及三组以上数据进行比较,两两比较采用最小显著差异方法,P<0.05为差异有统计学意义。
1. TCGA样本生存分析提示:YTHDC2高表达在结肠癌(P<0.001)、直肠癌(P<0.001)亦或是结直肠癌(P<0.001)中均与总生存率呈正相关(
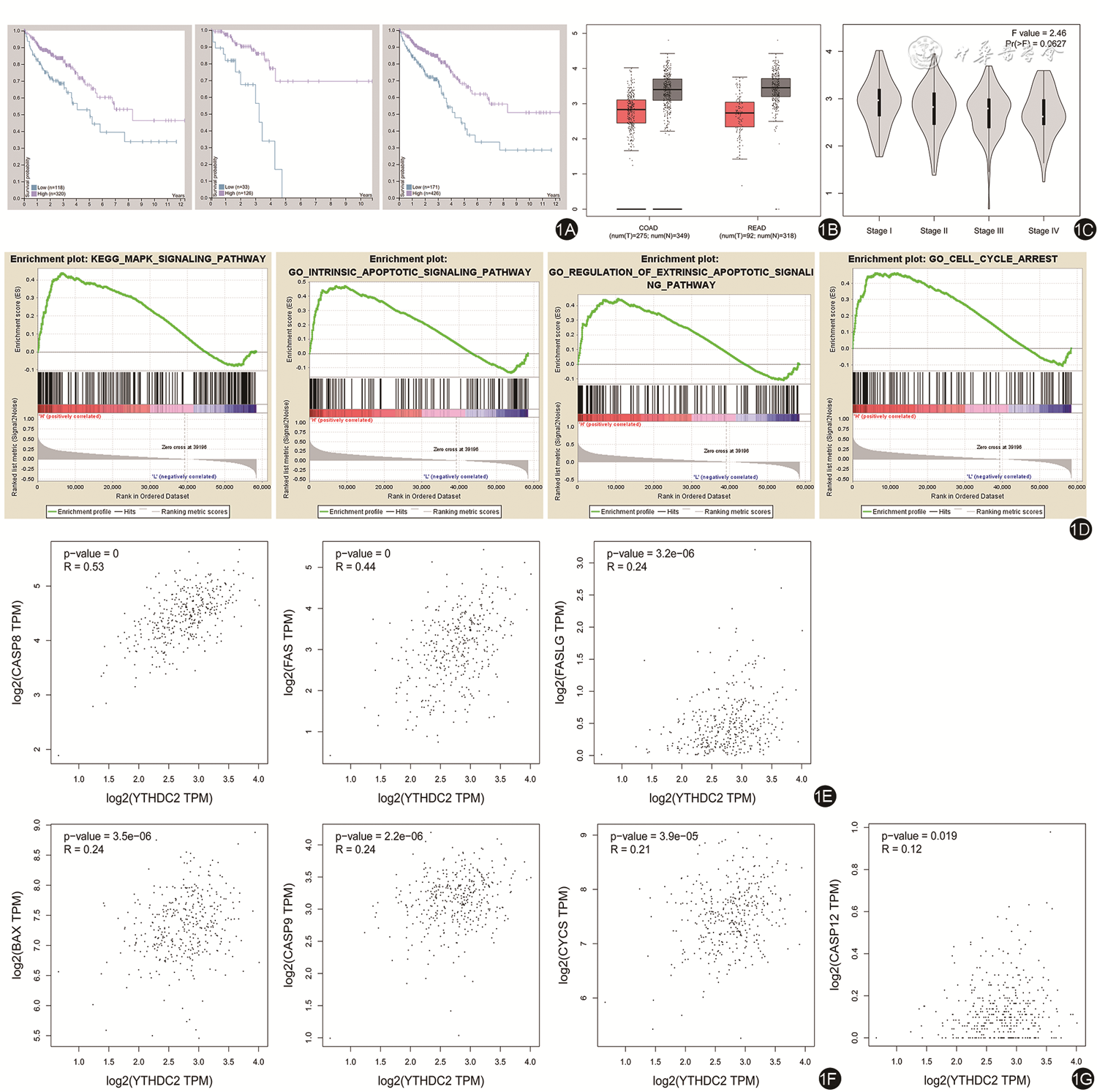
2. KEGG富集分析提示:YTHDC2与丝裂原激活蛋白激酶(MAPK)信号通路有关[效应大小(ES)=0.44,错误发现率(FDR)=0.118,P=0.028],而GO富集分析提示YTHDC2与外在凋亡信号通路(ES=0.45,FDR=0.069,P=0.019)、内在凋亡信号通路(ES=0.47,FDR=0.053,P=0.013)的调控及细胞周期停止(ES=0.46,FDR=0.057,P=0.01)有关(
3. 应用GEPIA网站对YTHDC2和MAPK信号通路下游各种凋亡蛋白进行相关性分析:外源性死亡受体激活通路中,代表性凋亡蛋白Caspase 8(P=0,R=0.53)、Fas(P=0,R=0.44)和Fas L(P=3.2×10-6,R=0.24)与YTHDC2的表达呈正相关(
流式细胞术结果显示,HCT116细胞中,YTHDC2组的细胞凋亡率(18.44%)高于con-YTHDC2组(11.94%)和siYTHDC2组(7.13%)。siYTHDC2组的细胞凋亡率与NC-siYTHDC2组(9.46%)相比更低。Caco2细胞表现出YTHDC2的高表达,免疫荧光实验结果显示YTHDC2主要位于细胞核和核周围区域(
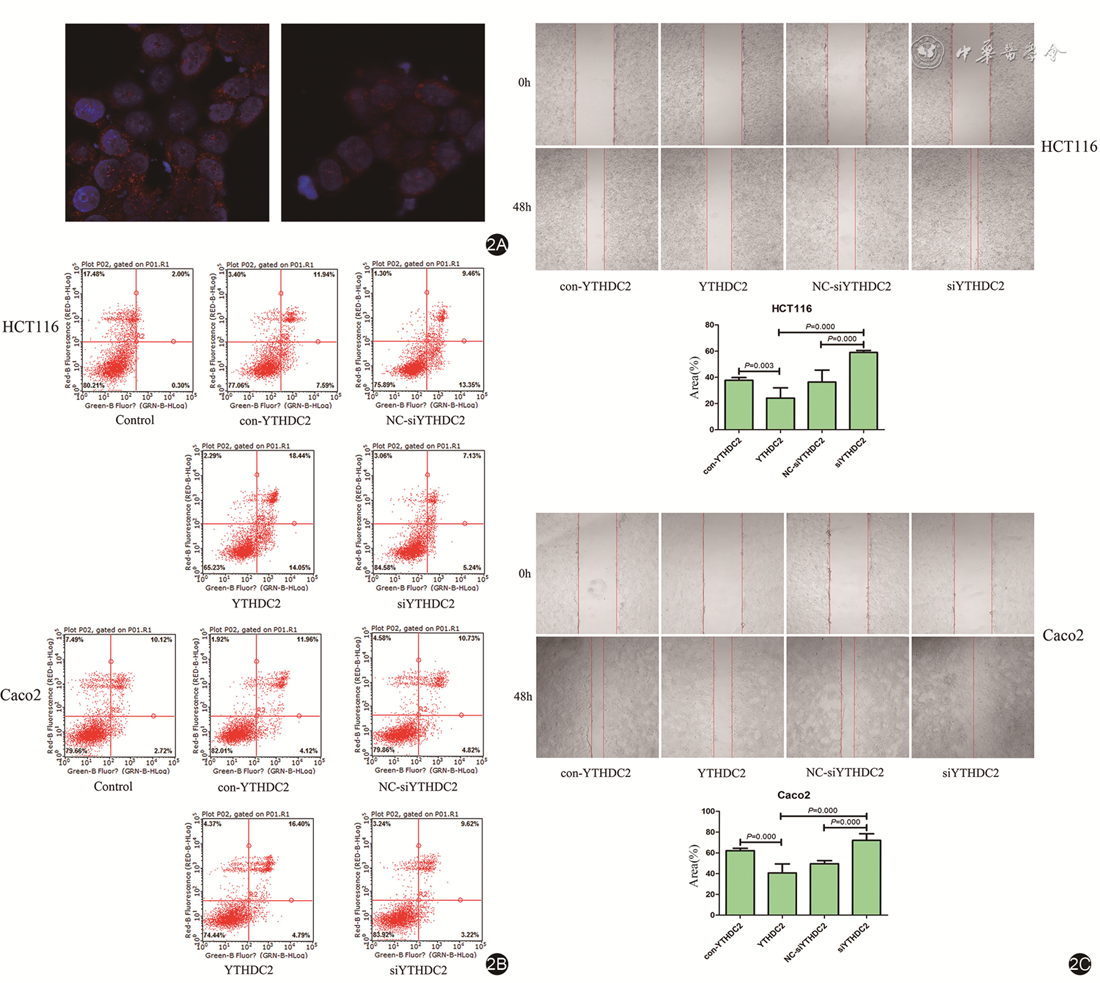
划痕实验结果显示,HCT116细胞的生长在所有转染组之间差异存在统计学意义(F=27.342,P<0.001)。48小时后,YTHDC2组的生长速度显著低于con-YTHDC2组和NC-siYTHDC2组(P=0.003),siYTHDC2组的生长速度则显著高于NC-siYTHDC2组(P<0.001)。YTHDC2组和siYTHDC2组之间差异存在显著统计学意义(P<0.001)。在Caco2细胞中,各组之间的差异同样显著(F=29.051,P<0.001)(
Western blot结果显示,p38MAPK的相对表达水平在HCT116或Caco2细胞中四组之间差异无统计学意义(HCT116:F=0.373,P=0.775;Caco2:F=0.261,P=0.851)。而p-p38MAPK水平差异有统计学意义(HCT116:F=13.088,P=0.002;Caco2:F=4.630,P=0.037),YTHDC2组的表达量显著高于con-YTHDC2组(HCT116:P=0.046,Caco2:P=0.035)和siYTHDC2组(HCT116:P<0.001,Caco2:P=0.007)。在HCT116细胞中,siYTHDC2组的p-p38MAPK水平较NC-siYTHDC2组显著降低(P=0.002)。在Caco2细胞中,siYTHDC2组p-p38MAPK水平与NC-siYTHDC2组相比,表达量存在下降趋势(P=0.106)(
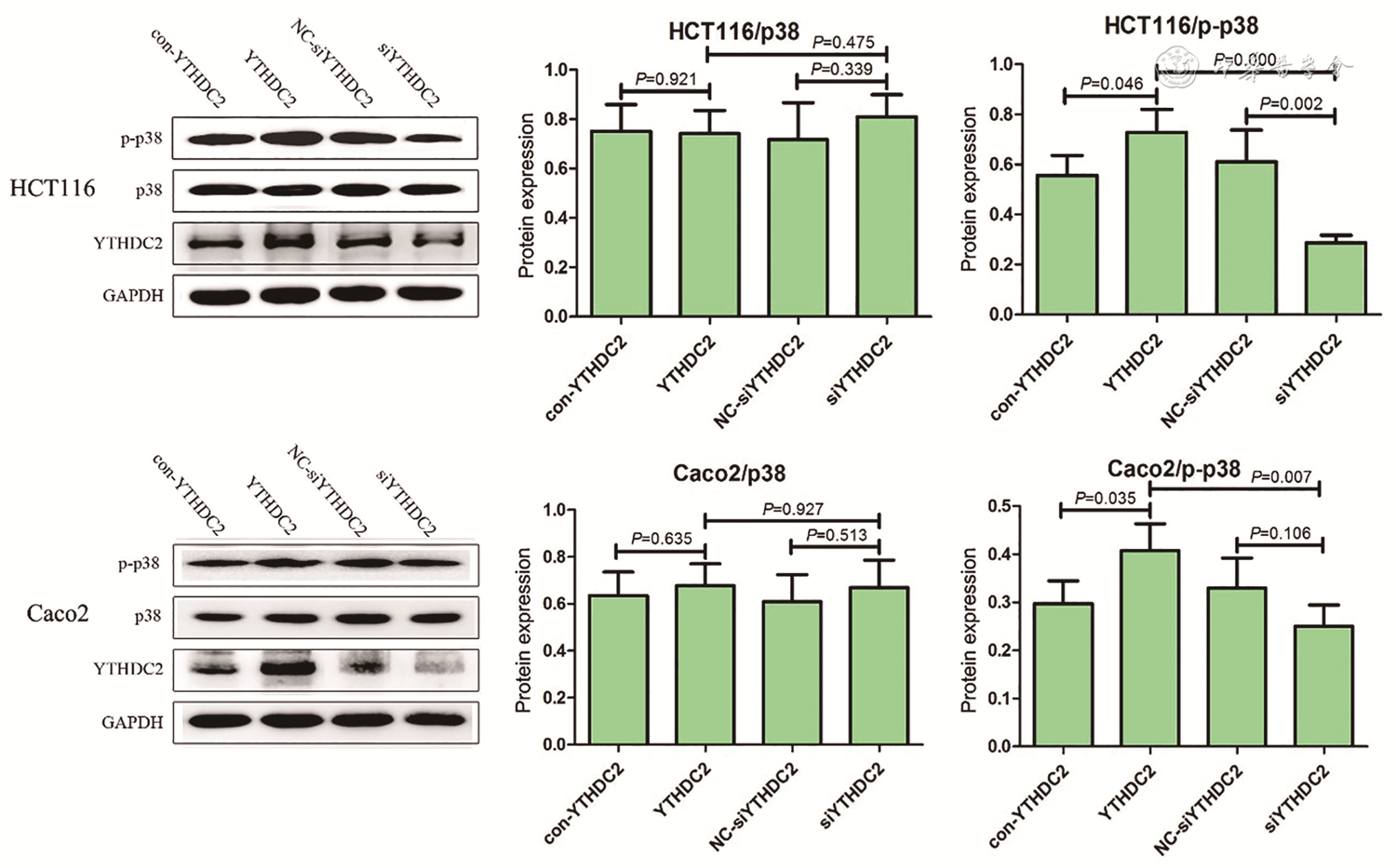
外源性死亡受体激活途径中,Caspase8 mRNA和蛋白在HCT116细胞各组中的表达差异无统计学意义(F=0.542,P=0.667;F=1.776,P=0.229),在Caco2细胞各组中的表达差异有统计学意义(P=0.000;P=0.000)。RT-PCR和Western blot结果显示,Fas mRNA和蛋白在HCT116细胞(F=22.020,P=0.000;F=49.709,P=0.000)和Caco2细胞(P=0.000;P=0.001)中YTHDC2组和siYTHDC2的表达差异均有统计学意义。在HCT116和Caco 2细胞中,YTHDC2组Fas L mRNA表达显著增加,siYTHDC2组Fas L mRNA表达显著降低(P=0.002;P=0.000)。Western blot显示,在HCT116细胞中,随着YTHDC2表达的变化,Fas L蛋白表达无显著变化,四组间差异无统计学意义(F=0.228,P=0.874)。在Caco2细胞中,Fas L蛋白的表达与YTHDC2或Caspase8的表达相比差异无统计学意义(F=7.691,P=0.010)。Caspase 8和Fas L在HCT116和Caco 2细胞中表达水平的差异可能是由于YTHDC2在这两种细胞中表达水平不同所致(
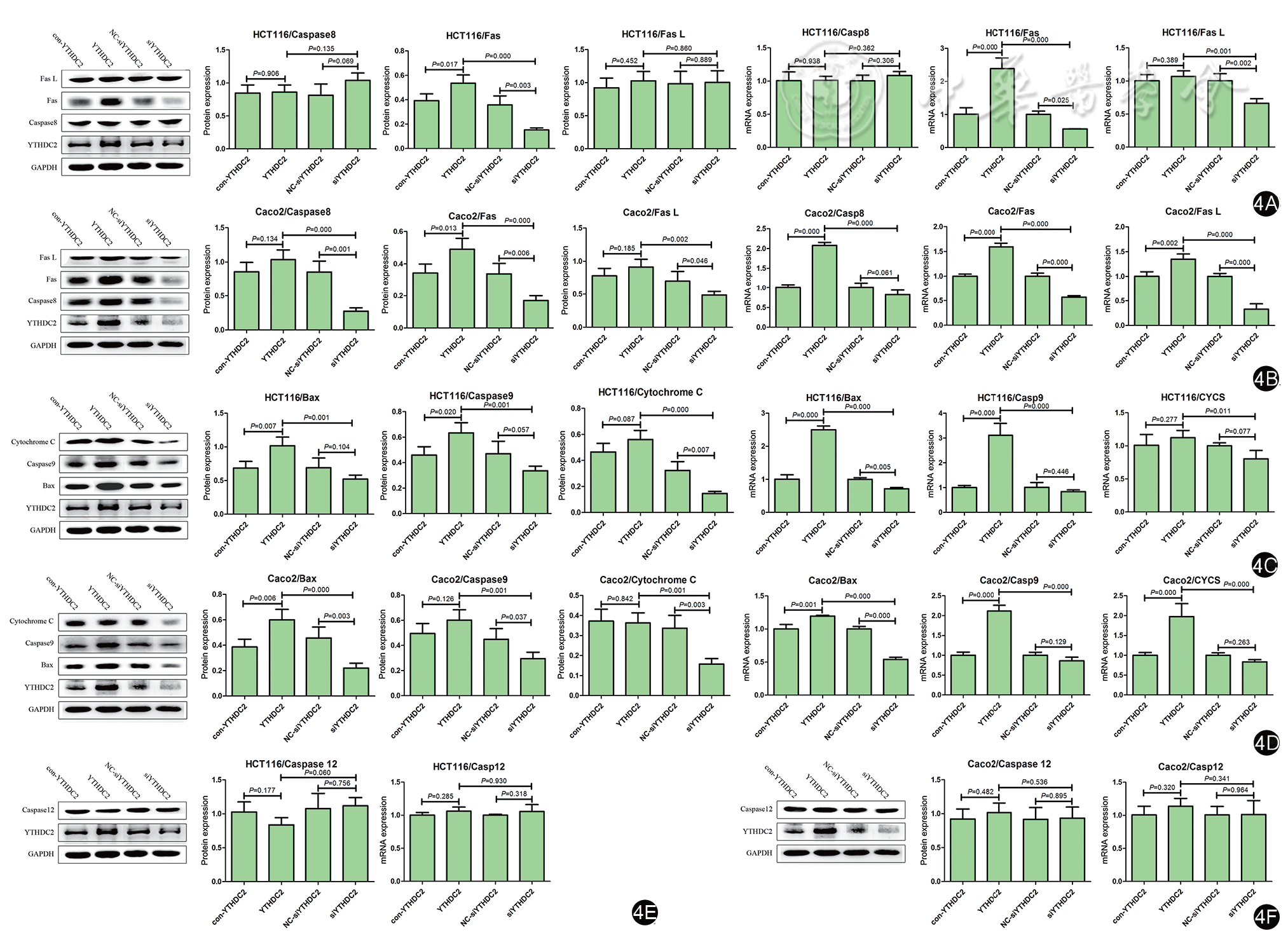
内源性线粒体凋亡相关途径中,HCT116细胞各组中bax mRNA和蛋白表达差异有统计学意义(F=228.456,P=0.000;F=10.211,P=0.004),在Caco2细胞中观察到类似情况。HCT116和Caco2细胞中siYTHDC2组和NC-siYTHDC2组之间Caspase9 mRNA的表达差异无统计学意义(P=0.446;P=0.129),其余各组间差异均有统计学意义(P<0.05)。Caspase9在HCT116和Caco2细胞各组中的蛋白表达差异均有统计学意义(F=8.237,P=0.008;F=8.442,P=0.007)。在HCT116细胞中,Cytochrome C mRNA的表达除YTHDC2和siYTHDC2组(P=0.011)外,其余各组间差异均无统计学意义(P>0.05)。在Caco2细胞中,Cytochrome C mRNA的表达情况与Caspase9相似(P=0.000)。YTHDC2在HCT116和Caco2细胞中的表达变化显著影响Cytochrome C的蛋白表达(F=27.236,P=0.000;F=11.254,P=0.003)。并非所有的凋亡蛋白均表现出统计学上的显著差异,但它们表达的变化反映了YTHDC2表达的变化,表明YTHDC2的变化影响了内源性线粒体凋亡相关的途径(
在内质网凋亡途径中,RT-PCR(HCT116:F=0.818,P=0.519;Caco2:F=0.545,P=0.665)和Western blot(HCT116:F=1.868,P=0.213;Caco2:F=0.268,P=0.847)结果显示Caspase 12在HCT116和Caco2细胞中的表达差异无统计学意义,Caspase12的表达并不随YTHDC2表达的变化而变化,表明YTHDC2介导的促进结直肠癌细胞凋亡的作用并不是通过内源性内质网凋亡途径实现的(
YTH家族蛋白的YTH结构域可以识别和结合含有m6A的RNA,在决定m6A修饰RNA代谢去向的过程中发挥着不同的功能[8]。YTHDF3与YTHDF1相互作用,帮助促进蛋白质翻译,并与YTHDF2相互作用,影响甲基化mRNA转录的降解[9]。YTHDC2是具有YTH结构域的RNA螺旋酶。与其他YTH家族蛋白相似,YTHDC2能够识别并结合mRNA中的m6A分子,从而起到调控作用,其R3H结构域通过稳定YTHDC2与其含m6A的底物之间的相互作用来促进RNA的结合[10],在蛋白质寡聚化过程中起到作用[11, 12]。Helicase结构域包括Helicase N和Helicase C功能区,具有ATP依赖的RNA解旋酶功能,5’-3’核糖核酸外切酶XRN1的相互作用由Helicase结构域中包含的锚蛋白重复序列介导,提示YTHDC2具有调控mRNA稳定性的功能[10, 11]。YTHDF2通过招募TATA(CCR4-NOT)复合体导致含有m6A的RNA处于不稳定状态,加速mRNA的降解过程[12]。Kretschmer等[10]的研究表明,YTHDC2于核周空间富集,与小核糖体亚单位相互作用,提高翻译效率。其他研究表明,YTHDC2可能与胰腺癌易感性相关[6],在肝脏中有助于降低靶mRNA的稳定性,并以m6A依赖的方式抑制基因表达[13],YTHDC2的表达下调可能会导致肺癌细胞的增殖和迁移[14]。
目前YTHDC2在结直肠癌中的相关研究较少,我们通过GSEA富集分析发现,YTHDC2与结直肠癌MAPK信号通路有关,参与调控内源性凋亡信号通路、外源性凋亡信号通路和细胞周期阻滞等生物学过程;p38MAPK是MAPK信号通路的关键组成部分,磷酸化的p38MAPK在细胞增殖、分化、迁移、凋亡和死亡过程中起着重要的调控作用。通过Western blot检测各组细胞中p38MAPK和p-p38MAPK蛋白表达水平的变化,观察过表达或敲低YTHDC2后p38MAPK信号通路激活情况,结果显示,过表达或敲低YTHDC2后,p-p38MAPK蛋白表达水平与YTHDC2表达量呈正相关,流式细胞术结果显示,随YTHDC2表达量的增加,结直肠癌细胞凋亡比例也随之上升,划痕实验结果显示,过表达YTHDC2之后细胞增殖速度较慢,且凋亡比例增加,表明YTHDC2通过p38MAPK信号通路推动结直肠癌细胞凋亡。
本研究发现,YTHDC2的表达水平与结直肠癌的总生存率呈正相关,与肿瘤分期呈负相关。YTHDC2的过表达导致HCT116和Caco2细胞的凋亡比例上升,并降低结直肠癌细胞的增殖速度。YTHDC2可以抑制肿瘤细胞的增殖、转移和侵袭能力,改善结直肠癌的预后。然而,这与Tanabe等[15]的研究结果不同,他们认为YTHDC2可能通过促进缺氧诱导因子-1α(HIF-1α)的翻译增强结直肠癌转移能力,而HIF-1α的表达与肿瘤分期呈正相关,这种差异可能是YTHDC2的作用靶点不同导致的,提示YTHDC2在结直肠癌增殖凋亡方面可能存在双向调节能力,具体机制尚待进一步深入研究。
综上所述,YTHDC2过表达可以通过调控p38MAPK信号通路促进结直肠癌细胞的凋亡,改善结直肠癌患者的预后,YTHDC2调控细胞凋亡是通过激活外源性死亡受体和内源性线粒体凋亡途径实现的,深入研究YTHDC2介导细胞凋亡的机制,可能为开发治疗结直肠癌的新策略提供依据。
[1]
[2]
[3]
[4]
[5]
[6]
[7]
[8]
[9]
[10]
[11]
[12]
[13]
[14]
[15]
收藏此内容
推荐给朋友