牙根吸收是正畸治疗常见并发症,严重者可引起牙齿松动甚至脱落。目前,影像学技术仍是牙根吸收的主要诊断手段[1,2],但其辐射损伤、诊断滞后的缺陷可增加正畸患者的痛苦和正畸治疗的风险[3]。无创性生化诊断是近年学者研究牙根吸收诊断方法的新方向,主要通过酶联免疫吸附测定(enzyme-linked immunosorbent assay,ELISA)无创性提取检测龈沟液中牙根吸收特异性蛋白——牙本质涎磷蛋白(dentin sialophosphoprotein,DSPP)含量变化,间接诊断牙根吸收[4,5,6,7]。电化学ELISA将ELISA与电化学分析结合,具有免疫分析的高特异性和电化学的高灵敏度[8],非常适用于少量样品的分析,且不易受溶血、浑浊等因素干扰,已经用于人血清中癌胚抗原、甲胎蛋白、乙型肝炎E抗体等抗原抗体的检测[9,10,11,12,13,14]。
本项研究建立四甲基联苯胺(tetramethylbenzidine,TMB)-过氧化氢(hydeogen peroxide,H2O2)-辣根过氧化物酶(horse radish peroxidase,HRP)电化学ELISA检测体系,检测DSPP标准样品的电流反应信号并绘制质量浓度-电流标准工作曲线图,在此基础上测定患者龈沟液中DSPP含量,为电化学ELISA方法应用于正畸牙根吸收诊断提供理论依据。
本项研究获得首都医科大学北京口腔医学院伦理委员会审查批准[北京口腔(2014)伦审第(18)号]。
选择2012年1月至2014年12月就诊于首都医科大学口腔医学院正畸科的患者20例,女性12例,男性8例,年龄13~ 24岁,错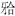 畸形类型不限,为接受治疗8~ 12个月的治疗中患者。纳入标准:患者双侧上颌中切牙口腔卫生良好,无牙周疾病,无探针出血,无龋齿,无系统性疾病。患者均知情同意。
畸形类型不限,为接受治疗8~ 12个月的治疗中患者。纳入标准:患者双侧上颌中切牙口腔卫生良好,无牙周疾病,无探针出血,无龋齿,无系统性疾病。患者均知情同意。
提取患者上颌双侧中切牙龈沟液。具体方法:冲洗、吹干患者上颌双侧中切牙,使用棉卷隔湿。使用吸潮纸尖(天津中津生物技术有限公司)分别从牙齿的近中及远中提取龈沟液。将吸潮纸尖插入龈沟内1~ 2 mm,静置30 s,同样过程1 min后重复,共获得160个样本(每名患者8个样本),取样前后使用分析天平测定吸潮纸尖重量变化。提取龈沟液后,将吸潮纸尖置于离心试管中,加入磷酸盐缓冲溶液(phosphate buffer saline,PBS)(包含蛋白酶抗氧化剂,即0.1 ml苯甲基磺酰氟100 μl),离心5 min(转速150 00 r/min,离心半径为13.5 cm),提取上层溶液,重复离心1次。将两次离心的提取液混合,约200 μl,将同一位置前后两次提取的样本混合,存储于-20 ℃冰箱内,最终共获得80份样本(每例患者4份样本)。
每份样品分别使用电化学ELISA、分光光度ELISA检测龈沟液中DSPP含量。
(1)电化学ELISA检测患者龈沟液中DSPP含量:与传统ELISA类似,首先建立电化学ELISA质量浓度-电流信号标准工作曲线,在该浓度范围内,样品反应电流与质量浓度间呈线性关系。基于同样体系测试患者龈沟液样品反应信号强度,并依据线性范围工作曲线读取患者样品中DSPP质量浓度。具体方法:先将标准人DSPP在小试管中倍比稀释,向预先包被了DSPP单克隆抗体的酶标孔中加入质量浓度分别为0、25、50、100、200、400、800 ng/L的DSPP标准品和生物素标志的抗DSPP抗体混合溶液50 μl,链霉亲和素标志的HRP溶液50 μl,37 ℃下温育60 min后用含0.05% Tween-20的0.02%PBS洗涤5次,去除未结合的标志酶,再向酶标板中加入底物溶液200 μl(底物溶液配制方法:于10 ml比色管中依次加入4.0×10-3 mol/L TMB溶液0.2 ml, 1.0×10-2 mol/L H2O2溶液1.0 ml, 0.2 mol/L pH为6.0的磷酸-醋酸-硼酸缓冲溶液5.0 ml,稀释至刻度并混合均匀),在37 ℃反应30 min进行酶催化反应,反应后向每个酶标孔中加入50 μl 0.2 mol/L pH 5.0磷酸-醋酸-硼酸缓冲液作为终止液,将JP-303极谱分析仪(成都仪器厂)的微型三电极系统直接插入酶标孔中检测产物,在一定浓度范围内检测电流信号强度与DSPP质量浓度呈线性关系,绘制DSPP电化学ELISA的线性回归方程,获得并建立DSPP电化学ELISA标准工作曲线,由此可测定患者龈沟液样品中DSPP准确含量。以上过程以HRP为标志酶,TMB作为反应底物,该底物被H2O2氧化形成具有电活性的产物。在最佳反应条件下,TMB-H2O2-HRP系统与ELISA反应结合,进而用于龈沟液中DSPP的检测。
(2)分光光度ELISA检测相同样本中DSPP含量:采用同样TMB底物体系的分光光度ELSA进行对比验证。使用成熟的DSPP商品ELISA检测试剂盒(上海晶天生物科技有限公司),首先建立分光光度ELISA质量浓度-吸光度信号标准工作曲线,在该浓度范围内,样品测试吸光度与质量浓度间呈线性关系。具体操作方法:先将标准人DSPP在小试管中倍比稀释,向预先包被了DSPP单克隆抗体的酶标孔中加入质量浓度分别为0、25、50、100、500、1 000、1 500 ng/L的DSPP标准品和生物素标志抗DSPP抗体混合溶液50 μl以及HRP溶液50 μl,37 ℃恒温孵育60 min,充分洗涤酶标板,加入TMB底物溶液200 μl,避光反应30 min后加入终止液50 μl,于420 nm波长处测量吸光度值(A值)。绘制DSPP分光光度ELISA的线性回归方程,获得并建立DSPP分光光度ELISA标准工作曲线,由此用分光光度测定患者相同龈沟液样品中DSPP含量。
使用SPSS 13.0统计学软件,检测数据非正态分布,故用"中位数(四分位数间距)"形式表达数据,并对电化学ELISA和分光光度ELISA检测的龈沟液中DSPP含量进行配对秩和检验,检验水准为双侧α=0.05.
电化学ELISA检测标准DSPP的线性回归方程为Ip?(μA)=0.015 0+2.59×10-5C(ng/L)(n=7,r=1.000,P <0.001),方程中Ip?为电化学ELISA检测信号峰值电流,C为DSPP样品质量浓度(图1),根据方程可知基于TMB底物体系的电化学ELISA测定DSPP线性范围为0.25~ 800.00 ng/L,检测下限为0.25 ng/L。分光光度ELISA检测标准DSPP的线性回归方程为A=0.003 3+ 10.26×10-6C(ng/L)(n=7,r=0.973,P<0.001),方程中A为吸光度值,C为样品质量浓度,其线性范围为5~1 500 ng/L,检测下限为5 ng/L。

电化学ELISA检测的DSPP质量浓度范围为314~671 ng/L,分光光度ELISA为308~645 ng/L;电化学ELISA的DSPP质量浓度[478(317)ng/L]与分光光度ELISA[486(308)ng/L]间差异无统计学意义(Z=-2.023,P=0.063)。
本项研究结果显示,电化学ELISA检测的DSPP质量浓度与分光光度ELISA间差异无统计学意义。就灵敏度而言,电化学ELISA的检测下限为0.25 ng/L,基于同样TMB显色底物体系的分光光度ELISA方法的检测下限为5 ng/L,因此,电化学ELISA在检测痕量DSPP时有更大的优势,更加适合小样本检测[9]。
分光光度反应依靠反应体系吸光度的变化实现待测物质含量的精确测定,例如浑浊、杂质等对光吸收产生影响的因素均可对分光光度造成误差。与分光光度相比,电化学ELISA有免疫反应的特异性和电化学分析的敏感性,其反应机制是特异性待测样品在电极表面发生电化学反应产生瞬间电流[9,10,11,12,13,14]。所产生电化学反应电流信号不受反应物颜色、入射光强弱、样本浑浊程度等因素影响,在患者体液中DSPP含量测试过程中抗干扰能力强,精确度好,更适用于临床患者DSPP含量的快速测定。
正畸牙根吸收是正畸治疗常见的并发症,明确诊断可帮助医师尽快改变矫治方案,从而防止牙根吸收的进一步发展[15,16]。正畸医师通常使用影像学方法诊断牙根吸收,存在明显的滞后性[17]。目前,学者已认可DSPP是诊断牙根吸收的特异性蛋白[18],使用分光光度ELISA检测DSPP浓度在临床上已有应用,本项研究显示,电化学ELISA是检测龈沟液中DSPP含量的新方法,可及时发现DSPP的微弱变化并实现对牙根吸收的实时监控。该方法无创,适合连续、系统地监测正畸牙根吸收进展,尤其适合龈沟液中痕量DSPP的精确检测,较传统ELISA更适用于牙根吸收的早期诊断。
总之,电化学ELISA是检测牙根吸收标志蛋白DSPP的一种可行、可靠并且灵敏的方法,其有助于对正畸牙根吸收进行连续纵向的观察进而揭示牙根吸收的病因。另外,该技术还可用于其他微量生物样本的检测。

探讨电化学酶联免疫吸附测定(enzyme-linked immunosorbent assay,ELISA)检测正畸患者龈沟液中牙根吸收标志性蛋白牙本质涎磷蛋白(dentin sialophosphoprotein, DSPP)含量的可行性。
使用线性回归方程建立电化学ELISA和分光光度ELISA检测标准DSPP的曲线图。选取于首都医科大学口腔医学院正畸科就诊的患者20例,提取上颌双侧中切牙龈沟液,分别使用电化学ELISA、分光光度ELISA检测DSPP含量,并使用配对秩和检验比较两种方法精确性的差异。
电化学ELISA检测标准DSPP,线性范围为0.25~ 800.00 ng/L,检测下限为0.25 ng/L,灵敏度明显优于分光光度ELISA(线性范围为5~1 500 ng/L,检测下限为5 ng/L)。两种方法检测的正畸患者龈沟液DSPP质量浓度差异无统计学意义(P=0.063)。
电化学ELISA能更灵敏地检测龈沟液中DSPP含量。