神经重症患者胃液pH值监测与医院获得性肺炎的相关性
2016年11月
中华神经科杂志,第49卷第11期 第864页-第868页
马晨,卫婧雅,惠博,朱继文,郑鑫,康涛,康晓刚,杨方,江文
神经系统危重症常并发医院获得性肺炎(HAP),是患者病情加重、预后不良的重要因素。其发生率可达11.7%~30.9%,病死率为10.4%~35.3%[1,2]。 2004年一项大样本研究发现,与安慰剂相比,质子泵抑制剂可增加社区获得性肺炎(CAP)风险[3]。2009年一项前瞻性队列研究(63 878例非机械通气患者)显示,使用质子泵抑制剂可使HAP发生率增加30%[4]。研究表明,留置胃管可引起胃食管反流,增加误吸性肺炎的发生[5]。神经重症患者多伴有吞咽障碍,需管饲饮食、持续的肠内营养以及预防性应用抑酸剂等,这些因素均可造成胃液pH值增高,但目前神经重症患者胃液pH值与HAP的相关性鲜有报道。鉴于此,我们拟前瞻性动态监测神经重症患者胃液pH值,观察其变化与HAP的相关性,胃腔菌群定植对HAP病原学的影响,从而指导胃液pH值的合理调控,为防治神经重症患者并发HAP提供理论基础。
为2014年10月1日到2015年5月1日于第四军医大学西京医院神经内科重症监护病房住院的连续性接受管饲饮食的神经重症患者,根据住院期间有无新的HAP分为感染组和无感染的对照组。纳入标准:(1)男女不限;(2)意识障碍、昏迷和神经危重症疾病不能经口进食者;(3)吞咽困难和失去咀嚼能力者。排除标准:(1)合并消化道出血或手术部位在上消化道者;(2)严重的肝肾功能障碍或消化道溃疡;(3)孕妇及哺乳期妇女;(4)拔除胃管患者。
新发肺炎即入院≥48 h在医院内发生的肺炎,痰液标本中分离出新的细菌,浓度在105 CFU/ml,且伴有新出现的或进展性肺部浸润病变,可同时出现发热、脓性痰、血象改变等。HAP、呼吸机相关性肺炎(VAP)诊断标准参照2005年美国《成人医院获得性、呼吸机相关性和卫生保健相关性肺炎指南》[6]。
符合纳入标准和排除标准患者均在知情同意后于入院后24 h内留置鼻胃管,于监测前一晚00:00时后停止管饲,并冲洗胃管,次日07:00时测定空腹胃液pH值,管饲喂养后,分别于10:00、15:00时停止管饲并冲洗管道,1 h后测定餐后胃液pH。清晨及餐后同时同点采集胃液、口咽部及上呼吸道标本,行细菌培养、药敏检测,胃液标本用20 ml注射器从胃管抽吸,取样后置灭菌采样瓶。口咽部标本用咽拭子在咽后壁或悬雍垂的后侧采集,上呼吸道标本通过灭菌吸痰管,经人工气道吸引采集上呼吸道分泌物。胃液标本在接种的同时行pH值测定。如出现下列任何一项情况时即终止采样:①新发肺炎;②拔出胃管;③出院;④死亡。
统计分析使用SPSS 18.0统计软件,均为双侧检验,以P<0.05提示差异有统计学意义。计数资料组间比较采用χ2检验,当四格表中理论频数小于5时,使用连续校正公式,当理论频数小于1时,使用Fisher精确概率法。正态分布的计量资料以均数±标准差(
共有72例患者入组,以住院期间出现新的HAP患者为新发感染组即感染组,共40例(男31例,女9例),年龄14~81岁,平均(50.5±19.1)岁。未新发HAP患者为无新发感染组即对照组,共32例(男18例,女14例),年龄14~83岁,平均(50.9±18.9)岁。两组患者人口学特征、既往病史、实验室指标等分布相近,差异无统计学意义。基线时格拉斯哥昏迷评分(Glasgow Coma Score,GCS)、急性生理与慢性健康评分(Acute Physiology and Chronic Health Evaluation,APECHE-Ⅱ)差异无统计学意义,住院期间,两组患者预防性应用抑酸药物、呼吸机支持情况比较,差异无统计学意义(

见
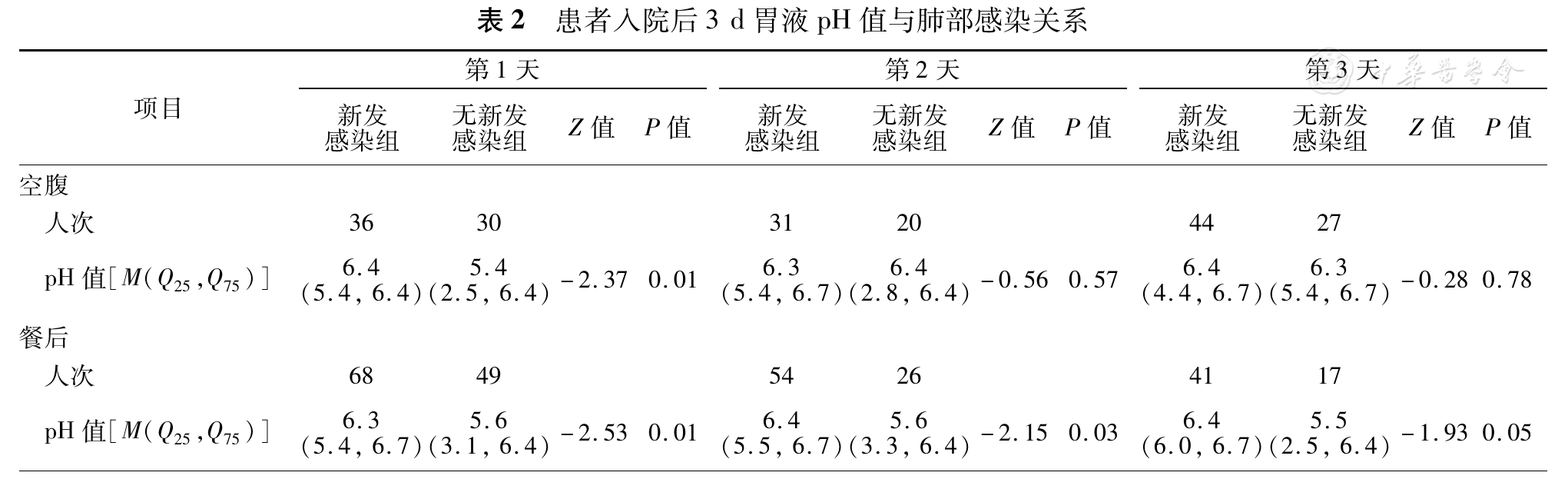
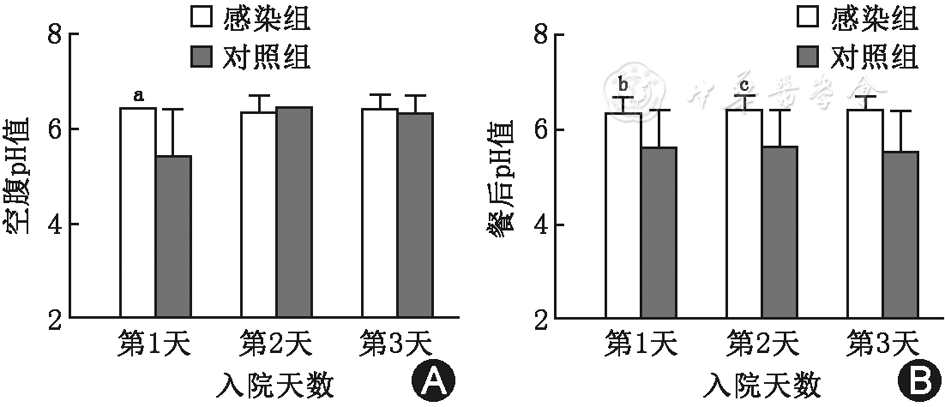
与对照组比较,aZ=-2.37, P<0.05,bZ=-2.53, P=0.01, cZ=-2.15, P=0.03
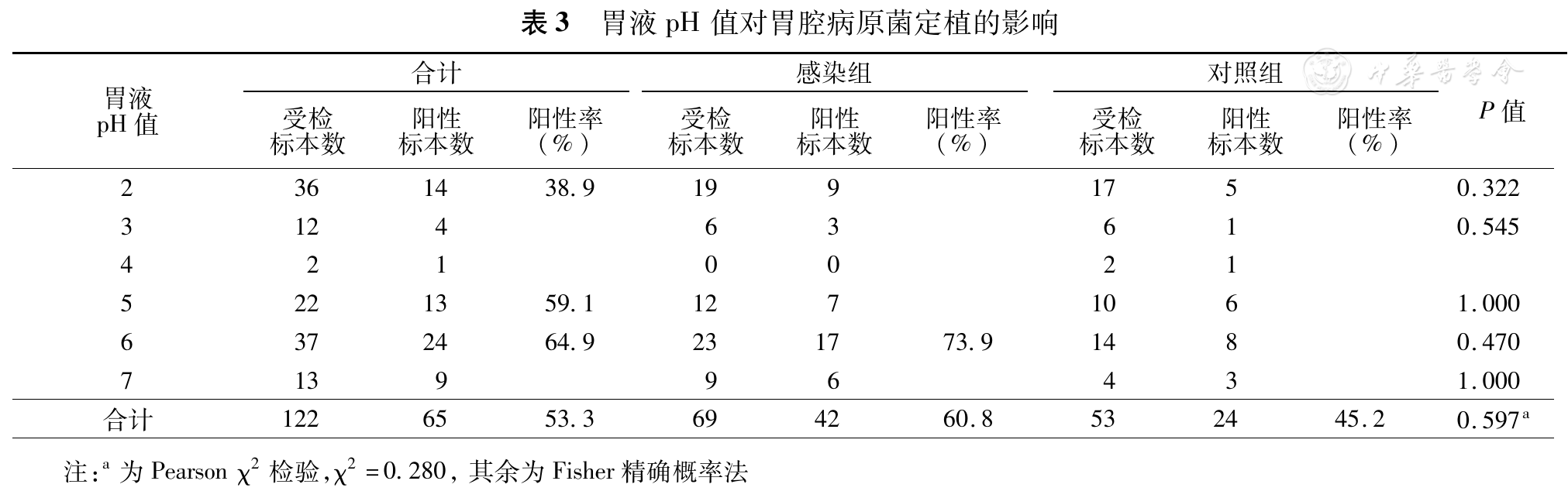
pH值对两组病原体定植的影响是类似的,感染组胃腔总的病原体定植率(60.8%)高于对照组(45.2%;χ2 =0.28, P=0.597),但差异无统计学意义。
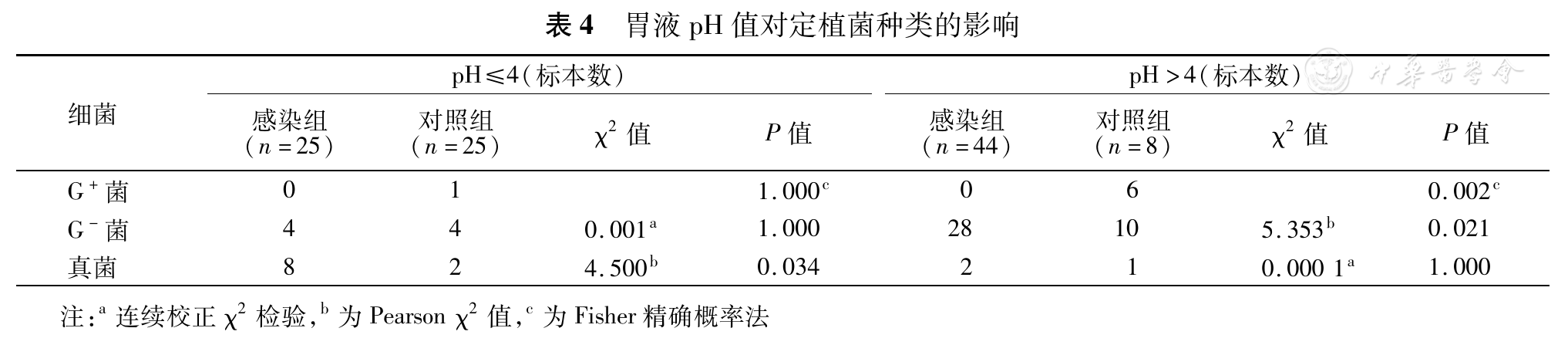
胃液pH值影响胃腔定植菌种类,胃液pH>4时,胃腔内革兰阴性杆菌分离率明显上升,感染组高于对照组。
感染组胃腔与口咽部定植菌种类的比较见
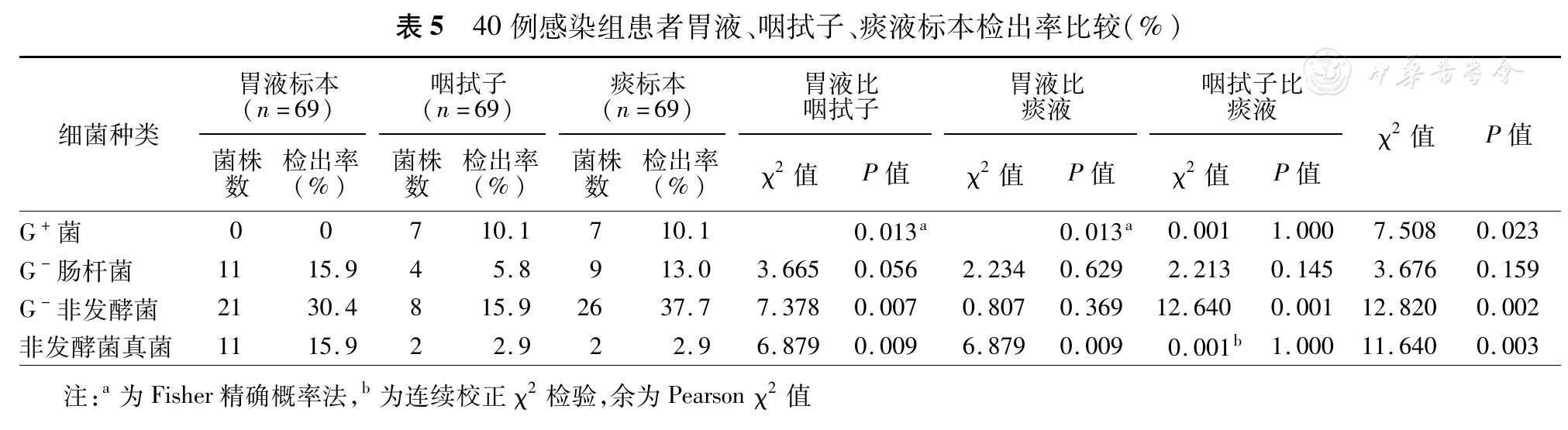
近10余年来,关于胃腔定植、胃液pH值、病原菌易位在HAP中的作用研究较多。众所周知,胃腔可接受包括外源性(胃管注入食物及口咽部分泌物)及内源性(十二指肠胃反流)的潜在病原微生物,正常情况下,非发酵菌(如铜绿假单胞菌、鲍曼不动杆菌)多源自周围环境,在胃肠道内罕见。当胃液pH值<3.5时,可抑制细菌定植,但胃液pH≥4时,微生物可在胃中繁殖至高浓度,使胃腔成为细菌的储存库[7]。
既往研究表明,抑酸药物通过改变胃肠道菌群使肺炎发生的风险增加[8]。Garvey等[9]发现碱化胃液可使胃腔内细菌及真菌增多。Daschner等[10]曾报道,当胃液pH<3.4时,VAP发生率40.6%,pH>5.0时,VAP发生率为69.2%,提示胃液pH对HAP的发生率有重要意义。危重患者机体内环境和胃液酸度可发生改变,高龄、病情危重者体内胃酸分泌减少,预防性使用抑酸药物、持续肠内喂养均可使胃液酸度降低[11]。且神经重症监护病房的患者多数存在意识障碍、球麻痹、肌无力、使用镇静药物等,均能使咳嗽反射减弱,增加误吸风险。此外,留置胃管可导致食管下端括约肌的持久松弛[12],胃内细菌逆行上移至咽,管饲喂养为胃腔定植提供培养基,均促进逆行感染的发生。2011年中国一项荟萃分析(17个队列研究)显示[13],神经疾病伴随吞咽障碍是HAP的危险因素。Segal等[14]对鼻饲饮食的老年人口咽部及胃液标本进行培养,发现胃液中革兰阴性菌及金黄色葡萄球菌分离的阳性率为74%,咽拭子为69%,提示口咽部及胃腔共同作为细菌的储存库,导致吸入性肺炎。遗憾的是,此试验未进行胃液pH检测。我们针对神经重症病房所有留置胃管的吞咽困难患者,采用1 d内多点检测胃液pH,结果发现,感染组胃液pH值有上升趋势,考虑到本试验样本量较少,提示今后仍需更大样本的研究来佐证这一结果。同时,我们发现,当胃液pH>4时,胃腔内革兰阴性杆菌分离率明显上升。这与国内学者马健等[15]、李华茵等[16]研究结果相似。另一方面,感染组中,通过动态比较同一患者的胃液、咽拭子、上呼吸道标本培养结果,我们发现胃腔中非发酵菌细菌多于口咽部,且40例患者中有7例上呼吸道病原菌与胃腔及口咽部培养菌群一致,推测存在胃腔至呼吸道的内源性感染途径。革兰阴性杆菌作为医院获得性肺炎最常见的病原体,占全部医院获得性肺炎的50%~80%。Johanson等[17]发现,革兰阴性杆菌在健康人咽部仅占6%,而重症患者口咽部检出率为73%,提示可能是造成HAP的重要途径。以往认为,口咽部定植致病菌来源于医院环境,但采取切断外源性传播或单纯口腔内涂布抗生素的措施并不能大幅降低VAP的发生。Price等[18]发现,选择性消化道净化与口咽局部使用氯己定相比,可降低重症监护病房患者病死率。有研究通过降低胃液pH来降低肺炎发生率来间接证明胃腔-肺部感染途径的存在,如Bonten等[19]发现间断肠内营养(18 h/d)与持续肠内营养(24 h/d)相比,患者可出现短暂的胃液pH减低,但VAP及胃腔细菌定植率两组无差别。Tulaimat等[20]发现使用山梨酸钾酸化管饲食物可减少机械通气患者胃内细菌定植,但未降低肺炎发生率。硫酸铝具有细胞保护[21]及抗菌作用[22],预防应激性溃疡同时不增高pH,可减低VAP发生率。
由于病情的严重及复杂性,大部分患者入住神经重症监护病房时已存在肺部感染,我们的试验以是否出现新发感染作为观察事件,最终发现,神经重症患者多存在胃液pH值增高,使胃腔定植菌增加,可能是引起内源性感染的重要因素。可以想象,病原菌误吸及咽下、胃腔定植均可造成感染反复,迁延不愈,如长期使用抗菌药物,导致细菌耐药性增强,易产生多重耐药菌。总之,调控合适的胃液pH,为我们在神经重症病房长期与感染的抗衡中,提供了预防及治疗的依据。
[1] Upadya A, Thorevska N, Sena KN, et al. Predictors and consequences of pneumonia in critically ill patients with stroke[J]. J Crit Care, 2004, 19(1):16-22.
[2] Dettenkofer M, Ebner W, Els T, et al. Surveillance of nosocomial infections in a neurology intensive care unit[J]. J Neurol, 2001, 248(11):959-964.
[3] Laheij RJ, Sturkenboom MC, Hassing RJ, et al. Risk of community-acquired pneumonia and use of gastric acid-suppressive drugs[J]. JAMA, 2004, 292(16):1955-1960.
[4] Herzig SJ, Howell MD, Ngo LH, et al. Acid-suppressive medication use and the risk for hospital-acquired pneumonia[J]. JAMA, 2009, 301(20):2120-2128.
[5] Mital RK, Stewart WR, Schirmer BD. Effect of a catheter in the pharynx on transient lower esophageal sphincter relaxations[J]. Gastroenterology, 1992, 103(4):1236-1240.
[6] American Thoracic Society, Infectious Diseases Society of America. Guidelines for the management of adults with hospital-acquired, ventilator-associated, and healthcare-associated pneumonia[J]. Am J Respir Crit Care Med, 2005, 171(4):388-416.
[7] Daschner F, Kappstein I, Engels I, et al. Stress ulcer prophylaxis and ventilation pneumonia: prevention by antibacterial cytoprotective agents?[J]. Infect Control Hospital Epidemiol, 1988, 9(2):59-65.
[8] Vakil N. Acid inhibition and infections outside the gastrointestinal tract[J]. Am J Gastroenterol, 2009, 104
[9] Garvey BM, McCambley JA, Tuxen DV. Effects of gastric alkalization on bacterial colonization in critically ill patients[J]. Crit Care Med, 1989, 17(3):211-216.
[10] Daschner F, Reuschenbach K, Pfisterer J, et al. The effect of stress ulcer prevention on the incidence of pneumonia in artificial respiration[J]. Anaesthesist, 1987, 36(1):9-18.
[11] Spilker CA, Hinthorn DR, Pingleton SK. Intermittent enteral feeding in mechanically ventilated patients: the effect on gastric pH and gastric cultures[J]. Chest, 1996, 110(1):243-248.
[12] Gomes GF, Pisani JC, Macedo ED, et al. The nasogastric feeding tube as a risk factor for aspiration and aspiration pneumonia[J]. Curr Opin Clin Nutr Metab Care, 2003, 6(3):327-333.
[13] 赵航,赵丛海,李桂杰, 等. 神经外科系统疾病合并医院获得性肺炎危险因素荟萃分析[J]. 中华医院感染学杂志, 2011, 21(16):3352-3354.
[14] Segal R, Pogoreliuk I, Dan M, et al. Gastric microbiota in elderly patients fed via nasogastric tubes for prolonged periods[J]. J Hosp Infect, 2006, 63(1):79-83.
[15] 马健,胡必杰,何礼贤. 胃腔定植菌在医院内肺炎患者发病机制中的作用[J]. 中华结核和呼吸杂志, 1999, 22(2):104-107.
[16] 李华茵,何礼贤,胡必杰, 等. 胃腔定植菌在机械通气相关性肺炎发病机制中的作用[J]. 中华内科杂志, 2004, 43(2):112-116.
[17] Johanson WG, Pierce AK, Sanford JP, et al. Changing Pharyngeal Bacterial Flora of Hospitalized Patients. Emergence of gram-negative bacilli[J]. N Engl J Med, 1969, 281(21):1137-1140.
[18] Price R, Maclennan G, Glen J, et al. Selective digestive or oropharyngeal decontamination and topical oropharyngeal chlorhexidine for prevention of death in general intensive care: systematic review and network meta-analysis[J]. BMJ, 2014, 31(348):g2197.
[19] Bonten MJ, Gaillard CA, van der Hulst R, et al. Intermittent enteral feeding:the influence on respiratory and digestive tract colonization in mechanically ventilated intensive-care-unit patients[J]. Am J Respir Crit Care Med, 1996, 154(2
[20] Tulaimat A, Laghi F, Mikrut K, et al. Potassium sorbate reduces gastric colonization in patients receiving mechanical ventilation[J]. J Crit Care, 2005, 20(3):281-287.
[21] Pilchman J, Lefton HB, Braden GL. Cytoprotection and stress ulceration[J]. Med Clin North Am, 1991, 75(4):853-863.
[22] Tryba M, Mantey-Stiers F. Antibacterial activity of sucralfate in human gastric juice[J]. Am J Med, 1987, 83(3B):125-127.
