中性粒细胞胞外诱捕网在血栓形成中发挥重要作用
2020年8月
中华神经科杂志,第43卷第8期 第763页-第767页
刘蕾,吴俊
2004年,Brinkmann等[1]首次发现中性粒细胞在吞噬病原体时,抗菌颗粒与吞噬体结合,刺激中性粒细胞释放一种颗粒蛋白和染色质组成的纤维网状结构,降解毒性因子并杀死细菌,这种结构被称为中性粒细胞胞外诱捕网(neutrophil extracellular traps,NET)。NET的网状结构由DNA链支架、组蛋白和其他修饰分子构成,包括弹性蛋白酶、髓过氧化物酶、杀菌通透性增强蛋白、组织蛋白酶G和其他具有抗菌作用的蛋白酶组成[1,2]。在高分辨率扫描电子显微镜下显示,NET包含直径为15~17 nm的平滑拉伸段和直径约25 nm的球形结构域,这些结构聚集成直径最大为50 nm的螺纹结构。透射电子显微镜检测发现,NET没有被膜包被[1]。未固定的、完全水合的NET外观呈云雾状,占据的空间比其来源的细胞体积大10~15倍,反映出当空间足够时它们在体内的形态[3]。
血栓形成和血栓栓塞两种病理过程所引起的疾病,临床上称为血栓性疾病。血栓性疾病严重威胁人类的生命健康,近年来,大量研究发现NET在多种疾病血栓形成中发挥着作用。
NET的形成不同于凋亡和坏死,细胞凋亡时染色质凝结和核碎裂而没有核被膜破裂以及胞质空泡化,细胞坏死时核膜保持完整。而NET形成时中性粒细胞核膜分解成大量囊泡,胞核失去了原有形态且常染色质和异染色质融合,胞质颗粒膜裂解,核内物质与颗粒内容物接触,NET的各成分之间相互混合,最后细胞质内的细胞器消失,细胞膜破裂并释放NET结构[4]。中性粒细胞产生NET网状结构的细胞死亡过程被称为NETosis[5,6]。
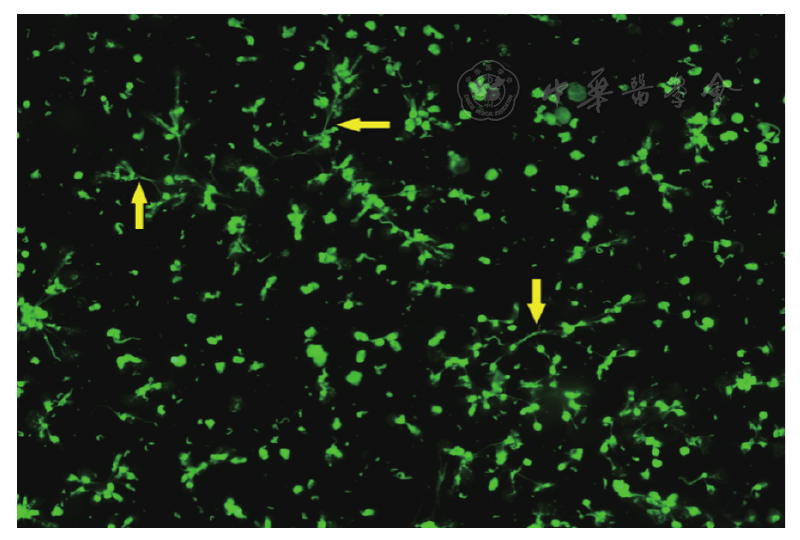
研究者对NET产生的条件和机制进行了一系列的研究,发现NET的产生依赖于还原型辅酶Ⅱ氧化酶的活性和活性氧的产生[2]。在体内,IL-8、脂多糖、细菌、真菌或激活的血小板都可以刺激中性粒细胞产生NET,在体外,十四烷酰佛波醇乙酸酯(
静脉血栓栓塞(venous thromboembolism,VTE)是住院患者致残和致死的主要原因之一,具有较高的发病率和死亡率,准确诊断和及时治疗可有效降低死亡率[10]。在狒狒髂静脉球囊置管深静脉血栓模型中,NET与血栓中的纤维蛋白链紧密联系相互作用,从而潜在地影响血栓结构稳定性[11]。在小鼠下腔静脉狭窄血栓形成模型中,NET存在于红色血栓部分,为血小板和红细胞提供血栓支架[11,12,13]。除了动物实验,大量体外实验表明,NET通过黏附和激活血小板,激活Ⅻ,促进凝血酶的生成而直接或间接的促进血栓的形成[14,15,16,17,18]。最新的研究还发现NET的组成成分H4和DNA可促进肝细胞核因子4αmRNA表达增加,具有直接或间接促进凝血因子形成的作用;在THP-1细胞中,H4可引起TF mRNA的增加,miR-17/92中microRNA(miRNA/miRs)的减少,这可能一定程度上解释了TF表达的增加;在HepG2细胞中,DNA和H4显著上调了凝血级联反应至关重要的凝血因子Ⅶ和Ⅻ的mRNA水平以及丝氨酸蛋白酶抑制剂家族F的成员2(编码α2-抗纤溶酶)的水平[19]。通过这些研究发现,NET可能是血栓形成的一个新的机制[20],也为VTE的诊断提供了一个新的方向。
癌症患者发生VTE的风险很高[21]。癌细胞的增殖和转移使血液呈高凝状态,提高了TF的表达和凝血酶的生成,是癌症相关血栓形成的起始因素[22],进一步活化血小板,促进NET的产生,而促进血栓的形成[23]。从胰腺癌和胃癌患者血液中分离中性粒细胞,可以快速的诱导NET的形成,通过NET可增强健康人血浆凝血酶和纤维蛋白的生成[24]。NET在癌症相关血栓形成中的作用也得到了动物实验的证实,在慢性粒细胞性白血病的小鼠模型中,恶性和正常的中性粒细胞都更容易形成NET,在乳腺癌[25]和肺癌模型中也观察到中性粒细胞产生NET的敏感性增加,癌症通过诱导外周血中性粒细胞的增加,而诱导NET形成的增加,并且,在乳腺癌晚期模型中,NET的形成过程与肺静脉血栓的形成同时发生,表明NET与癌症相关的血栓形成密切相关[26]。研究发现,肿瘤细胞在血液中释放多种细胞因子,例如,中粒细胞集落刺激因子,可以促进中性粒细胞数量的增加并诱导活化产生NET,在肿瘤小鼠模型中确证了这一过程,并最终导致小鼠的血小板减少和微血栓形成[27]。一项大型的临床研究发现NET可以作为一种生物标志物预测癌症患者VTE的风险[28]。
脓毒症是感染引起的全身炎症反应综合征[29]。脓毒症患者多表现为凝血系统激活、进行性血栓形成前状态,抗凝系统的失调可能导致弥散性血管内凝血[30],微血管血栓形成、低灌注,最终发展为多器官功能障碍综合征和死亡[31]。脓毒症患者体内细菌脱落大量的脂多糖,是激活中性粒细胞产生NET的重要物质[32],这可能是脓毒症NET形成的原因之一。血小板不仅参与凝血过程,在感染性疾病时还发挥着诱导炎症和抗感染的作用[33]。脓毒症时活化的血小板可以直接隔离或杀死病原体,或通过激活巨噬细胞和中性粒细胞促进病原体清除,特定受体TLR4被激活促进NET的形成,最终血小板聚集和微血栓形成[34]。从脓毒症患者血液中分离的中性粒细胞可以通过NET释放组织因子,这种形式的TF可诱导体外凝血酶生成,在脓毒症凝血系统的激活中起关键作用[35]。脓毒症患者血液中分离的血浆和血小板在体外能够诱导中性粒细胞释放NET,并且与健康对照组相比,脓毒症患者的中性粒细胞产生的NET具有很好的促凝活性[36]。McDonald等[13]的研究中,使用多色共聚焦活体显微镜检查脓毒症小鼠,观察到无论是否有细菌刺激,体内血小板聚集、凝血酶激活和纤维蛋白凝块形成过程中均有大量NET参与其中,NET对脓毒症诱导的血管内凝血的发生是至关重要的。实时灌注成像显示,阻滞NET诱导的凝血显著改善了微血管灌注,这与脓毒症小鼠全身血管内凝血和终末器官损害的标志物减少有关[13]。NET通过与血小板的相互作用在脓毒症患者的血栓形成中发挥着重要的作用。
免疫性血栓形成是指血管内,尤其是微血管内的血栓形成诱导的先天免疫应答[37]。免疫血栓形成得到免疫细胞和特定的血栓形成相关分子的支持,并产生有助于识别,遏制和破坏病原体的血管内支架,从而保护机体不被病原体损伤[38]。中性粒细胞通过免疫应答过程的细胞特异性机制来增强血栓形成,激活后产生的NET不仅具有抗菌能力,还具有诱导促凝血反应的功能[39]。NET在多方面促进血栓形成,是免疫血栓形成的关键因素[10,40]。微血管血栓性疾病主要包括溶血尿毒综合征和血栓性血小板减少性紫癜(thrombotic thrombocytopenic purpura,TTP),统称为血栓性微血管病(thrombotic microangiopathy,TMA)[41]。在溶血尿毒综合征中,NET除了发挥促进炎症反应和抗菌作用外,还促进了微血管血栓形成,从而导致患者肾功能衰竭[42,43]。在移植相关的研究中,NET水平的升高,发生移植相关TMA的风险显著增加[44],这可能是由于TMA患者血浆中缺乏可以降解NET的DNase 1[45]。ADAMTS13是一种血浆金属蛋白酶,可以裂解血管性血友病因子,是诊断TTP的关键酶[46]。最近的研究中使用外源性重组人ADAMTS13和DNase 1处理的小鼠,体内NET的产生明显减少,证明ADAMTS13可能抑制了NET的形成,DNase 1可降解NET结构[47]。TTP的发生是由于ADAMTS13的缺乏,NET是否与TTP的微血栓形成有关值得探究。
在自身免疫性疾病中NET可促进抗中性粒细胞胞浆抗体相关血管炎相关血栓的形成,NET的形成与系统性红斑狼疮的活动性有关,并且NET可损伤和杀死内皮细胞,促进动脉粥样硬化斑块的炎症反应,从而加速系统性红斑狼疮的动脉粥样硬化[48]。抗磷脂抗体可以刺激中性粒细胞产生NET,这与抗磷脂抗体综合征患者血栓形成密切相关[49]。
补体系统是由血浆和细胞表面30多种蛋白质组成的先天性免疫系统的一部分,是抗体介导免疫的主要效应机制之一。中性粒细胞被激活后可释放补体因子P、补体因子B和C3等补体成分,其中CFP沉积在NET和细菌上,诱导攻膜复合物C5b-9的形成[50]。在一项抗磷脂抗体诱导血栓形成的小鼠实验中,补体成分C3基因敲除(C3-/-)和C5基因敲除(C5-/-)的小鼠血栓形成明显受到抑制,表明补体激活在抗磷脂抗体诱导的血栓形成中起着重要的作用[51]。另一个小鼠实验中,补体C5促进了与组蛋白诱导的致死性血栓形成相关的肝损伤[52]。
补体与血小板之间也存在着相互作用,表现为Ⅴa因子通过与补体攻膜复合物C5b-9诱导的结合位点结合,促进其与Ⅹa因子结合,再与血小板表面功能性凝血酶原结合位点结合,最终激活血小板[53],这些研究为补体在血栓形成中的作用的研究提供了基础。在自发性小肠肿瘤模型(APCMin/-小鼠)中,肿瘤的发展与高凝状态都和中性粒细胞相关,尤其与低密度中性粒细胞的出现有关。低密度中性粒细胞具有促肿瘤中性粒细胞的明显特征,在补体C3a受体(C3aR)作用下与没有C3aR的作用对比得出,在C3aR作用下更易产生NET,导致小肠肿瘤的凝血激活,高凝状态和血栓形成[54]。多种细菌感染过程中补体在发挥调理作用的同时促进了NET的释放,并且补体CR1在这一过程中起主导作用,补体CR3起协助作用[55]。NET可以作为血栓形成和补体激活的直接支架,补体系统的调理作用和溶解活性增强了NET的抗菌性能。尽管NET、补体蛋白和凝血因子的作用过程不同,但仍可以在一个大的联合体内发挥作用,保护宿主免受出血和感染,这种合作并不局限于受伤部位,也发生在血流中,当这种平衡被打破,可能会出现严重的并发症,例如脓毒症、深静脉血栓、自身免疫性疾病甚至癌症[56]。NET与补体之间存在密切的关系,且两者都在血栓形成过程中发挥作用,三者在发挥作用上都有一定的联系,但具体的分工和是否存在反馈机制仍需要进一步研究。
自2004年首次发现NET以来,其在预防感染及杀灭细菌中的作用是重要且不可忽视的,而NET的产生也促进了血栓的形成,增加了静脉血栓栓塞的风险,如何正确评价NET在人体内的作用还需要更全面的评估。NET在血栓形成中的作用目前仍无法监测,如何预测血栓风险需要进一步研究。NET在病理血栓形成中的作用逐渐明确,为溶栓提供了新的方向,而NET对溶栓的影响尚不清楚。在多项研究中使用DNase 1裂解NET结构,均减少了血栓的形成[32,57],而什么时候应用DNase 1和用量仍需要进一步研究来确定一个标准。重组人ADAMTS13可以减少NET的形成[47],为NET相关的血栓形成的研究提供了一个新的思路。
[1] Brinkmann V, Reichard U, Goosmann C, et al. Neutrophil Extracellular Traps Kill Bacteria[J]. Science, 2004, 303(5663): 1532-1535.
[2] Stoiber W, Obermayer A, Steinbacher P, et al. The Role of Reactive Oxygen Species (ROS) in the Formation of Extracellular Traps (ETs) in Humans[J]. Biomolecules, 2015, 5(2): 702-723.
[3] Brinkmann V, Zychlinsky A. Neutrophil extracellular traps: is immunity the second function of chromatin?[J]. J Cell Biol, 2012, 198(5): 773-783.
[4] Fuchs TA, Abed U, Goosmann C, et al. Novel cell death program leads to neutrophil extracellular traps[J]. J Cell Biol, 2007, 176(2): 231-241.
[5] Steinberg BE, Grinstein S. Unconventional roles of the NADPH oxidase: signaling, ion homeostasis, and cell death[J]. Sci STKE, 2007, 2007(379): e11.
[6] Mesa MA, Vasquez G. NETosis[J]. Autoimmune Dis, 2013,b2013:
[7] Brinkmann V, Zychlinsky A. Beneficial suicide: why neutrophils die to make NET[J]. Nat Rev Microbiol, 2007, 5(8): 577-582.
[8] Li P, Li M, Lindberg MR, et al. PAD4 is essential for antibacterial innate immunity mediated by neutrophil extracellular traps[J]. J Exp Med, 2010, 207(9): 1853-1862.
[9] Wong SL, Wagner DD. Peptidylarginine deiminase 4: a nuclear button triggering neutrophil extracellular traps in inflammatory diseases and aging[J]. FASEB J, 2018: j201800691R.
[10] Olaf M, Cooney R. Deep Venous Thrombosis[J]. Emerg Med Clin North Am, 2017, 35(4): 743-770.
[11] Fuchs TA, Brill A, Duerschmied D, et al. Extracellular DNA traps promote thrombosis[J]. Proc Natl Acad Sci U S A, 2010, 107(36): 15880-15885.
[12] Brill A, Fuchs TA, Savchenko AS, et al. Neutrophil extracellular traps promote deep vein thrombosis in mice[J]. J Thromb Haemost, 2012,10(1):v136-144.
[13] McDonald B, Davis RP, Kim S, et al. Platelets and neutrophil extracellular traps collaborate to promote intravascular coagulation during sepsis in mice[J]. Blood, 2017, 129(10): 1357-1367.
[14] Gould TJ, Vu TT, Swystun LL, et al. Neutrophil extracellular traps promote thrombin generation through platelet-dependent and platelet-independent mechanisms[J]. Arterioscler Thromb Vasc Biol, 2014, 34(9): 1977-1984.
[15] Tripodi A, Ammollo CT, Semeraro F, et al. Hypercoagulability in patients with Cushing disease detected by thrombin generation assay is associated with increased levels of neutrophil extracellular trap-related factors[J]. Endocrine, 2017, 56(2): 298-307.
[16] Zucoloto AZ, Jenne CN. Platelet-Neutrophil Interplay: Insights Into Neutrophil Extracellular Trap (NET)-Driven Coagulation in Infection[J]. Front Cardiovasc Med, 2019, 6: 85.
[17] Borissoff JI, Ten CH. From neutrophil extracellular traps release to thrombosis: an overshooting host-defense mechanism?[J]. J Thromb Haemost, 2011, 9(9): 1791-1794.
[18] von Bruhl ML, Stark K, Steinhart A, et al. Monocytes, neutrophils, and platelets cooperate to initiate and propagate venous thrombosis in mice in vivo[J]. J Exp Med, 2012, 209(4): 819-835.
[19] Reyes-García AMDL, Aroca A, Arroyo AB, et al. Neutrophil extracellular trap components increase the expression of coagulation factors[J]. Biomed Rep, 2019, 10(3): 195-197.
[20] Th?lin C, Hisada Y, Lundstr?m S, et al. Neutrophil Extracellular Traps: Villains and Targets in Arterial, Venous, and Cancer-Associated Thrombosis [J]. Arterioscler Thromb Vasc Biol, 2019,39(9):1724-1738.
[21] Connolly GC, Francis CW. Cancer-associated thrombosis[J]. Hematology Am Soc Hematol Educ Program, 2013, 2013: 684-691.
[22] Mukai M, Oka T. Mechanism and management of cancer-associated thrombosis[J]. J Cardiol, 2018, 72(2): 89-93.
[23] Cedervall J, Hamidi A, Olsson A. Platelets, NET and cancer[J]. Thromb Res, 2018, 164: S148-S152.
[24] Thalin C, Hisada Y, Lundstrom S, et al. Neutrophil Extracellular Traps: Villains and Targets in Arterial, Venous, and Cancer-Associated Thrombosis[J]. Arterioscler Thromb Vasc Biol, 2019, 39(9): 1724-1738.
[25] Snoderly HT, Boone BA, Bennewitz MF. Neutrophil extracellular traps in breast cancer and beyond: current perspectives on NET stimuli, thrombosis and metastasis, and clinical utility for diagnosis and treatment[J]. Breast Cancer Res,2019,21(1):145.
[26] Demers M, Krause DS, Schatzberg D, et al. Cancers predispose neutrophils to release extracellular DNA traps that contribute to cancer-associated thrombosis[J]. Proc Natl Acad Sci U S A, 2012, 109(32): 13076-13081.
[27]
[28] Mauracher LM, Posch F, Martinod K, et al. Citrullinated histone H3, a biomarker of neutrophil extracellular trap formation, predicts the risk of venous thromboembolism in cancer patients[J]. J Thromb Haemost, 2018, 16(3): 508-518.
[29] Singer M, Deutschman CS, Seymour CW, et al. The Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3)[J]. JAMA, 2016, 315(8): 801-810.
[30] Semeraro N, Ammollo CT, Semeraro F, et al. Sepsis, thrombosis and organ dysfunction[J]. Thromb Res, 2012, 129(3): 290-295.
[31] Tsao CM, Ho ST, Wu CC. Coagulation abnormalities in sepsis[J]. Acta Anaesthesiol Taiwan, 2015, 53(1): 16-22.
[32] Clark SR, Ma AC, Tavener SA, et al. Platelet TLR4 activates neutrophil extracellular traps to ensnare bacteria in septic blood[J]. Nat Med, 2007, 13(4): 463-469.
[33] Klinger MH, Jelkmann W. Role of blood platelets in infection and inflammation[J]. J Interferon Cytokine Res, 2002, 22(9): 913-922.
[34] Ma AC, Kubes P. Platelets, neutrophils, and neutrophil extracellular traps (NET) in sepsis[J]. J Thromb Haemost, 2008, 6(3): 415-420.
[35] Kambas K, Mitroulis I, Apostolidou E, et al. Autophagy mediates the delivery of thrombogenic tissue factor to neutrophil extracellular traps in human sepsis[J]. PLoS One, 2012, 7(9): e45427.
[36] Yang S, Qi H, Kan K, et al. Neutrophil Extracellular Traps Promote Hypercoagulability in Patients With Sepsis[J]. SHOCK, 2017, 47(2): 132-139.
[37] Engelmann B, Massberg S. Thrombosis as an intravascular effector of innate immunity[J]. Nature reviews Immunology, 2013, 13(1): 34-45.
[38] Loof TG, Morgelin M, Johansson L, et al. Coagulation, an ancestral serine protease cascade, exerts a novel function in early immune defense[J]. Blood, 2011, 118(9): 2589-2598.
[39] Kimball AS, Obi AT, Diaz JA, et al. The Emerging Role of NET in Venous Thrombosis and Immunothrombosis[J]. Front Immunol, 2016, 7: 236.
[40]
[41] Shatzel JJ, Taylor JA. Syndromes of Thrombotic Microangiopathy[J]. Med Clin North Am, 2017, 101(2): 395-415.
[42] Ramos MV, Mejias MP, Sabbione F, et al. Induction of Neutrophil Extracellular Traps in Shiga Toxin-Associated Hemolytic Uremic Syndrome[J]. J Innate Immun, 2016, 8(4): 400-411.
[43] Leffler J, Prohászka Z, Mikes B, et al. Decreased Neutrophil Extracellular Trap Degradation in Shiga Toxin-Associated Haemolytic Uraemic Syndrome[J]. J Innate Immun, 2017, 9(1): 12-21.
[44] Arai Y, Yamashita K, Mizugishi K, et al. Serum Neutrophil Extracellular Trap Levels Predict Thrombotic Microangiopathy after Allogeneic Stem Cell Transplantation[J]. Biol Blood Marrow Transplant, 2013, 19(12): 1683-1689.
[45] Jimenez-Alcazar M, Napirei M, Panda R, et al. Impaired DNase1-mediated degradation of neutrophil extracellular traps is associated with acute thrombotic microangiopathies[J]. J Thromb Haemost, 2015, 13(5): 732-742.
[46] Chauhan AK, Motto DG, Lamb CB, et al. Systemic antithrombotic effects of ADAMTS13[J]. J Exp Med, 2006, 203(3): 767-776.
[47] Wong SL, Goverman J, Staudinger C, et al. Recombinant human ADAMTS13 treatment and anti-NET strategies enhance skin allograft survival in mice[J]. Am J Transplant, 2020, 20(4): 1162-1169.
[48] Barnado A, Crofford LJ, Oates JC. At the Bedside: Neutrophil extracellular traps (NET) as targets for biomarkers and therapies in autoimmune diseases[J]. J Leukoc Biol, 2016, 99(2): 265-278.
[49] Yalavarthi S, Gould TJ, Rao AN, et al. Antiphospholipid Antibodies Promote the Release of Neutrophil Extracellular Traps: A New Mechanism of Thrombosis in the Antiphospholipid Syndrome[J]. Arthritis Rheumatol, 2015, 67(11): 2990-3003.
[50] Yuen J, Pluthero FG, Douda DN, et al. NETosing Neutrophils Activate Complement Both on Their Own NET and Bacteria via Alternative and Non-alternative Pathways[J]. Front Immunol, 2016, 7: 137.
[51] Pierangeli SS, Girardi G, Vega-Ostertag M, et al. Requirement of activation of complement C3 and C5 for antiphospholipid antibody-mediated thrombophilia[J]. Arthritis Rheum, 2005,52(7):2120-2124.
[52] Mizuno T, Yoshioka K, Mizuno M, et al. Complement component 5 promotes lethal thrombosis[J]. Sci Rep, 2017, 7: 42714.
[53] Wiedmer T, Esmon CT, Sims PJ. On the mechanism by which complement proteins C5b-9 increase platelet prothrombinase activity[J]. J Biol Chem, 1986, 261(31): 14587.
[54] Guglietta S, Chiavelli A, Zagato E, et al. Coagulation induced by C3aR-dependent NETosis drives protumorigenic neutrophils during small intestinal tumorigenesis[J]. Nat Commun, 2016, 7: 11037.
[55] Palmer LJ, Damgaard C, Holmstrup P, et al. Influence of complement on neutrophil extracellular trap release induced by bacteria[J]. J Periodontal Res, 2016, 51(1): 70-76.
[56] de Bont CM, Boelens WC, Pruijn GJM. NETosis, complement, and coagulation: a triangular relationship[J]. Cell Mol Immunol, 2019, 16(1): 19-27.
[57] Jiménez-Alcázar M, Rangaswamy C, Panda R, et al. Host DNases prevent vascular occlusion by neutrophil extracellular traps[J]. Science, 2017, 358(6367): 1202-1206.
