胃癌是世界上最常见的恶性肿瘤,每年新发胃癌病例约100万[1]。胃癌患者确诊时,通常已经处于进展期[2]。其病死率高居癌症相关病死率的第3位[1]。就全球范围而言,无论在其发病率、病死率、还是在治疗效果方面,均体现了地域差异[3,4]。胃癌患者的生存预后在东西方地域存在的差别,主要是由于肿瘤分期标准存在差异。准确的肿瘤分期对胃癌个体化治疗方案的制定和预后判断具有重要的指导意义[5]。与其他肿瘤类似,TNM分期系统是对胃癌进行分期的金标准。新出的第八版胃癌TNM分期系统是基于对全球多个国家的胃癌数据进行分析、进而对旧的分期标准进行评价和更新而来,因此,具有普遍的代表性和国际通用性。第八版TNM分期除了对病理TNM (pTNM)分期标准做了较大变动以外,还新增加了胃癌临床TNM (cTNM)分期和新辅助治疗后TNM (ypTNM)分期标准。本文将对新的胃癌分期系统变更的内容进行讨论和解读。
第七版胃癌TNM分期系统于2009年制定并于2010年颁布[6,7,8]。所采用的数据主要来自于欧美的食管癌数据以及日本和韩国的胃癌数据。因此,该分期不能全面反映全球胃癌病例的真实情况,不具有代表性。由于日本首次参与了第七版的修订工作。因此,在日本胃癌协会(Japanese Gastric Cancer Association,JCGC)的建议下,由国际胃癌协会(International Gastric Cancer Association,IGCA)于2009年发起并设立专门的胃癌分期研究项目,旨在通过收集全球的胃癌病例数据并进行分析,为新版的TNM分期提供更为客观的数据支持,使新的TNM分期系统更具有国际代表性。在2011年4月韩国首尔举办的第9届国际胃癌大会上,IGCA理事会讨论了该项目的具体实施细节,日本Sano教授被任命为项目主要研究者(principal investigator,PI)。在美国癌症联合委员会(American Joint Committee on Cancer,AJCC )、国际抗癌协会(International Union for Cancer Control,UICC)和国际胃癌协会(International Gastric Cancer Association,IGCA)的共同协作和推动下,最终从全球15个国家59个中心(医院/研究所)回顾性收集了2000—2004年间采取手术治疗并有至少5年以上完整随访资料的胃癌患者共计25 411例,其中日本、韩国和其他亚洲国际以及西方国家分别占41.8%、43.0%、6.4%和8.8%[6]。通过对所纳入的数据进行分析,为新版TNM分期提供了数据支持和客观依据,使得胃癌TNM分期更加国际化。第八版肿瘤分期指南已经于2016年底出版[9]。据AJCC官方网站消息,新版TNM分期系统将于2018年1月开始实施,在此之前,仍然使用第七版TNM分期系统。
(1)肿瘤侵及胃食管交界线,且肿瘤中心位于胃食管交界线以下< 2 cm,则按照食管癌的分期系统进行分期;(2)肿瘤未侵犯胃食管交界线,且肿瘤中心位于胃食管交界线以下2 cm,则按照胃癌的分期系统进行分期;(3)肿瘤侵犯胃食管交界线,且肿瘤中心位于胃食管交界线> 2 cm,则按照胃癌的分期系统进行分期。
将N3分期细分成N3a和N3b两个亚群并纳入TNM分期系统。
新增的cTNM分期不同于pTNM分期。
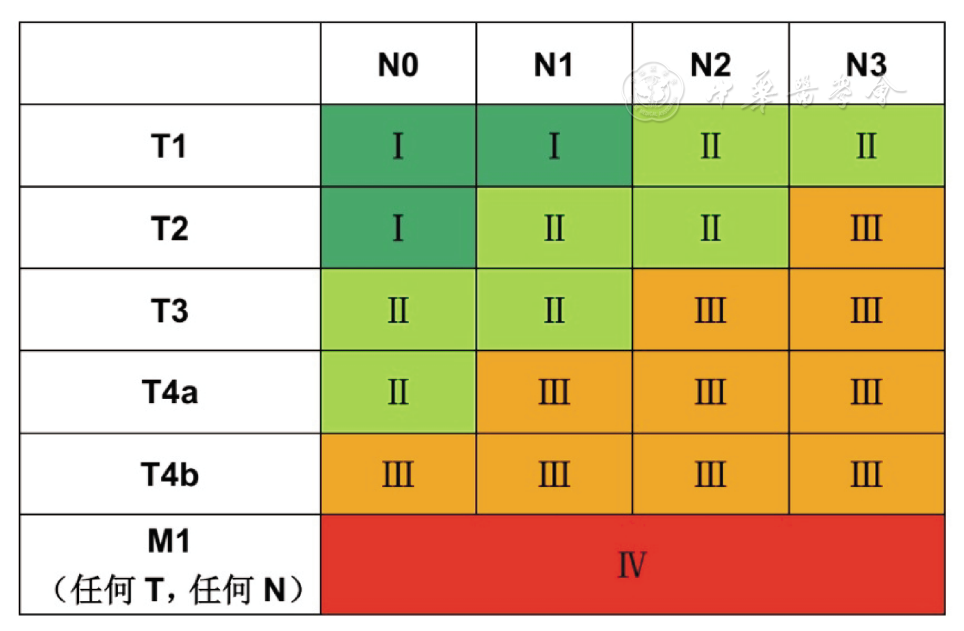
新增的ypTNM分期与pTNM分期类似,但是仅划分了4个大的分期(Ⅰ至Ⅳ期)。
将T4aN2M0期和T4bN0M0期由第七版的ⅢB期调整为ⅢA期。
以胃食管交界线为中心,以上5 cm(远端食管)和以下5 cm(近端胃)之间的这10 cm,是一直存在争议的区域。该区域的癌称作胃食管结合部癌。对其进行合适的分期及诊治模式的选择也成为新的研究热点。该部位肿瘤按照食管癌分期系统进行分期、还是按照胃癌的分期系统进行分期,对于指导临床治疗决策的选择和预后判断有重要的意义。
第七版TNM分期系统中,肿瘤中心位于胃食管交界线下5 cm以内并且肿瘤侵及胃食管交界线或食管下段,均按照食管癌分期系统进行分期。肿瘤位于胃食管交界线下5 cm以内,但是向上没有侵及胃食管交界线或食管下段,或者肿瘤中心位于胃食管交界线下>5 cm的胃部肿瘤均按照胃癌分期系统进行分期。
但是Sano教授等[6]通过对来自全球15个国家的1 170例胃食管结合部癌中的SiewertⅡ型和Ⅲ型病例分别按照第七版食管癌、胃癌以及IGCA胃癌TNM分期系统进行生存分析并绘制生存曲线的结果显示,按照食管癌的分期系统分期,约有40%的患者被划分到了ⅢC期,同时ⅡA期和ⅡB期患者的生存曲线是颠倒的,即ⅡB期患者的预后比ⅡA期患者要好,这显然不符合常理。按照胃癌分期系统分期的话,各分期的生存曲线分布较为合理。按照IGCA分期系统进行分期后,各分期的生存曲线分布更加合理。因此,需要重新划分解剖界限,从而使胃食管结合部肿瘤的分期标准选择更为准确。
在第八版TNM分期系统中,将胃食管结合部癌的分期标准选择进行了重新明确。肿瘤中心在胃食管交界线下< 2 cm,且肿瘤侵及胃食管交界线,则按照食管癌分期系统进行分期。如果肿瘤中心在胃食管交界线以下< 2 cm,但肿瘤未向上侵及胃食管交界线或肿瘤中心距离胃食管交界线以下> 2 cm、向上侵及胃食管交界线者,则按照胃癌TNM分期系统进行分期。见图1。
当患者确诊胃癌时,需要进一步行相关的检验和检查,为患者临床分期的评定提供参考依据。对胃癌进行临床分期有助于指导医生制定初步的治疗方案。既往没有正式的临床分期系统,医生常常套用pTNM分期标准进行cTNM分期。这种分期方式显然不合适,其有效性也尚未得到验证,一定程度上有可能还会错误引导临床治疗策略的选择。准确的临床分期是制定个体化治疗方案的重要参考依据。为了满足临床诊疗需求,第八版胃癌TNM分期系统中新增加了胃癌cTNM分期,见图2。
在cT分期方面:其分期标准与pT分期类似。分别为:T1a (肿瘤侵犯黏膜固有层或黏膜肌层)和T1b(肿瘤侵犯黏膜下层);T2指肿瘤侵犯固有肌层;T3是指肿瘤侵犯至浆膜下层,但不侵犯邻近结构或脏层腹膜;T4是指肿瘤穿透浆膜(T4a)或侵犯邻近结构或器官(T4b)。但是,特别指出了内镜超声(endoscopic ultrasonography,EUS)在cT分期中的重要地位。尽管随着多层螺旋CT的设备和技术的改进、胃部充盈状态的改善、动态静脉注射对比增强剂的应用以及CT图像三维重建的应用,对cT分期的评估判断有了一定的改进和提高[10,11,12]。但是也存在一定的局限性,尤其是对cT1、cT2和cT3的判断。CT在判断肿瘤侵及周围邻近结构(cT4)方面也存在一定的局限性。PET-CT一般也不用来进行cT分期,主要是因为正常胃黏膜也可以摄取对比剂;另外,印戒细胞癌和低分化腺癌对于对比剂摄取低。MRI与CT相比,具有更高的分辨率,但是其对cT分期评估也有一定的局限性。因此,第八版的TNM分期系统中指出,EUS是判断胃癌cT分期最为理想的检查手段。
在cN分期方面:其分期标准也与pN类似,分别为N0(无区域淋巴结转移证据)、N1 (1~ 2个区域淋巴结转移)、N2(3~ 6个区域淋巴结转移)和N3(7个或7个以上区域淋巴结转移)。EUS有助于判断肿大的或有恶性表现的淋巴结,进而有助于cN分期的判定。虽然增强CT和PET-CT检查可以用来评估局部淋巴结转移情况(cN ),但是,第八版TNM分期中指出:单纯靠CT和PET-CT检查手段很容易出现假阳性结果。在评估局部淋巴结转移方面,CT和PET-CT不是最佳的。对于T分期较早的(pT1)胃癌来说,PET-CT对淋巴结转移情况的判定效能有限,主要因为早期胃癌淋巴结转移和远处转移率低,同时PET-CT假阳性率高。
在cM分期方面:基于影像学检查发现有远处转移(包括腹膜转移)则定义为cM1。通过诊断性腹腔镜探查、或腹腔冲洗液证实存在的腹膜转移则认为是远处转移阳性。特别强调:在诊断性腹腔镜探查发现肉眼可见的转移灶,则被定为cTcNcM1(临床Ⅳ期)。然而,诊断性腹腔镜探查未发现明确的转移灶,是腹腔冲洗液肿瘤脱落细胞阳性,则被定为cTcNpM1(病理分期Ⅳ期)。对于晚期胃癌、临床T3或N+的患者,应该考虑行腹腔镜下分期及腹膜冲洗[13]。这一点NCCN指南也明确指出。增强CT检查在判断cM分期时有一定的意义。PET-CT检查可以发现通过CT检查遗漏的转移灶。MRI不是常规检查手段。
近年来,随着新辅助化疗的不断兴起,其临床价值也得到了初步证实。但是,在对这类患者进行分期时,我们一直沿用pTNM分期系统,尚没有专门的新辅助治疗后的肿瘤分期系统。因此,为了满足临床需求,在第八版中,也重点提出了ypTNM分期系统。见图3。
新辅助治疗后的病理反应评估应包括对切除的标本大体肉眼检查和显微镜下检查。显微镜下,治疗有效体现在恶性上皮细胞被致密的纤维化组织或者纤维炎性组织代替。ypT分期判断主要决定于残存肿瘤细胞位于胃壁的最深层次。阳性淋巴结定义为至少淋巴结中含有1个残存肿瘤灶。对于行新辅助治疗的胃癌病例,术后病理报告应该体现ypT和ypN。如果怀疑有远处转移,也应将转移灶送病理检查进一步明确,在M分期上应该为ypM1。如果影像学等检查显示远处转移,但是没有病理学依据,则记录为cM1。
第七版分期虽然将N3期分成了N3a期和N3b期,但是并没有纳入TNM分期系统。由于Sano等[6]通过对来自于全球15个国家的大数据进行生存分析发现,N3a和N3b两个亚组的患者其生存期存在显著差异。因此,第八版分期系统中,将N3a和N3b两个亚群单独列出,并纳入了TNM分期系统。由于更新,导致胃癌患者分期分布也出现了改变,各组的生存曲线之间的差异也更为明显。主要体现在以下7个方面:(1)将原来的T1N3M0(ⅡB)更改为T1N3aM0(ⅡB)和T1N3bM0(ⅢB);(2)将原来的T2N3M0(ⅢA)更改为T2N3aM0(ⅢA)和T2N3bM0(ⅢB);(3)将原来的T3N3M0(ⅢB)更改为T3N3aM0(ⅢB)和T3N3bM0 (ⅢC);(4)将原来的T4aN3M0 (ⅢC)更改为T4aN3aM0 (ⅢB)和T4aN3bM0(Ⅲ C);(5)将原来的T4bN3M0 (ⅢC)拆分成T4bN3aM0 (ⅢC)和T4bN3bM0(ⅢC ),分期不变;(6)将原来的T4aN2M0和T4bN0M0由原来的ⅢB期调整为ⅢA期;(7)将原来的T4bN2M0由原来的ⅢC期改成ⅢB期。从上可以看出,将N3细分为N3a和N3b,并且纳入pTNM分期标准,导致胃癌pTNM分期出现了很大的变化,分期更加细化。这也表明,新版的pTNM分期更加准确,更能够比较精确判断患者预后,并对患者术后选择合理的治疗方案有重要的指导意义。见图4。
TNM分期是胃癌的临床治疗决策选择和预后判断的重要参考依据。准确的分期可以指导医生制定更为合理的治疗计划,并且更为科学地评价治疗方案的疗效,同时有助于预后评估的准确性。第八版TNM分期系统较第七版TNM分期系统,能够更加合理地反应患者预后情况。尤其是对胃食管结合部癌的TNM分期系统的更新,以及将N分期的N3a和N3b两个亚群纳入到TNM分期系统,使得新版的分期更能反应真实的患者预后情况。此外,新版TNM分期系统新增了cTNM分期和ypTNM分期,这对于针对不同的患者给出较为确切的分期具有重要的意义。
新版的胃癌TNM分期系统也存在不足之处,体现在如下几个方面:建立所需要的数据尽管来源于全球15个国家59个中心,但是日本和韩国的数据占了将近85%。因此,对研究的结果可能会产生一定的偏倚。此外,新版TNM分期系统的提出所依赖的数据来源于回顾性的数据,术后处理方面的信息不完整,并且缺少手术标本病理处理的标准方法,还需要进一步的前瞻性研究数据进行验证其科学性。
我们期待通过进一步选取全球更多国家、覆盖范围更为广泛、更具有代表性的大样本临床胃癌数据并结合医学分子生物学的发展来进行分期,使胃癌TNM分期系统不断更新和完善,为广大临床医生提供更为准确的分期标准。





胃癌TNM分期已经成为胃癌临床治疗决策的选择和预后判断的重要参考依据。第七版胃癌TNM分期系统于2009年出版并于2010年实施。但是,在第七版胃癌分期系统临床应用过程中,发现其存在一定的不足,使得该分期系统已经不能满足临床诊疗需求。因此,在美国癌症联合委员会(AJCC )、国际抗癌协会(UICC)和国际胃癌协会(IGCA)的共同协作和推动下,通过胃癌大数据的积累和分析,于2016年底出版了第八版胃癌TNM分期系统。新的分期系统明确定义了胃食管结合部癌选择食管癌TNM分期标准还是胃癌TNM分期标准。将N3期细分成N3a期和N3b期,并将其纳入了TNM分期系统,使得新版的分期更加精确,更能反应真实的胃癌预后情况。此外,新版TNM分期系统还新增了胃癌临床TNM (cTNM)分期标准和新辅助治疗后TNM (ypTNM)分期标准。总之,第八版胃癌TNM分期系统可以指导医生制定更加合理的治疗方案,更为科学地评价治疗方案的疗效,同时有助于预后评估的准确性。对推动胃癌诊疗水平的提高有重要指导价值。